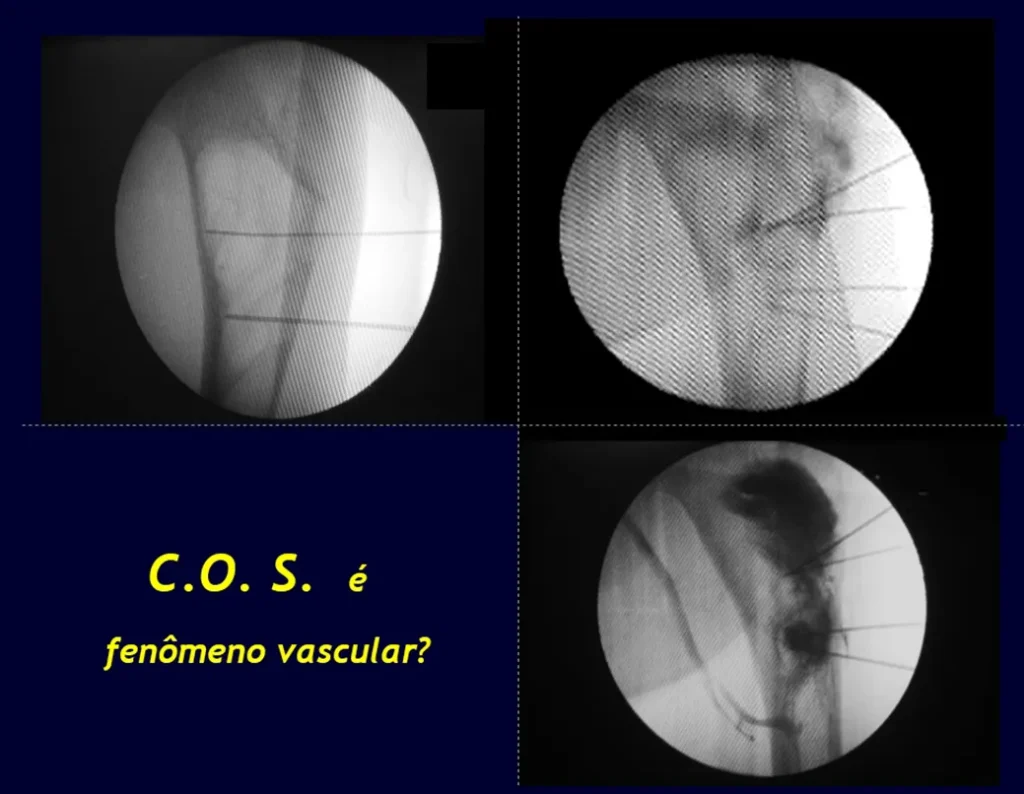
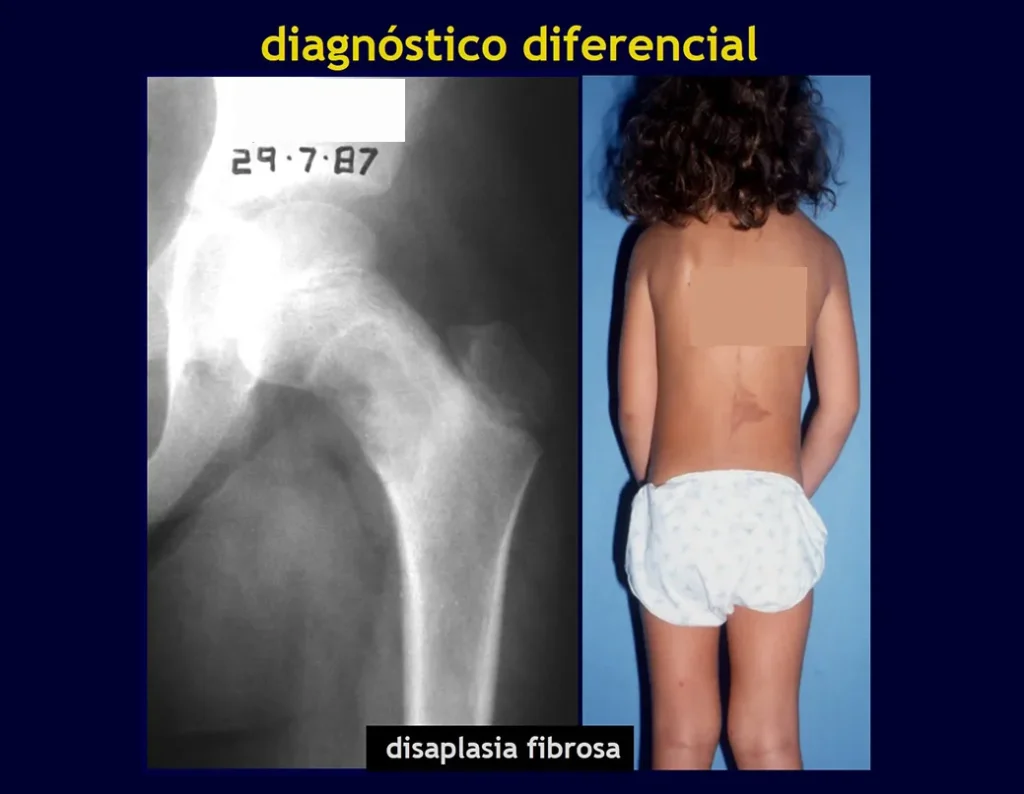
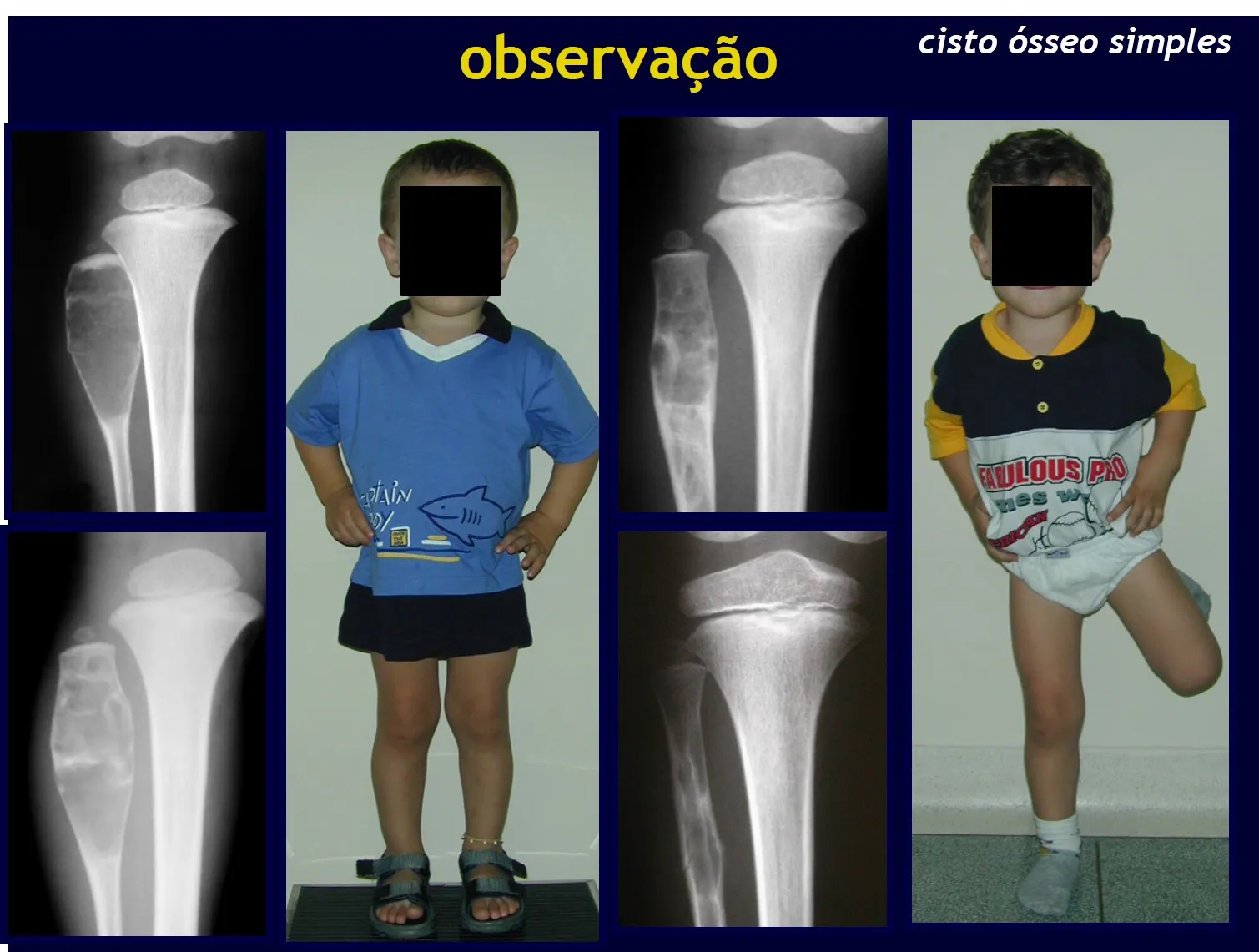
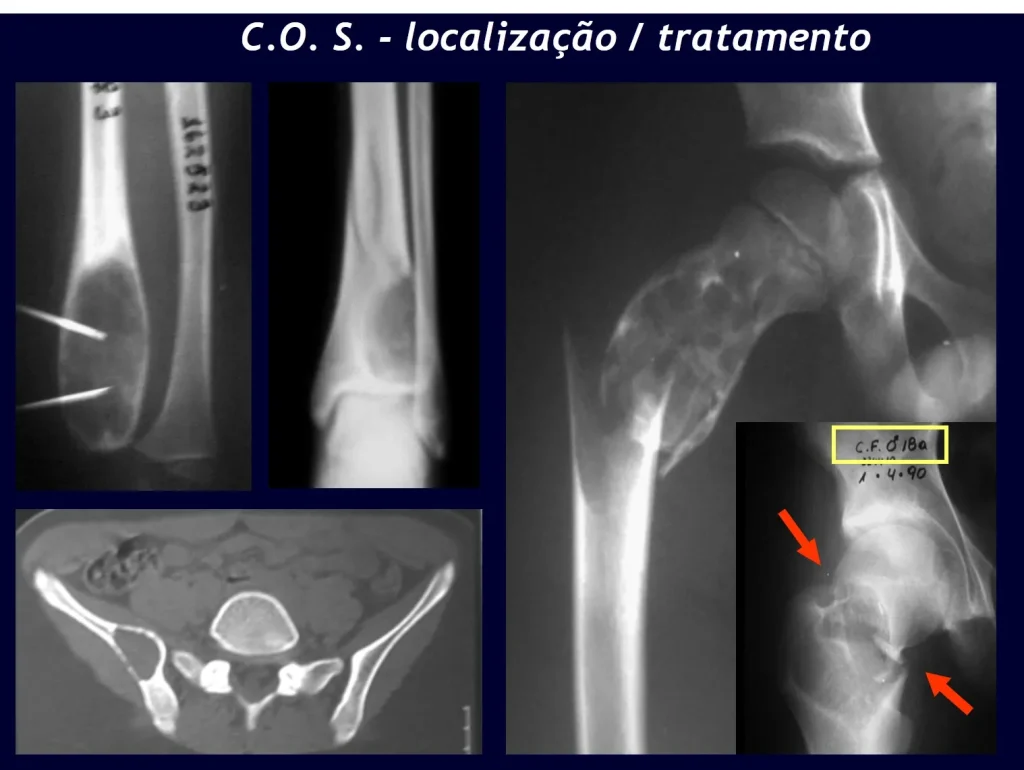
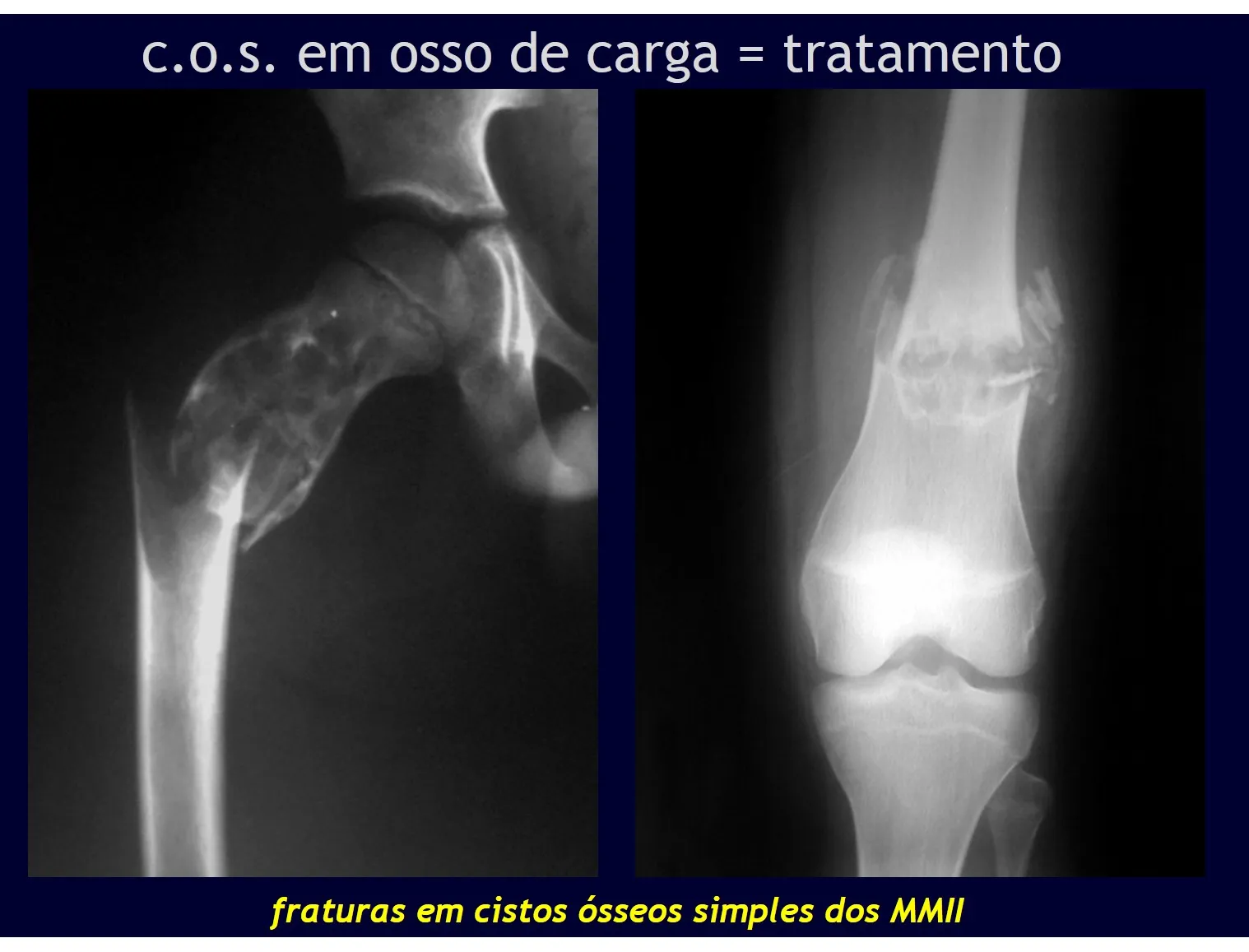
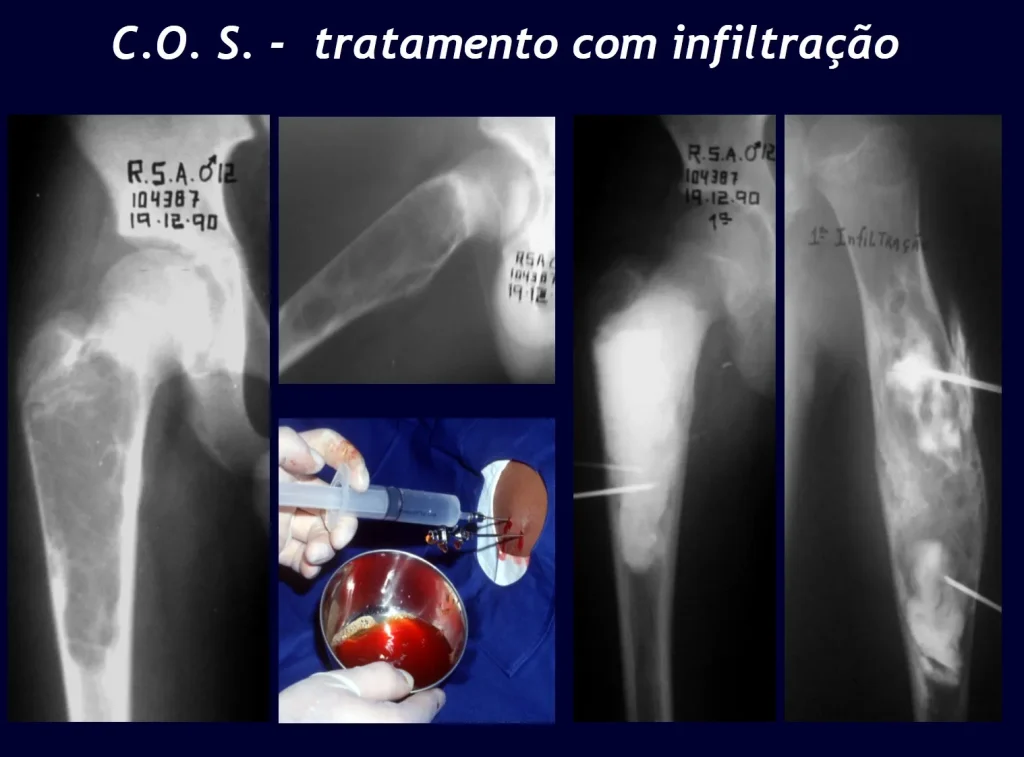
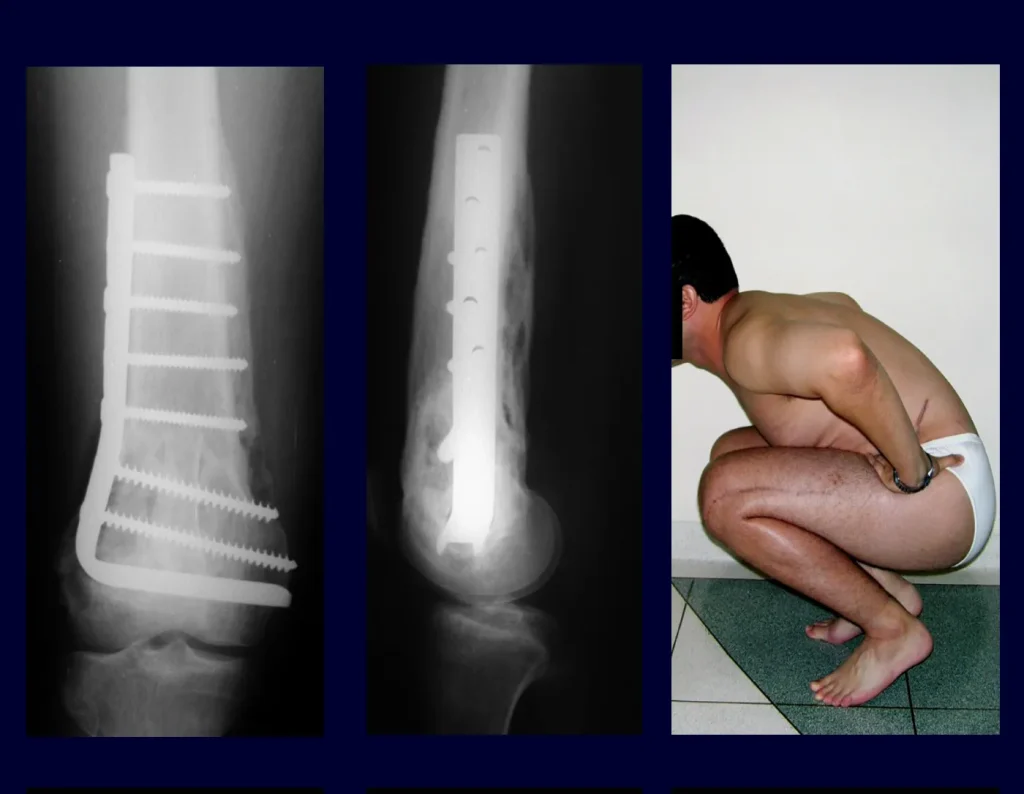
Nas lesões únicas o tratamento é a curetagem e enxerto ósseo quando necessário.
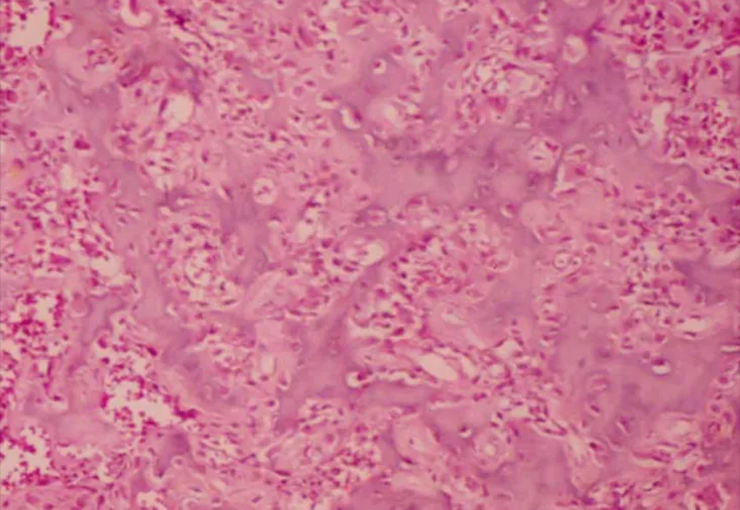
Definição: Lesão não neoplásica de etiologia desconhecida, caracterizada por uma intensa proliferação de elementos retículo histiocitários com variável número de eosinófilos, neutrófilos, linfócitos, plasmócitos e células gigantes multinucleadas. Freqüentes zonas de necrose, como também a presença de células gordurosas, especialmente em lesões antigas e múltiplas.
Incidência: A reticuloendoteliose apresenta várias formas de comprometimento, porém divide-se principalmente em três formas básicas: Granuloma Eosinófilo (75%), Hand-Schuller-Christian (15%) e Letterer-Siwe (10%).
Granuloma Eosinofílico: 5 a 20 anos
Hand-Schuller-Christian: 3 a 5 anos
Letterer-Siwe: 1 a 3 anos
Etiologia: A Reticuloendoteliose não tem uma etiologia conhecida, entretanto alguns autores a relacionam com uma provável causa viral ou imunológica, devido a presença de um fenômeno inflamatório com formação de um processo granulomatoso hiperplásico, muitas vezes semelhante a processos neoplásicos.
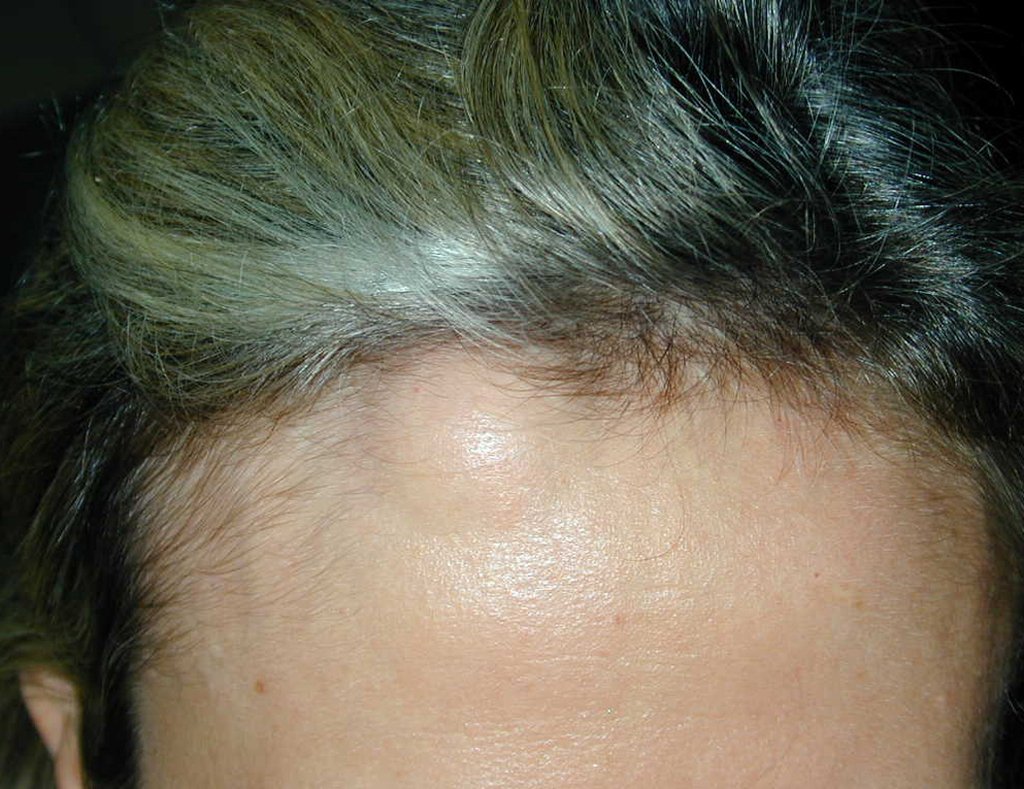
Manifestações Clínicas: A história natural da evolução dessa doença irá depender de umas das três formas em que ela se apresenta.
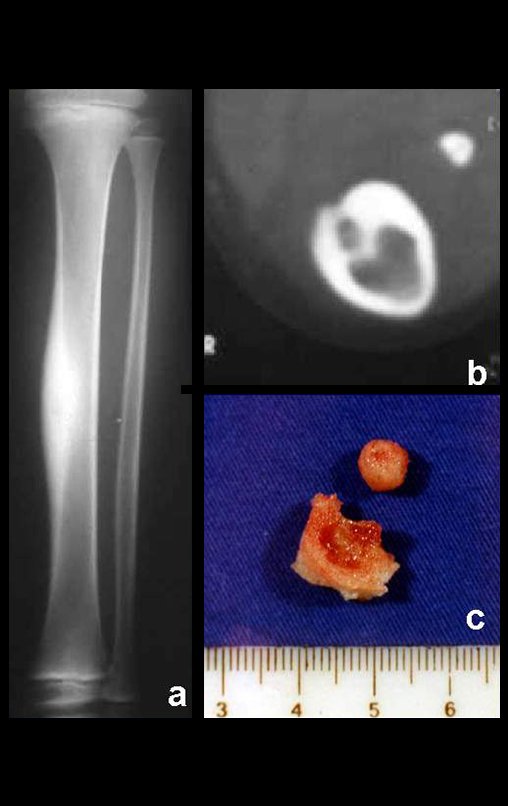
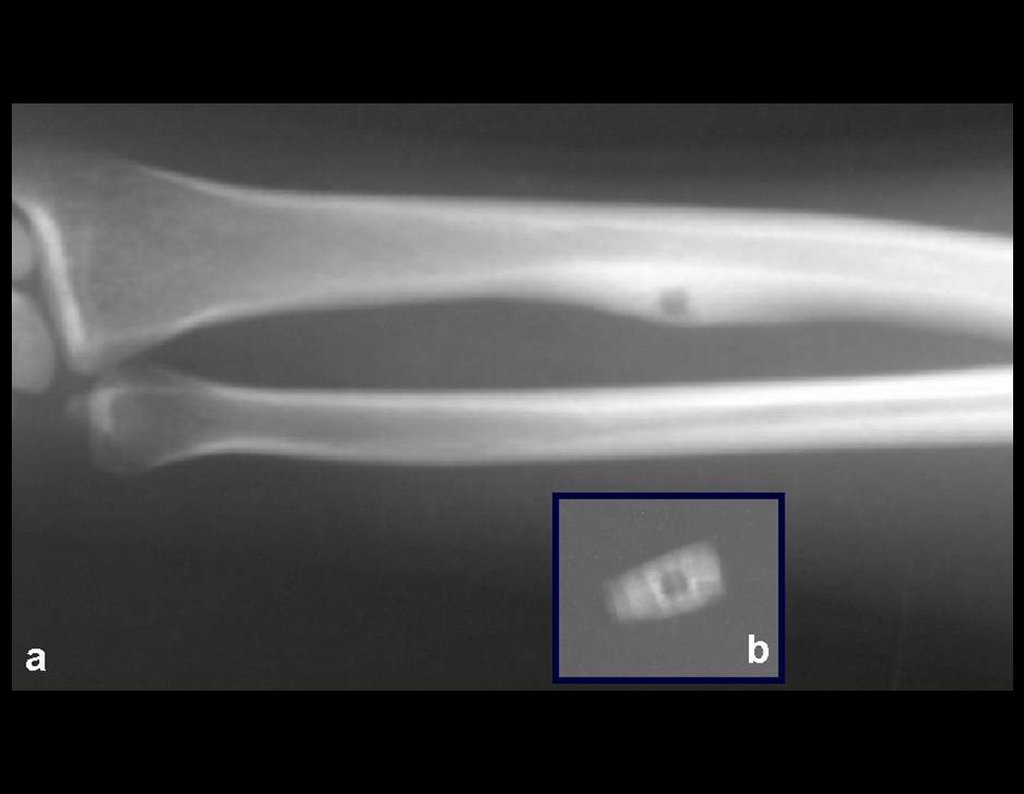
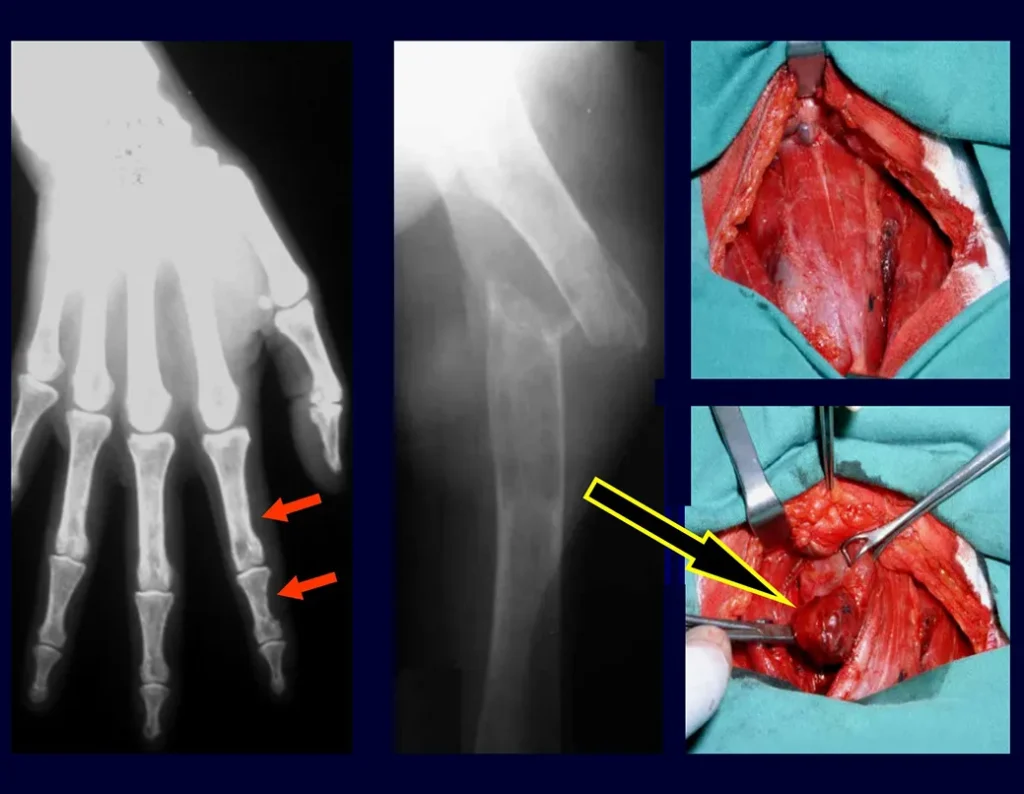
– Granuloma Eosinófilo: apresenta-se na grande maioria das vezes como uma lesão única acometendo preferencialmente a região diafisária e metafisária dos ossos longos, e de forma mais rara observamos também casos com comprometimento múltiplo, podendo ser simultâneo ou consecutivos iniciando o quadro na adolescência e arrastando-se até a vida adulta jovem. As lesãos únicas muitas vezes acabam tendo uma resolução espontânea ao longo do tempo, variando de meses a anos, sendo que raramente são incapacitantes ou levam a um quadro de fratura patológica.
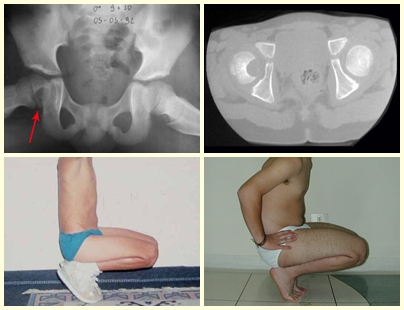
– Hand-Schuller-Christian : apresenta-se normalmente com múltiplas lesões, e sendo essas mais difíceis de serem tratadas e evoluem de forma mais incapacitante do que o do Granuloma Eosinofílico. Apresentam freqüentemente comprometimento secundário de outros tecidos, evoluem freqüentemente para Diabetes insipidus (comprometimento do glândula parapituitária), exoftalmia pelo comprometimento da órbita e comprometimentos do fígado e baço.
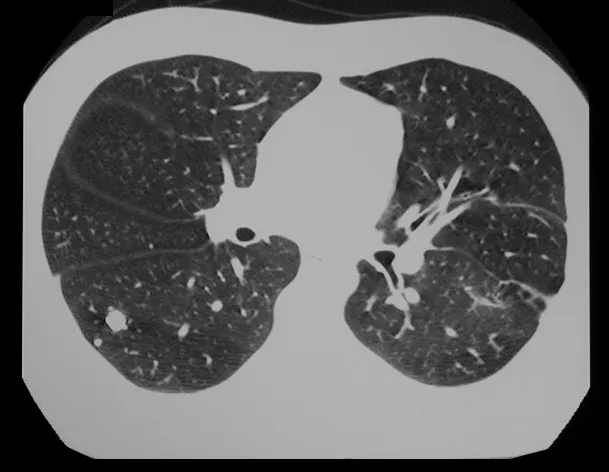
– Letterer-Siwe: os achados clínicos mais freqüentes são a febre, otite média e história freqüente de infecções bacterianas, e em alguns casos observa a anemia, hepatoesplenomegalia, quadros de hemorragia sem causa aparente, linfoadenopatia e lesões ósseas disseminadas. A evolução é freqüentemente fatal devido ao comprometimento sistêmico.
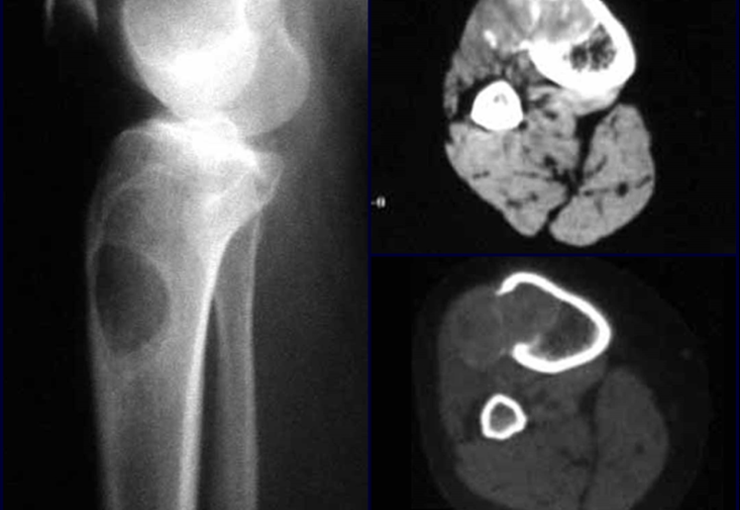
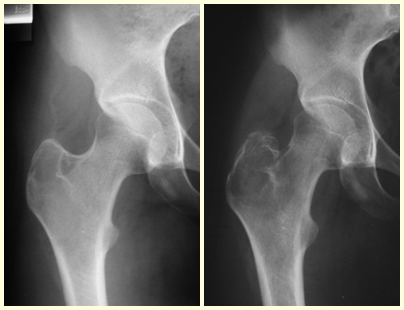
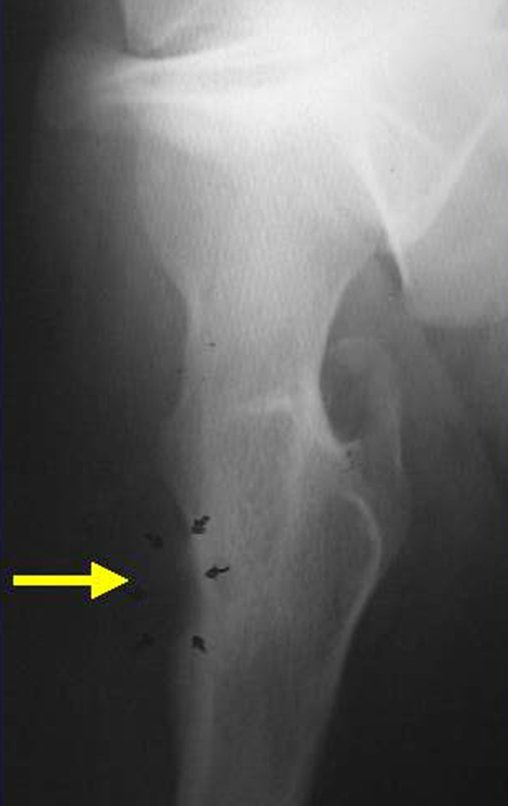
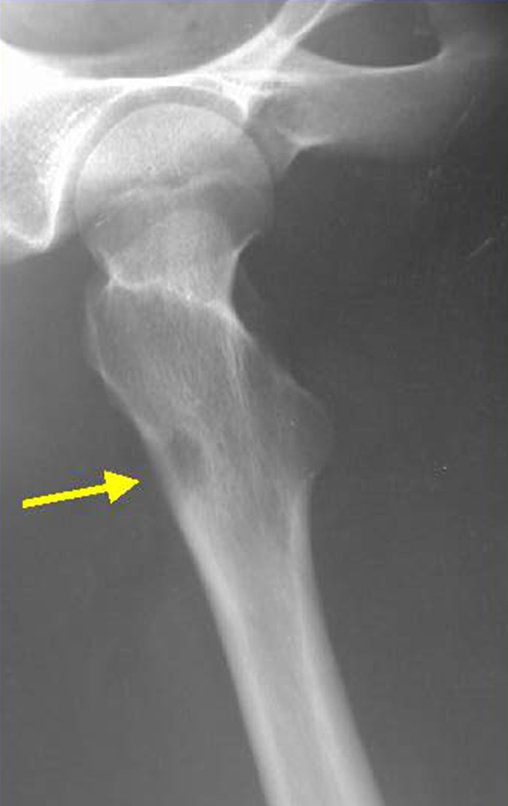
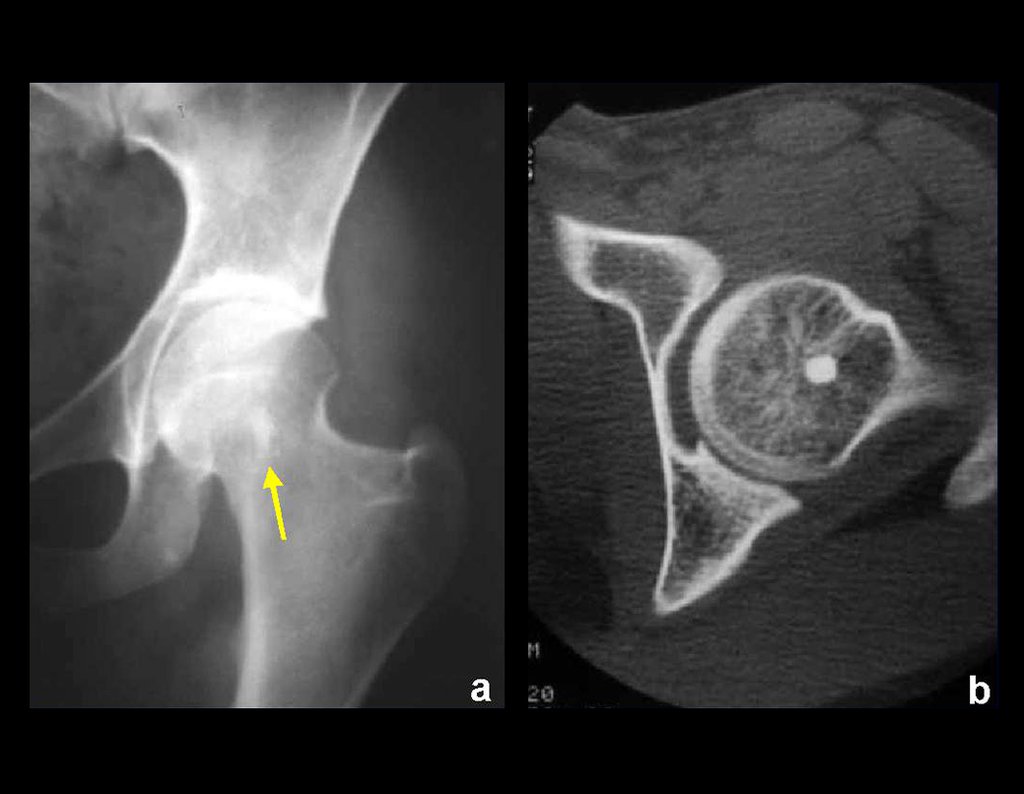
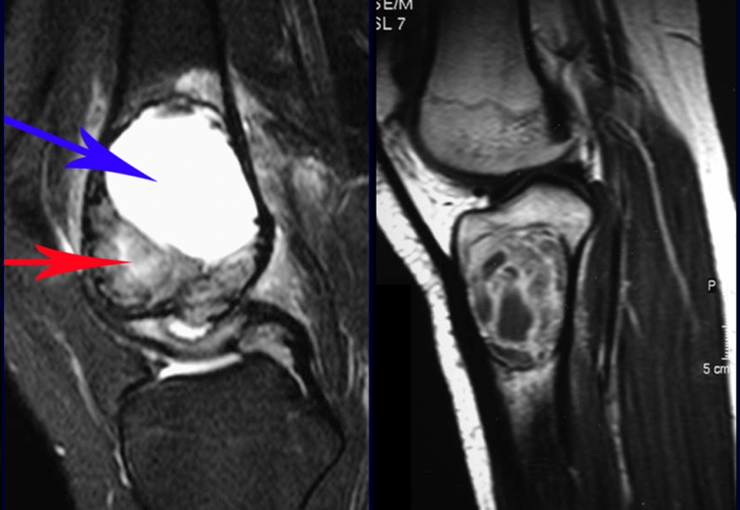
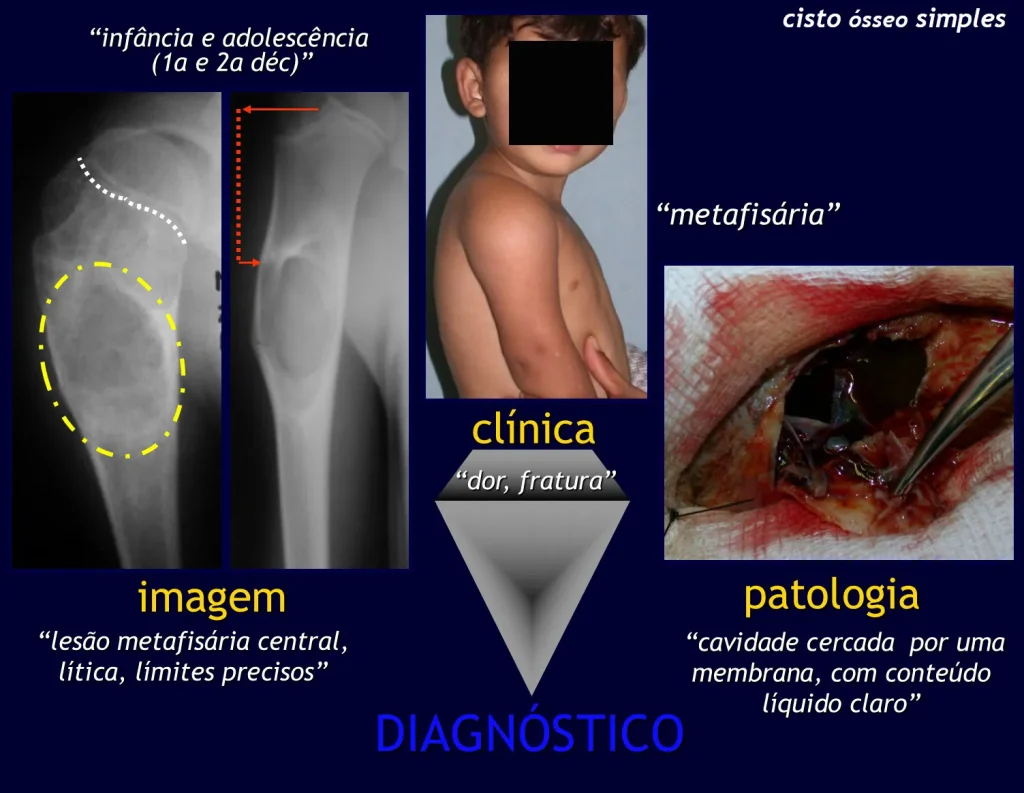
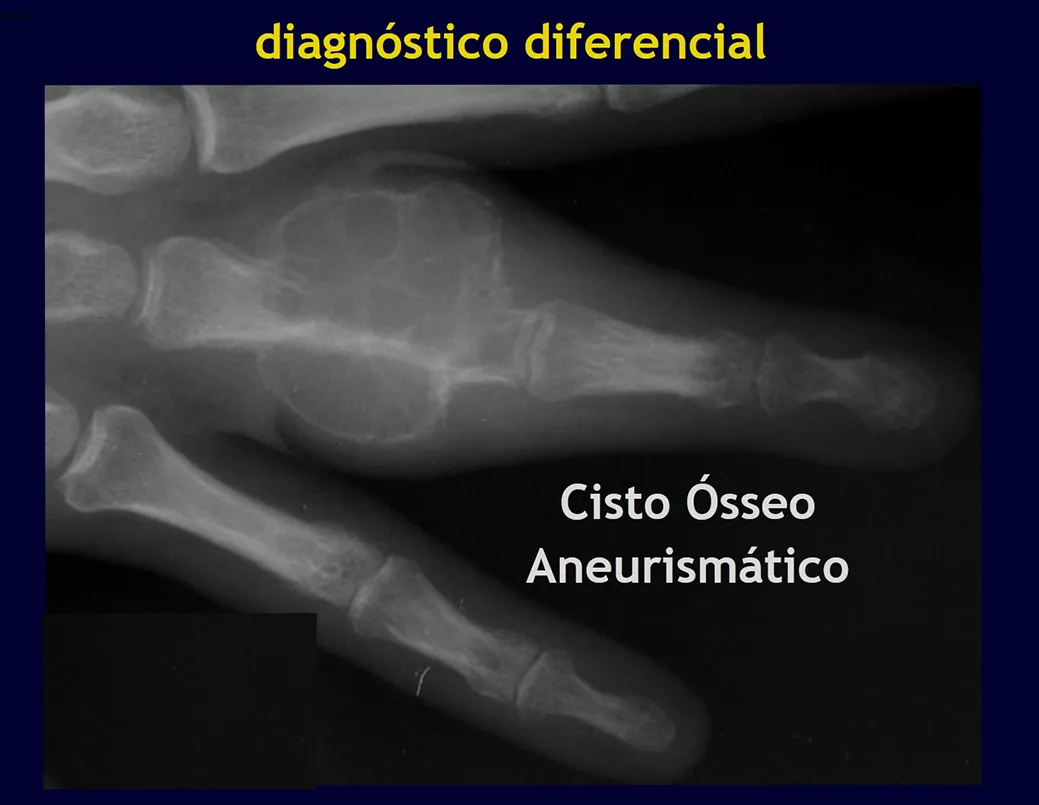
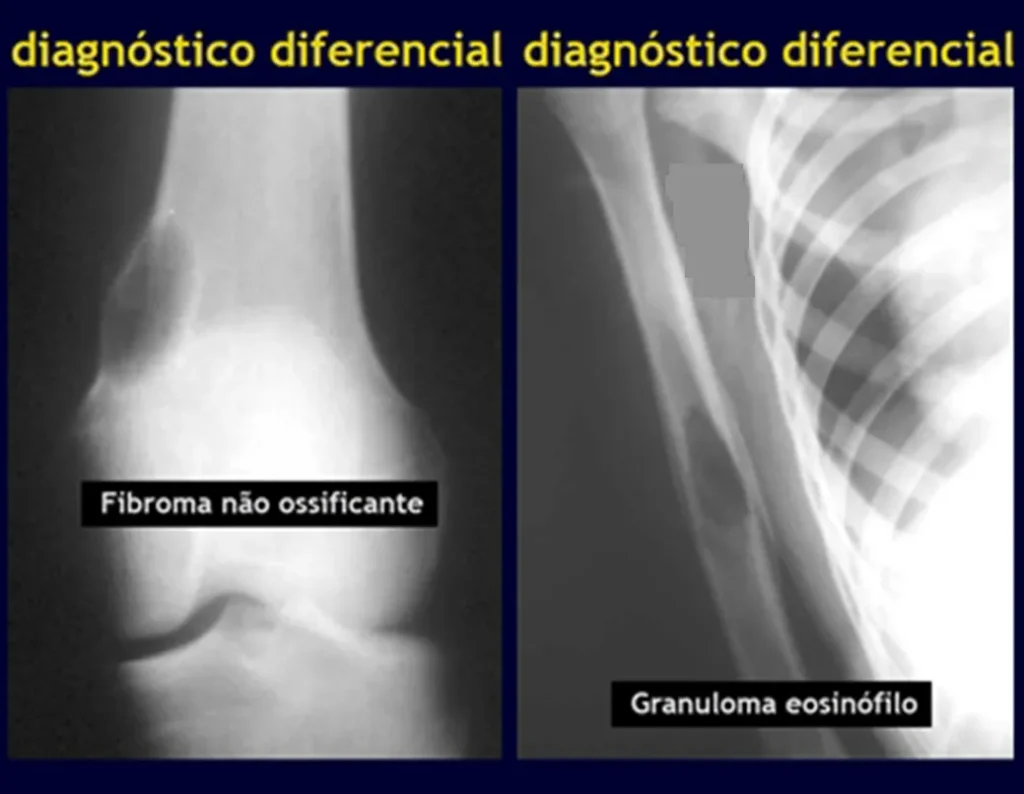
Aspectos Radiográficos: As lesões apresentam um aspecto radio transparente, com formato arredondado e ovoide, com bordos bem delimitados e bem definidos, e freqüentemente trabéculas no seu interior podem ser visíveis. Acometem freqüentemente a região diafisária de ossos longos e de forma menos comum na região metafisária, causando uma erosão da cortical e discreta expansão da cortical. É possível visualizar um pequeno levantamento periostal com reação em tipo “casca de cebola” semelhante ao do Sarcoma de Ewing e a osteomielite.
Quando o comprometimento é na coluna raramente leva a um comprometimento neurológico, embora haja um colapso da vértebra, apresentando um aplanamento e conhecido como “vértebra plana de Calvé”.
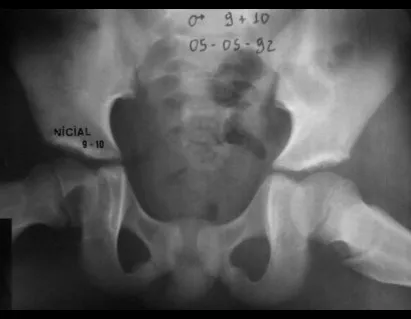
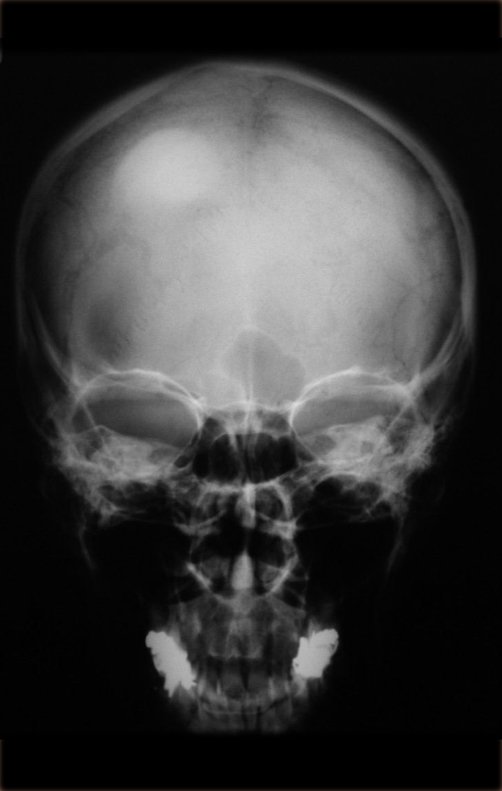
Em casos mais graves como na Síndrome de Hand-Schüller-Christian e Síndrome de Letterer-Siwe observam-se lesões radio transparentes disseminadas na calota craniana.
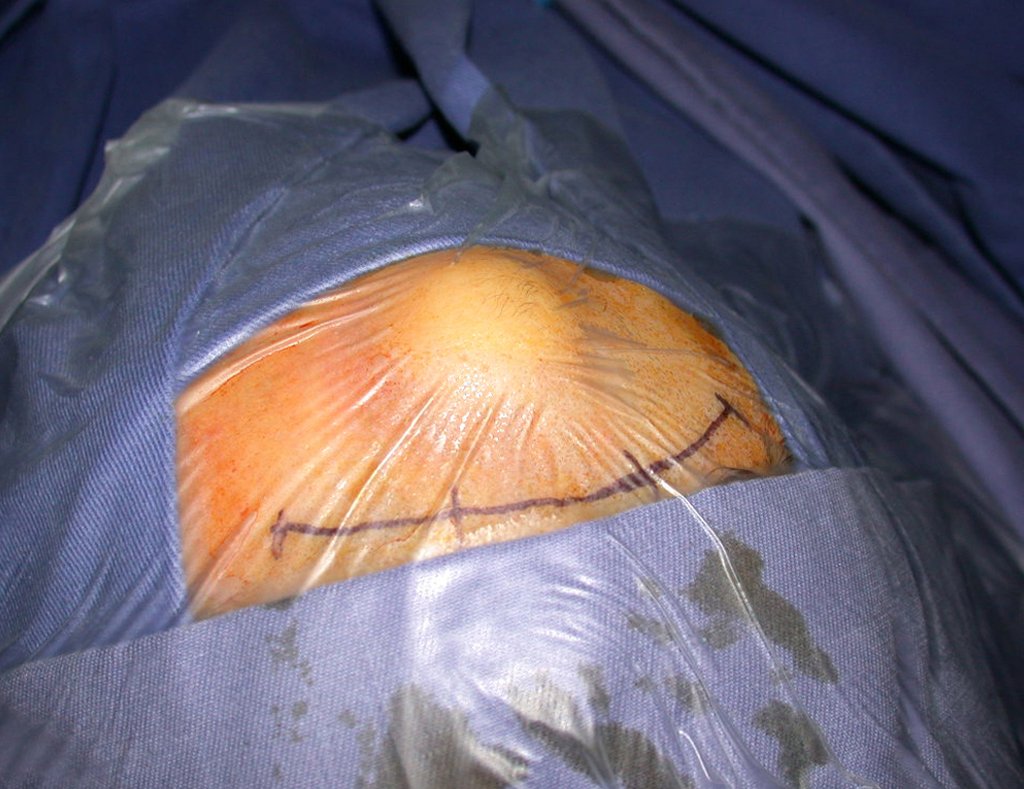
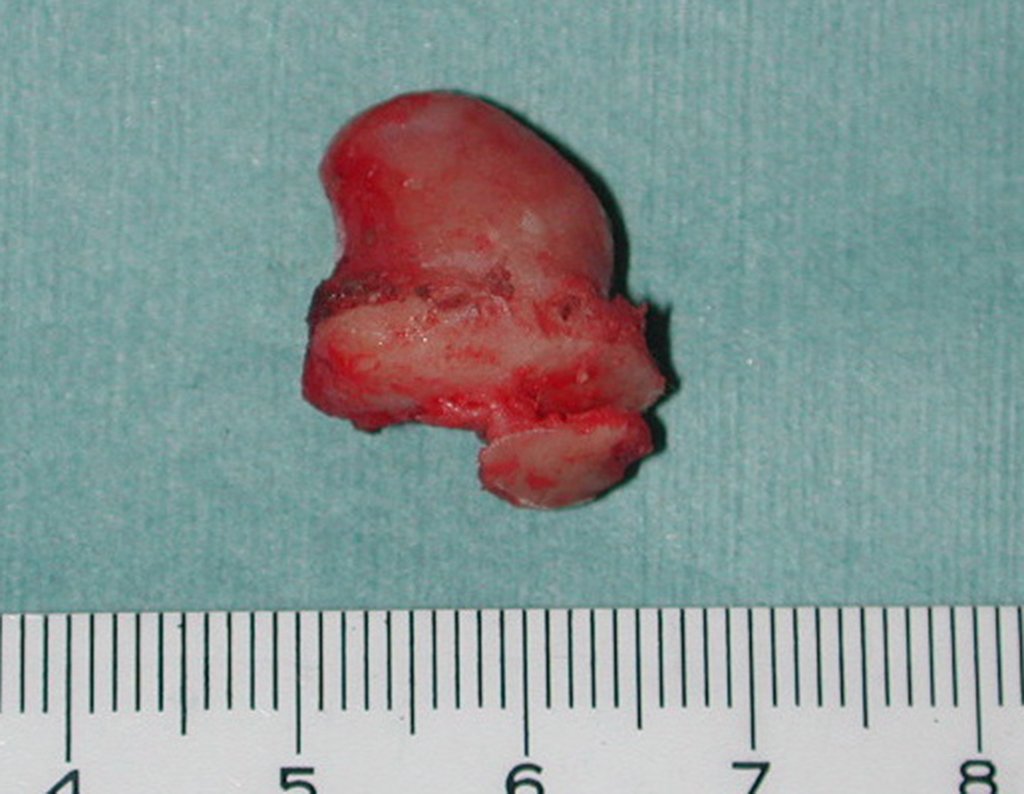
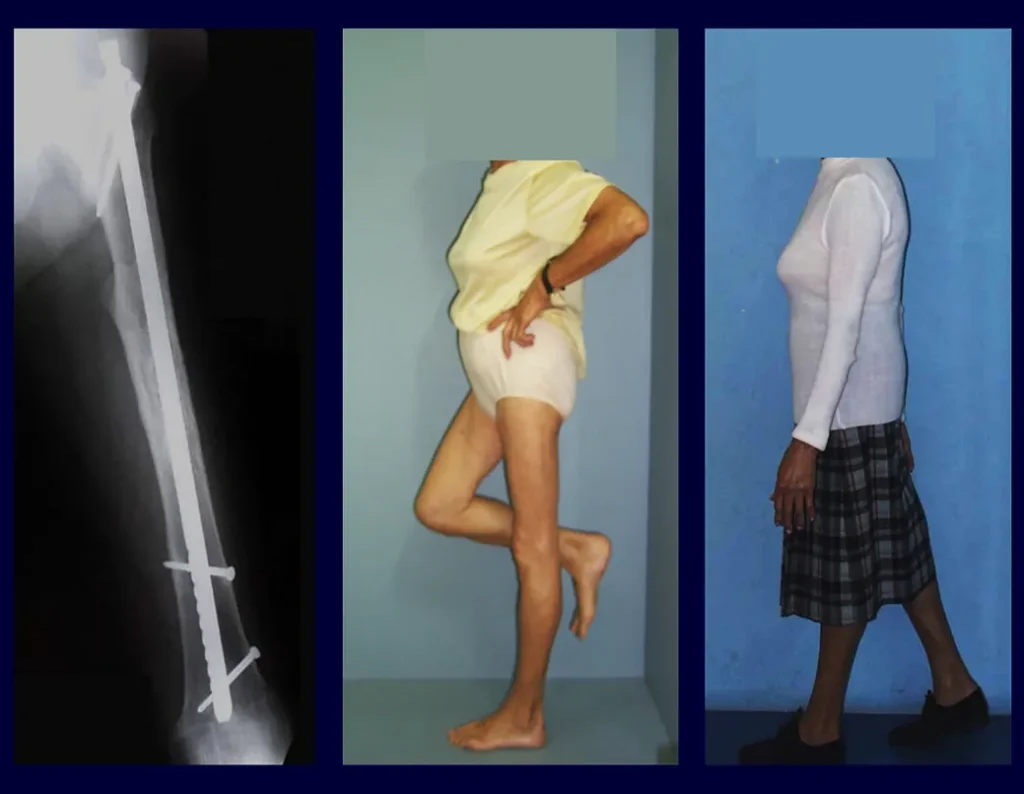
Tratamento e Prognóstico: O tratamento e o prognóstico da doença dependem diretamente do grau de comprometimento e das manifestações clínicas. Nas lesões únicas o tratamento de escolha é a curetagem e nas grandes falhas o preenchimento com osso esponjoso. Em alguns casos onde não há qualquer prejuízo da função ou comprometimento estético pode-se realizar a ressecção do osso comprometido, tais como costelas, clavícula, e parte superior da fíbula. Em casos de comprometimento múltiplos e sistêmicos parte do tratamento é realizado com uso de drogas quimioterápicas e corticoterapia.
1- Clique para ver mais: http://bit.ly/granuloma_eosinófilo-por
2- Caso de granuloma eosinófilo poliostótico: http://bit.ly/Granuloma_Eosinófilo_do-Rádio
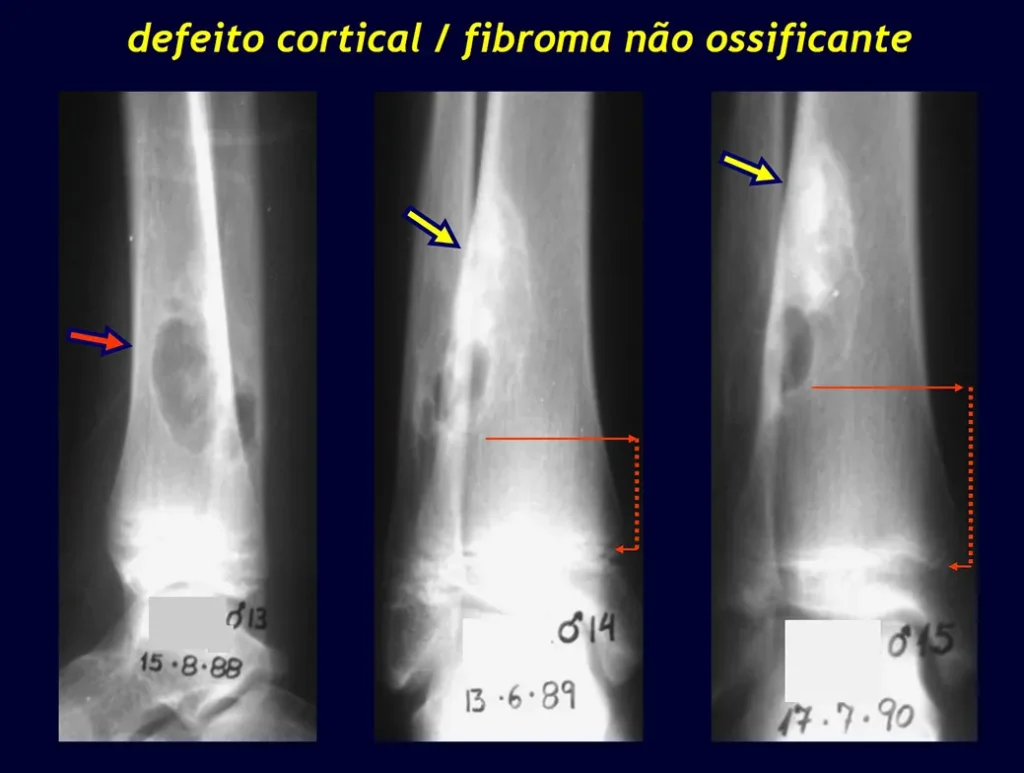
Defeito fibroso cortical / Fibroma não ossificante
O defeito fibroso cortical é lesão óssea benigna não-neoplásica, de causa desconhecida, que se caracteriza por proliferação fibrosa em pequena área de osso cortical. O fibroma não ossificante é o mesmo processo, com maior tamanho.
O defeito fibroso cortical geralmente não apresenta qualquer sintoma ou sinal clínico. Na grande maioria das vezes é diagnosticado em exame radiográfico realizado por algum motivo. Quando assume caracteres do fibroma não ossificante pode se manifestar por leve dor, saliência perceptível pelo paciente ou, menos freqüentemente, por fratura.