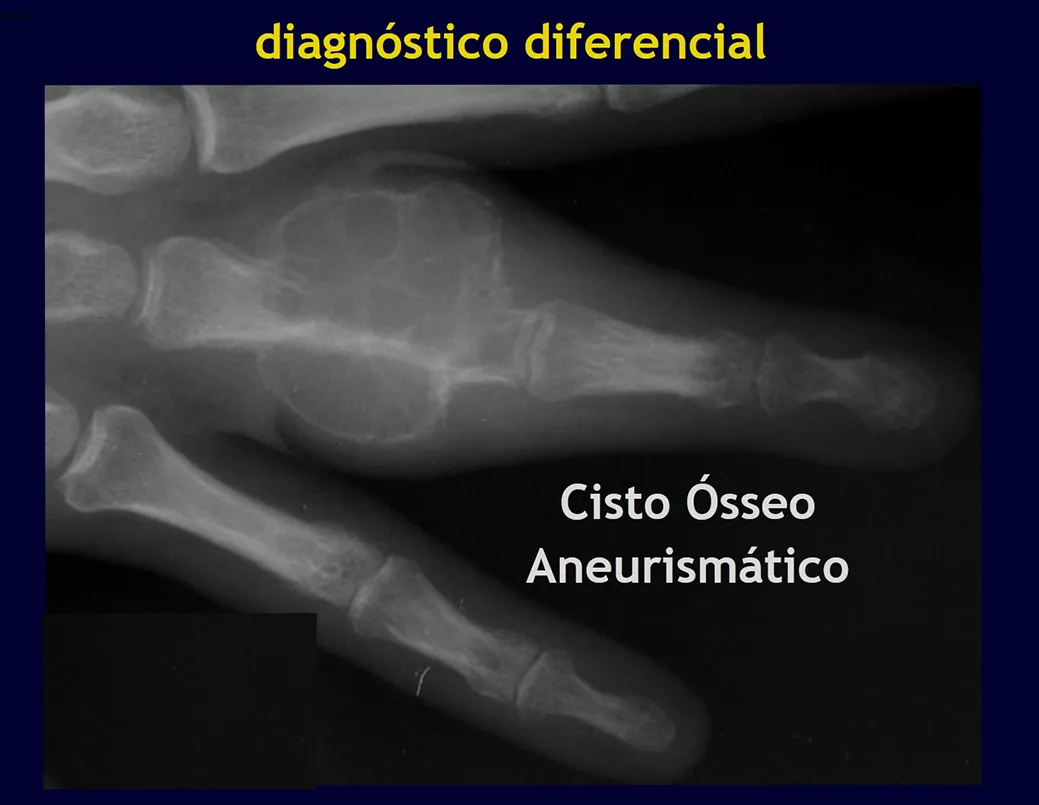
Cisto Ósseo Aneurismático
O Cisto ósseo aneurismático (C.O.A.) pertence ao grupo das lesões ósseas pseudotumorais. Este conjunto de doenças produzem alterações ósseas que mimetizam as lesões tumorais, do ponto de vista de imagem radiográfica.
Cisto Ósseo Aneurismático
As lesões que fazem parte deste grupo são:
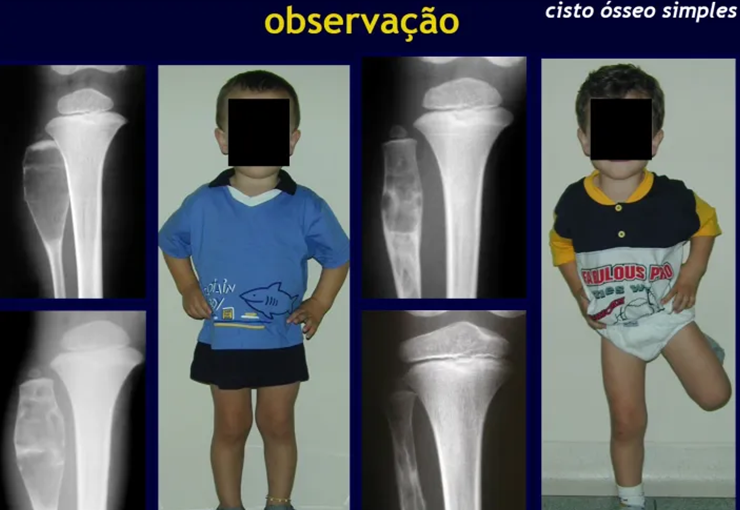
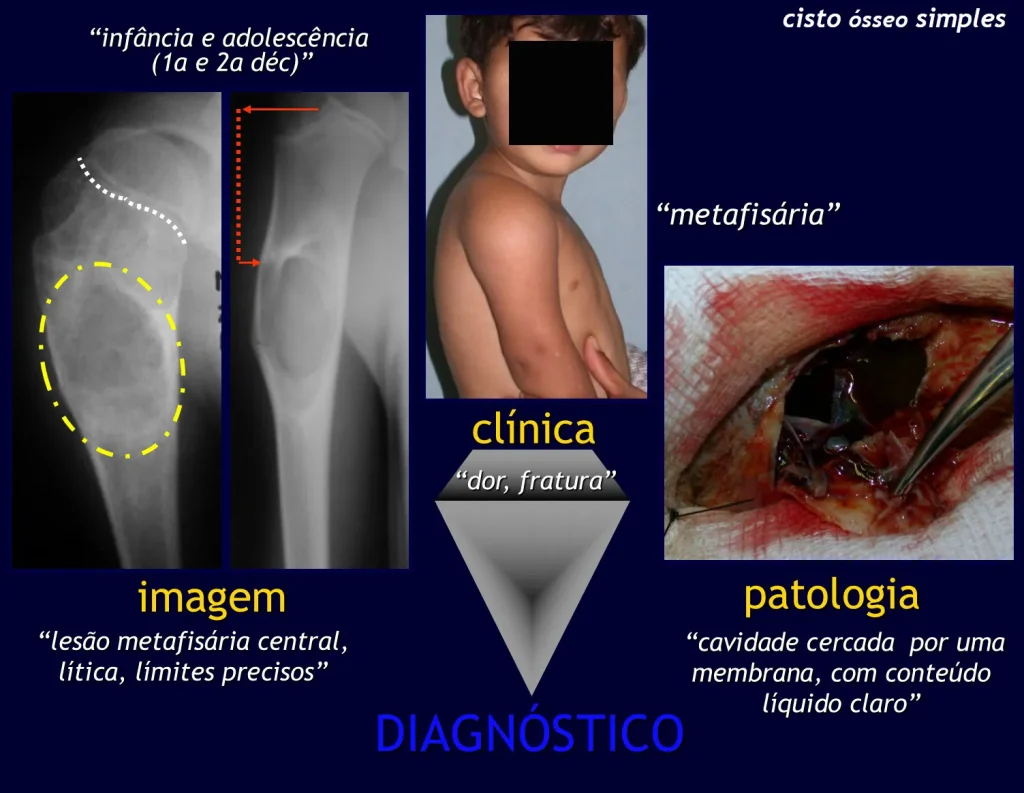
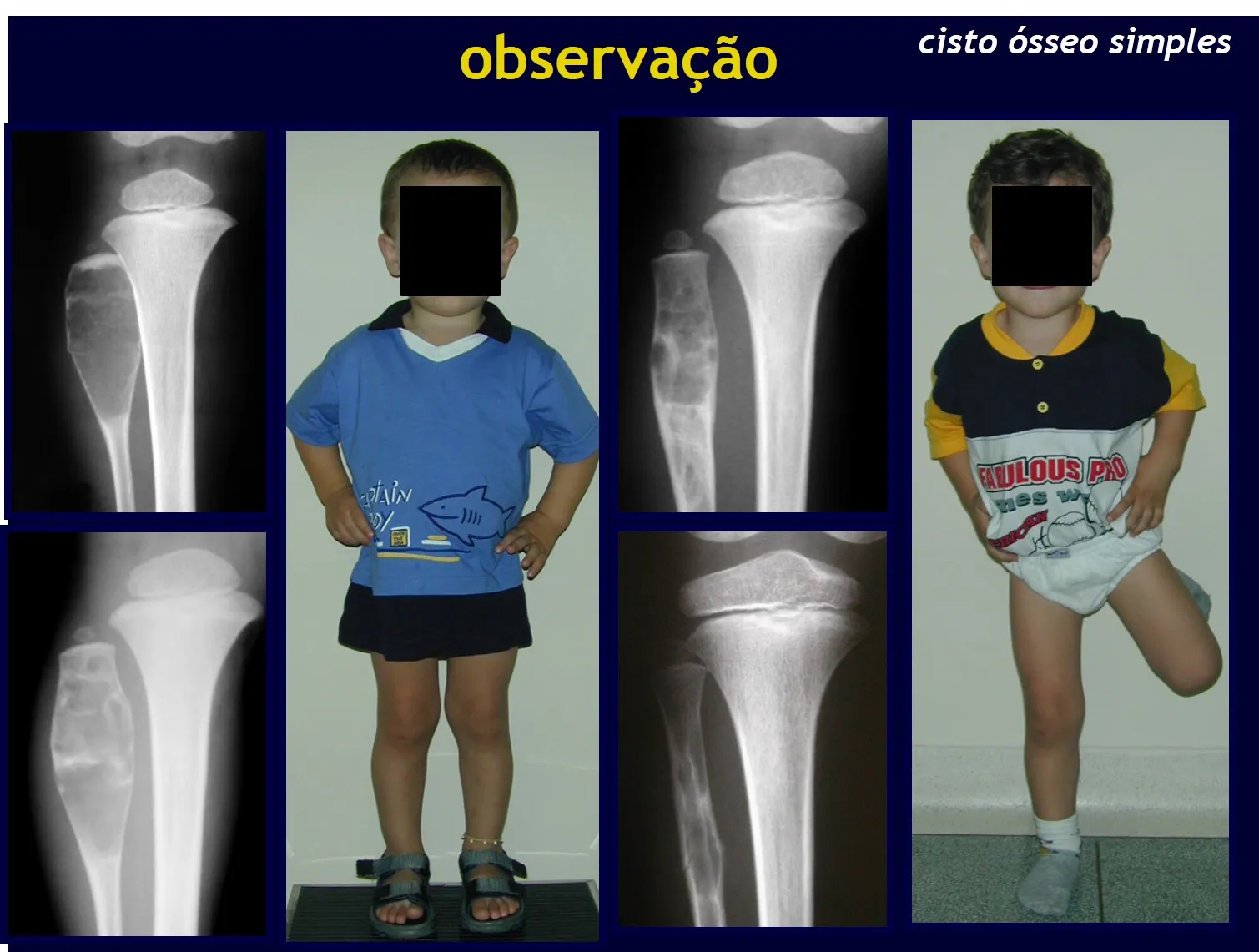
cisto ósseo simples.
cisto ósseo aneurismático.
cisto ósseo justacortical (gânglion intraósseo).
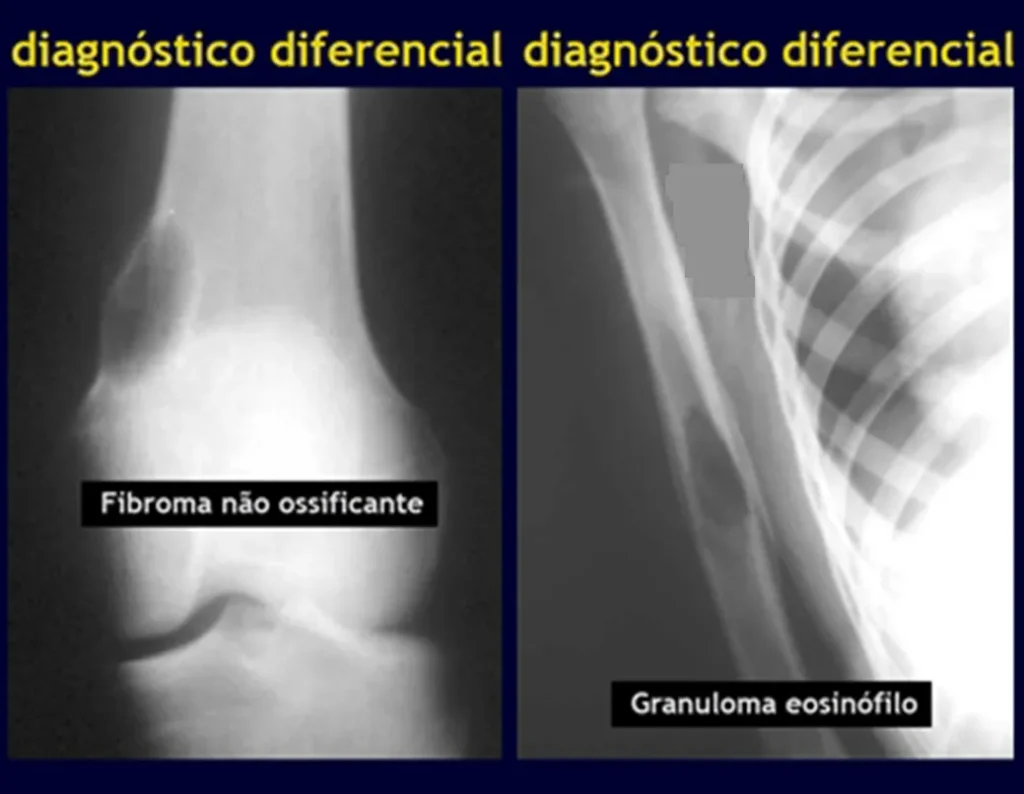
defeito fibroso metafisário (fibroma não ossificante).
granuloma eosinófilo.
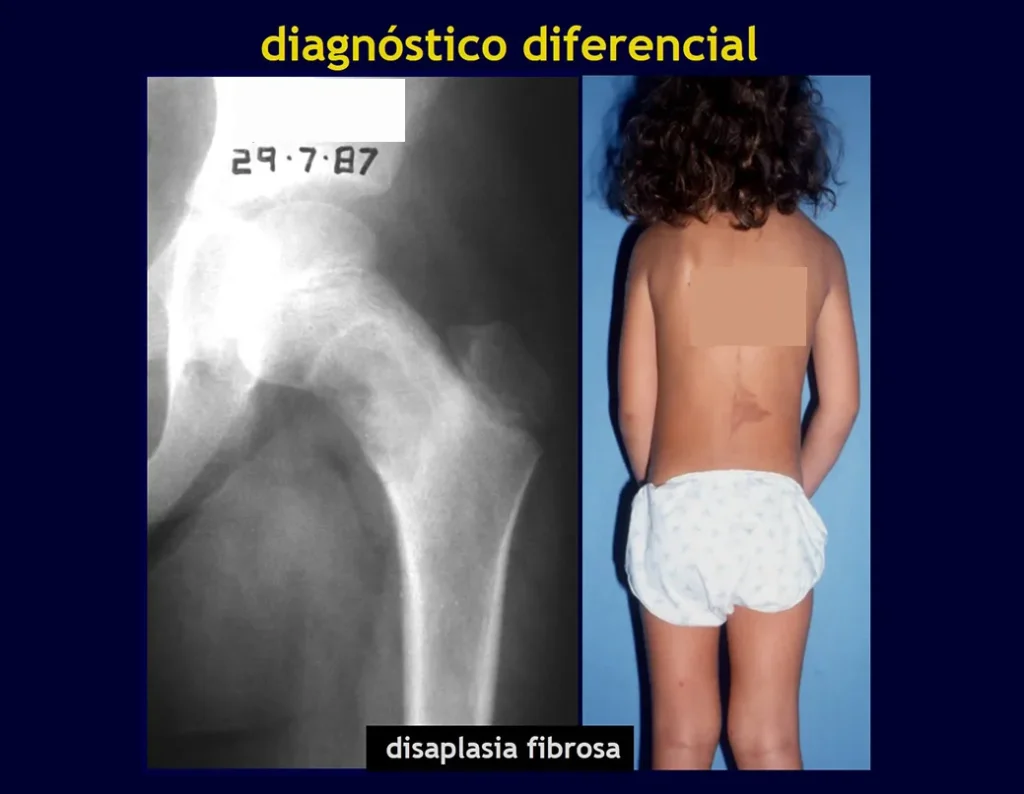
displasia fibrosa (osteofibrodisplasia).
miosite ossificante.
tumor marrom do hiperparatireoidismo.
cisto epidermóide intra-ósseo.
granuloma reparador de células gigantes.
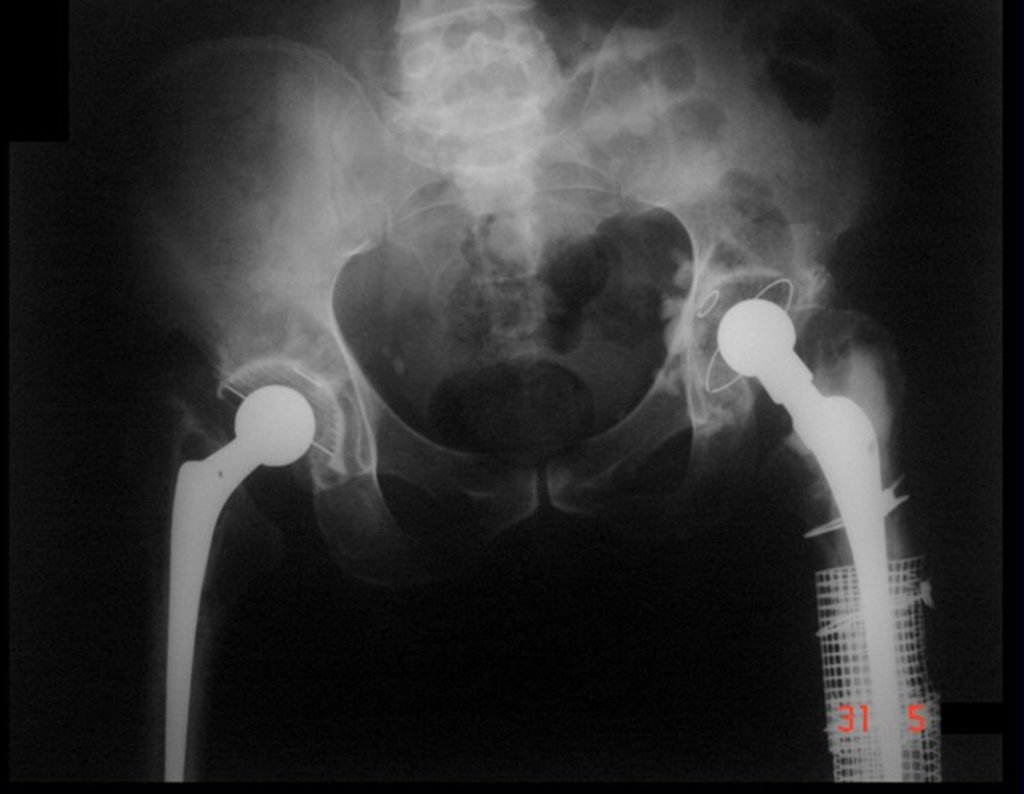
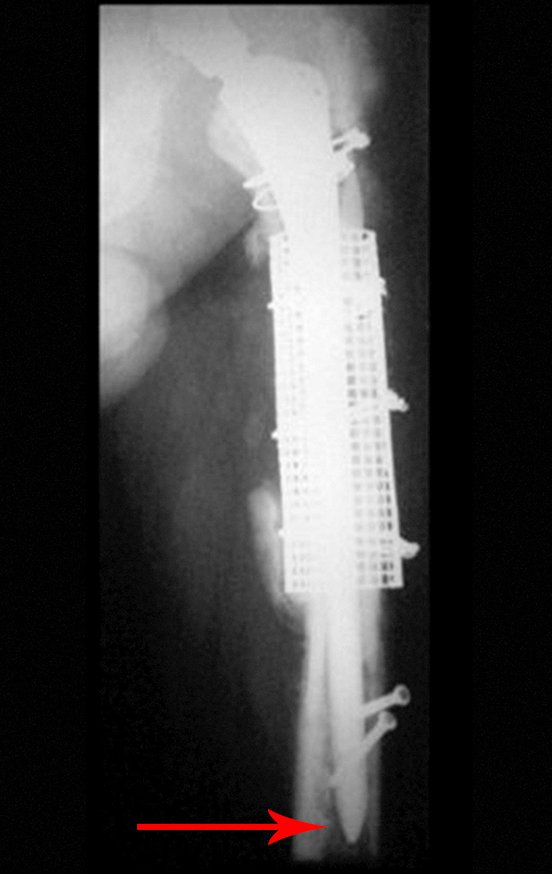
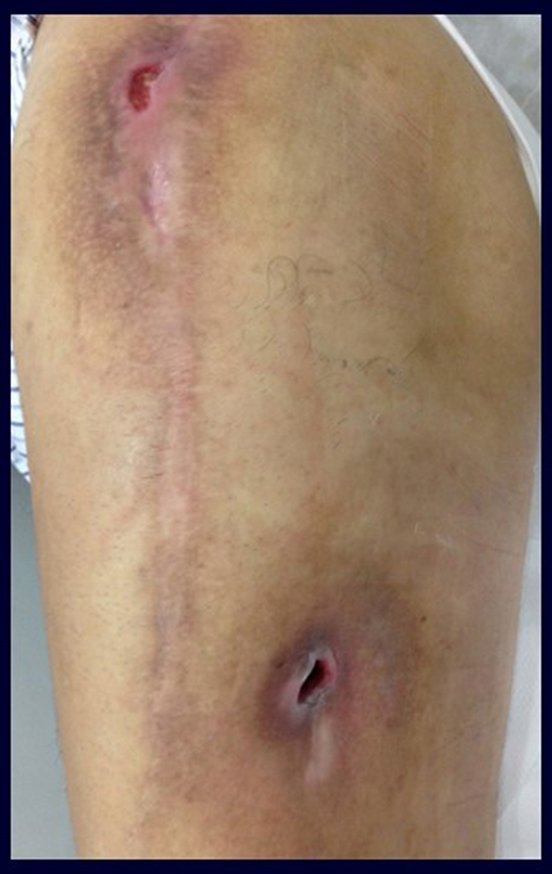
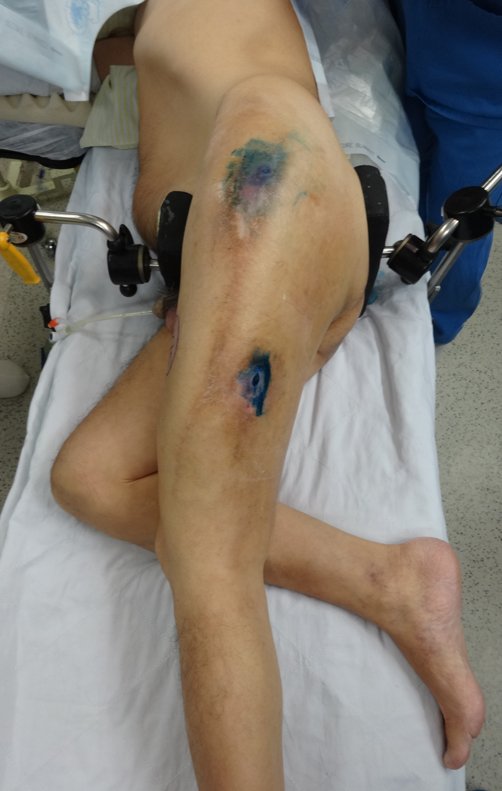
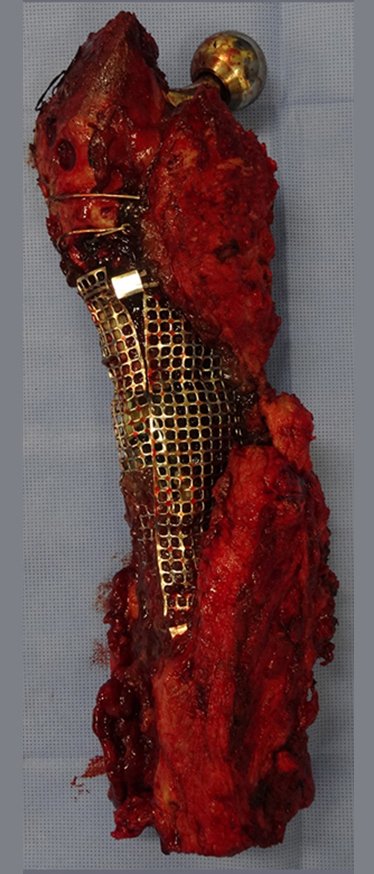
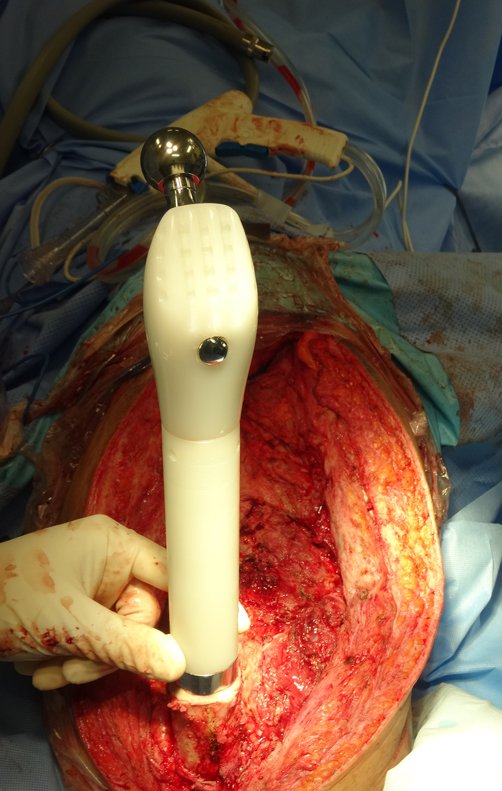
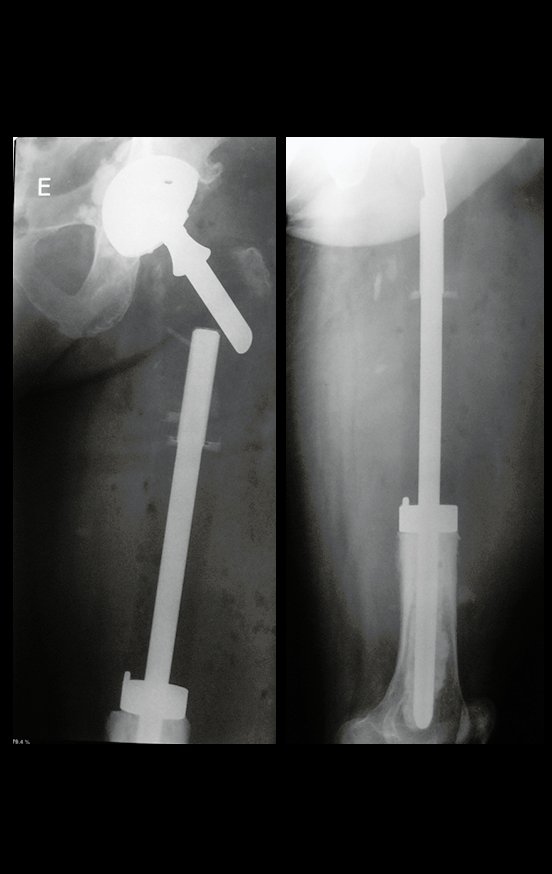
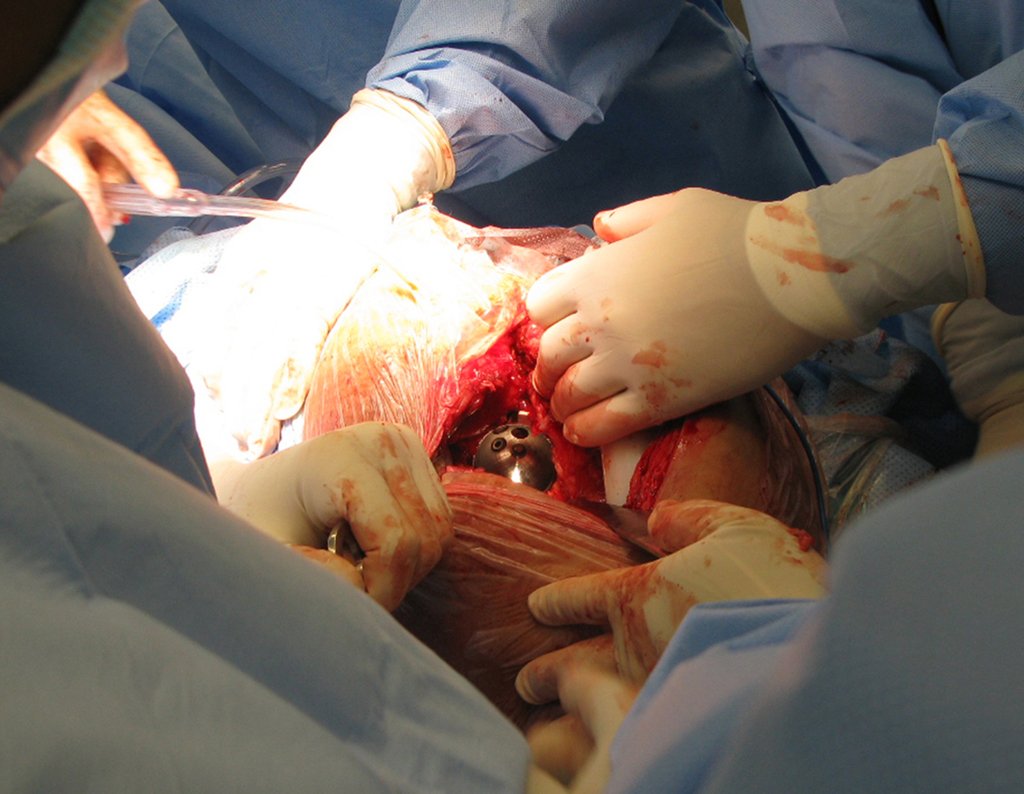
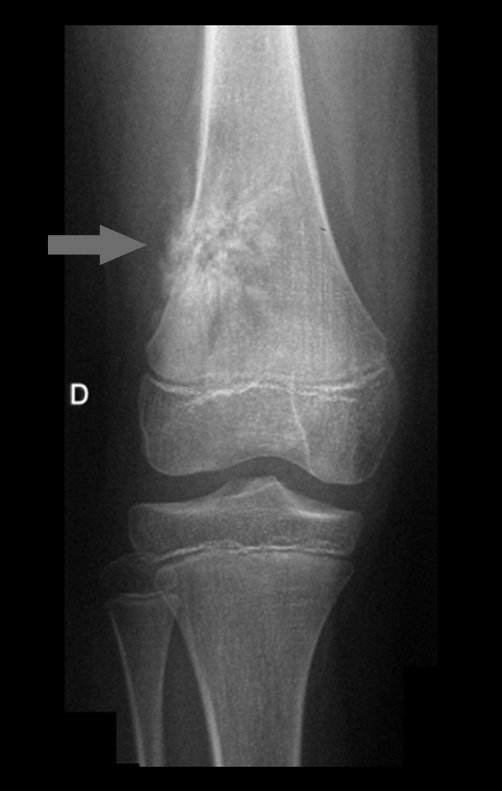
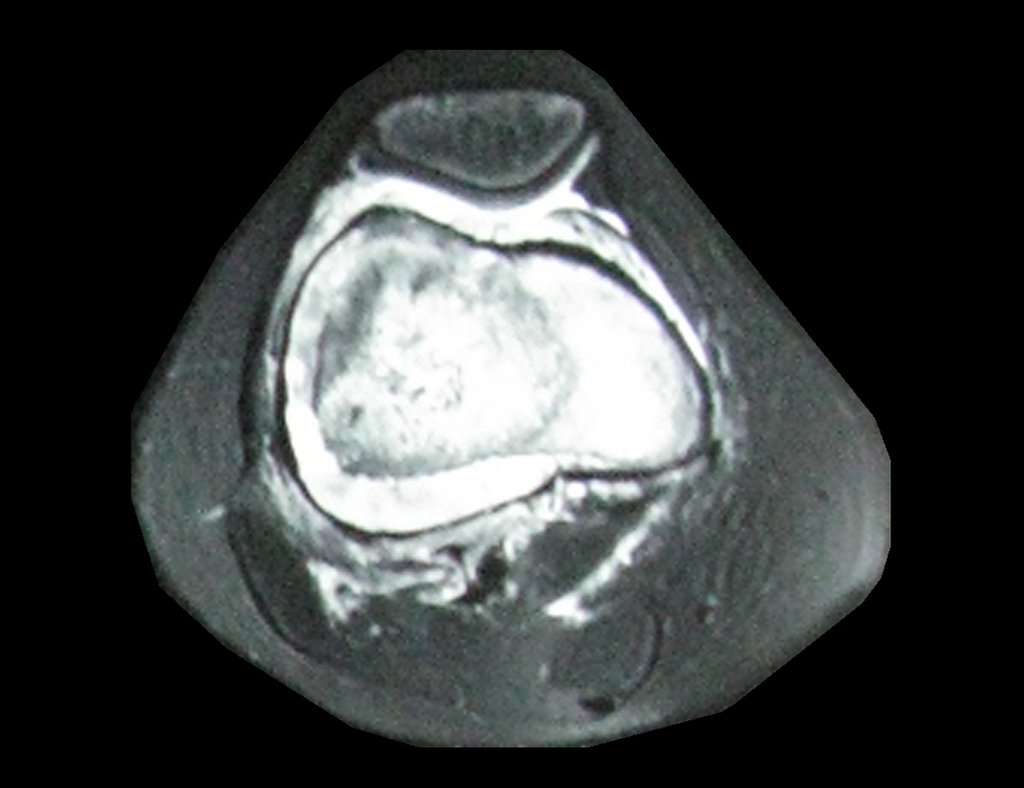
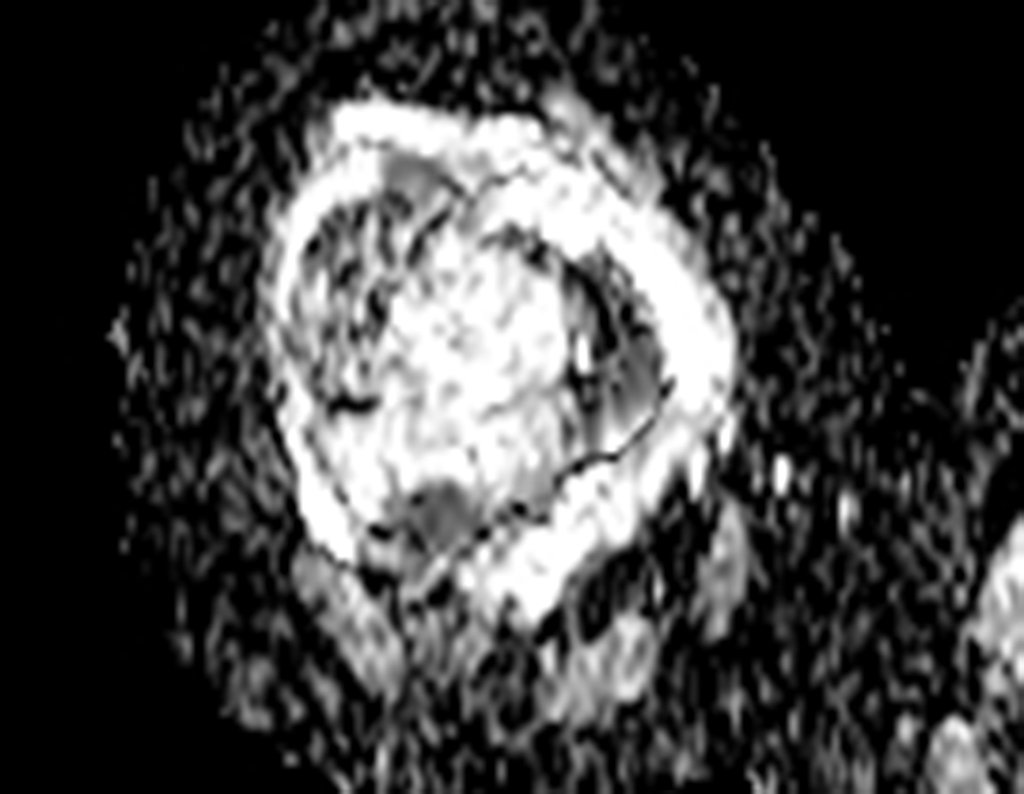
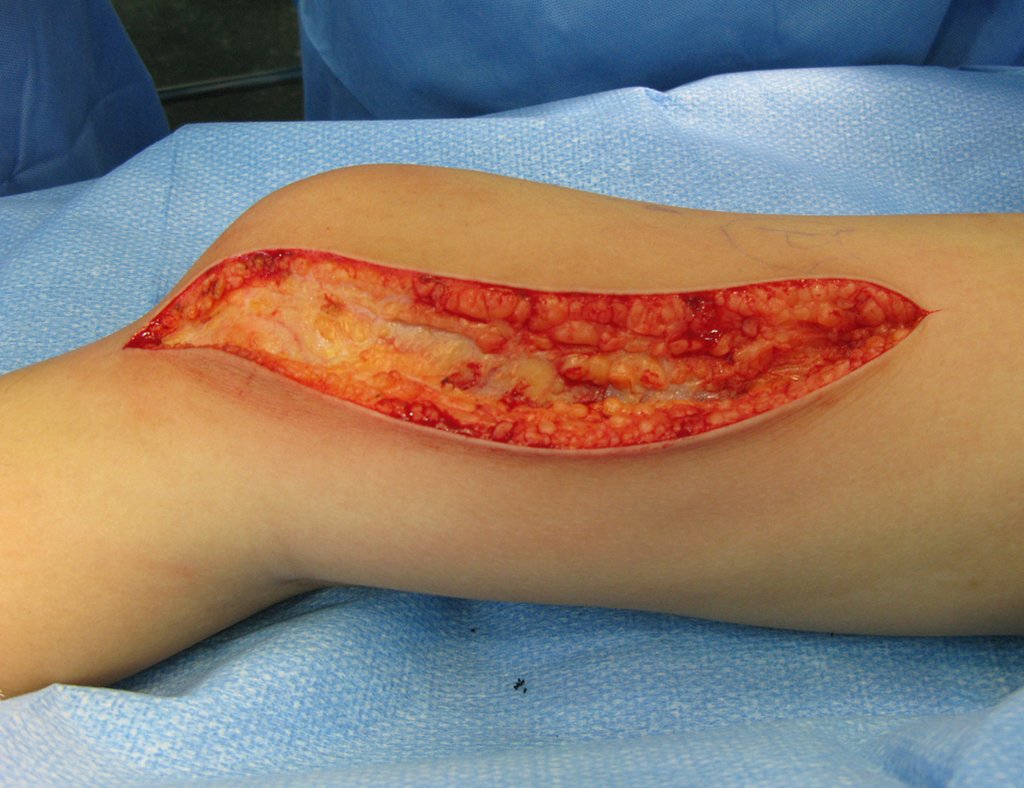
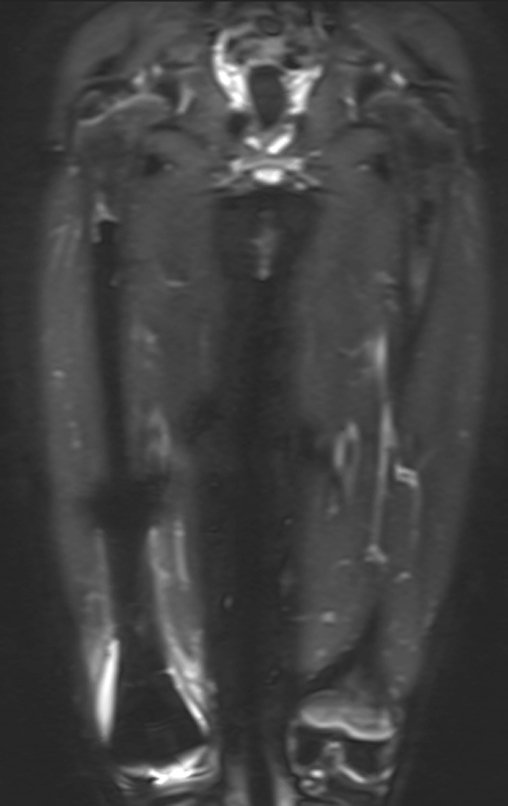
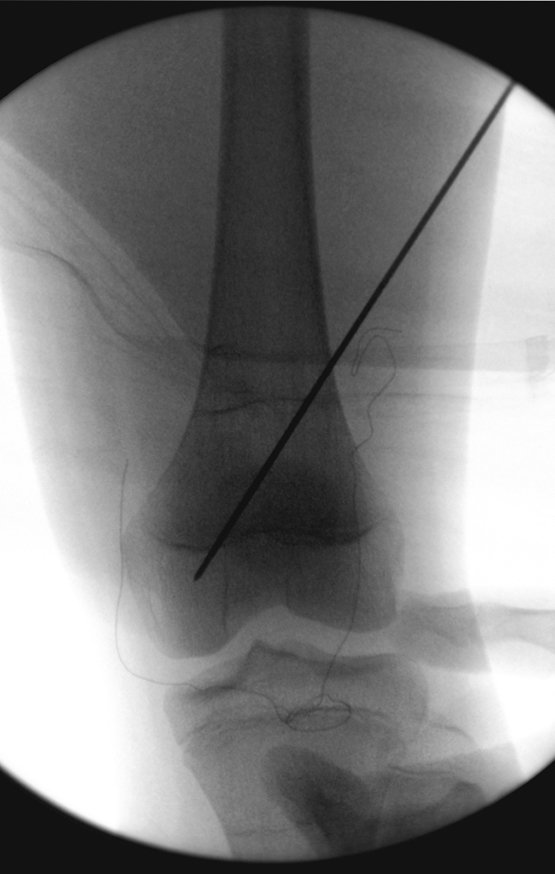
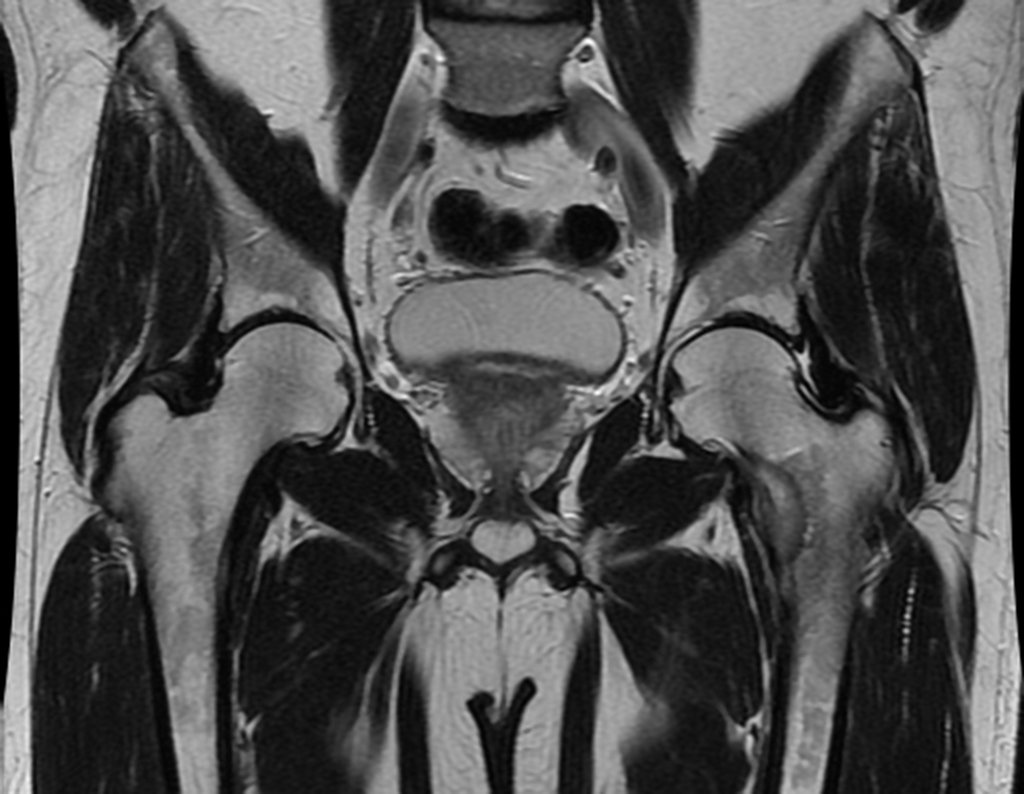
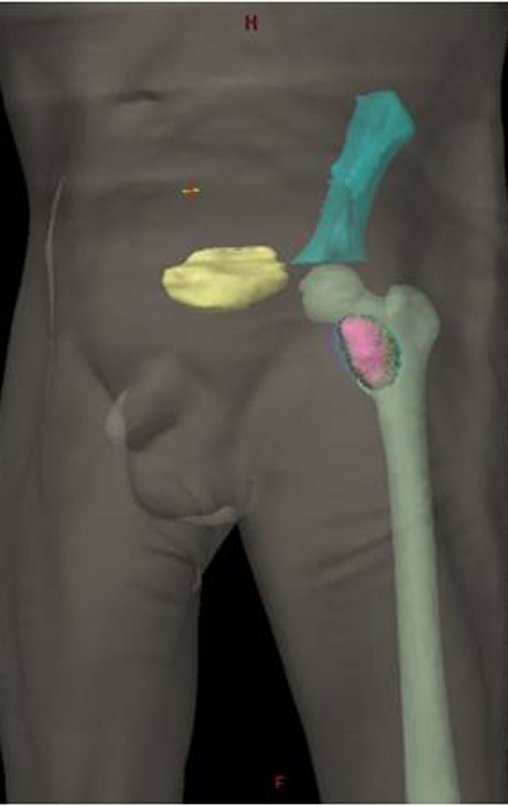
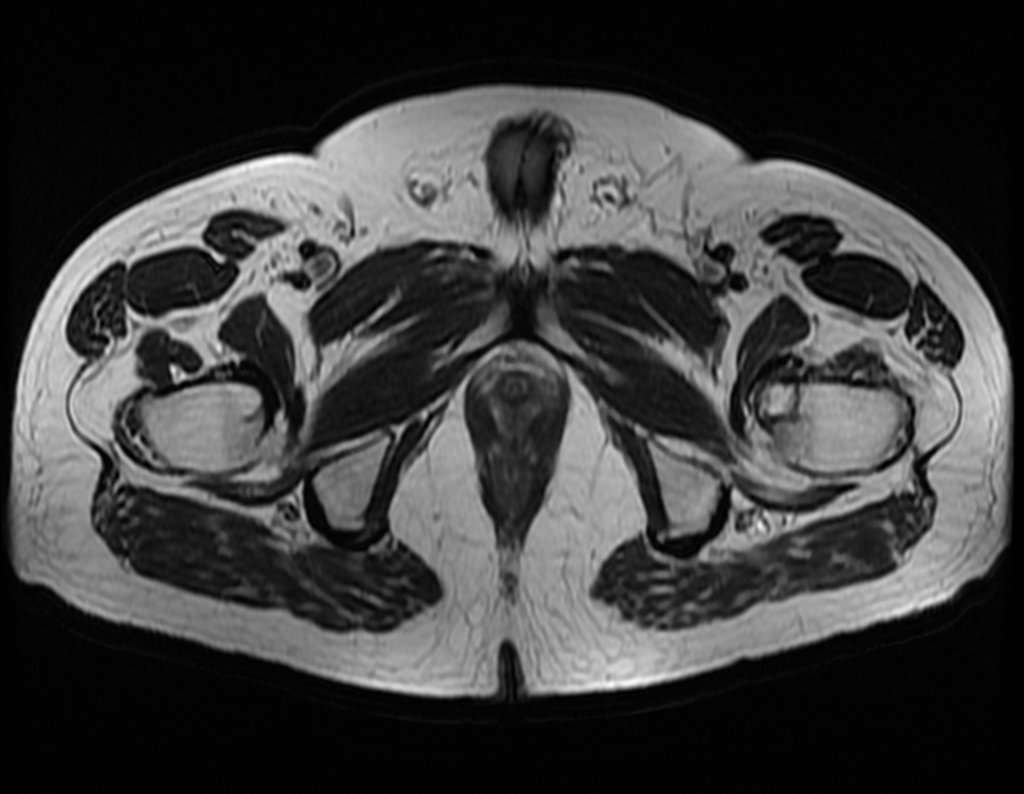
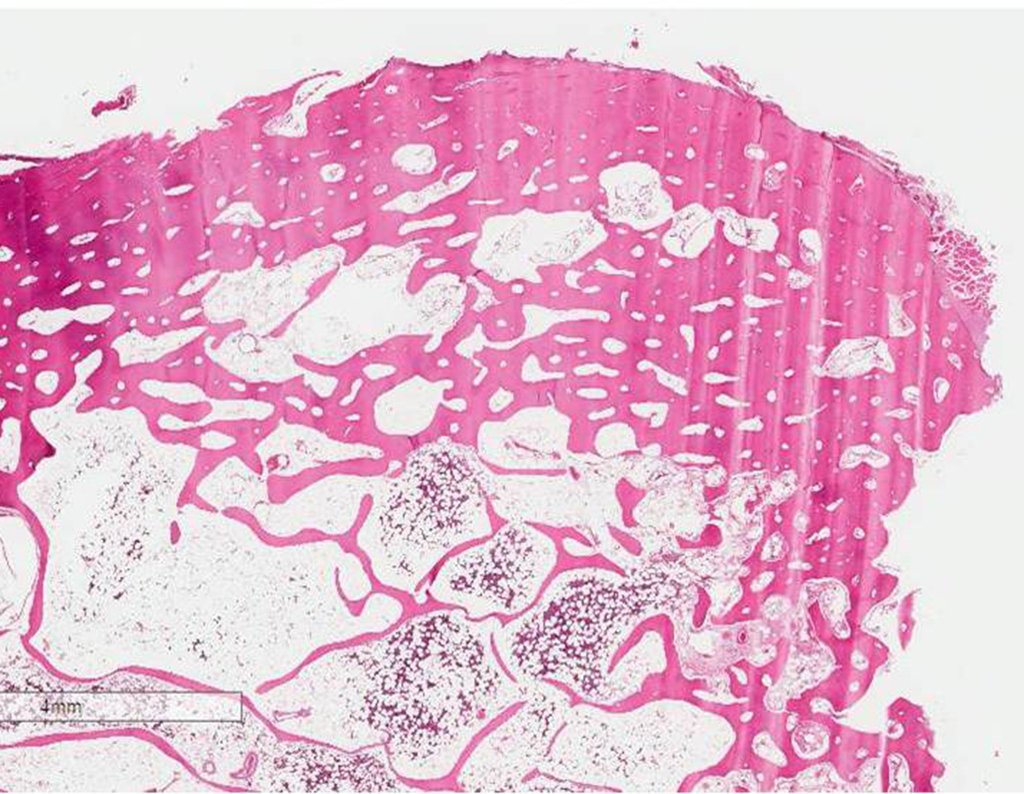
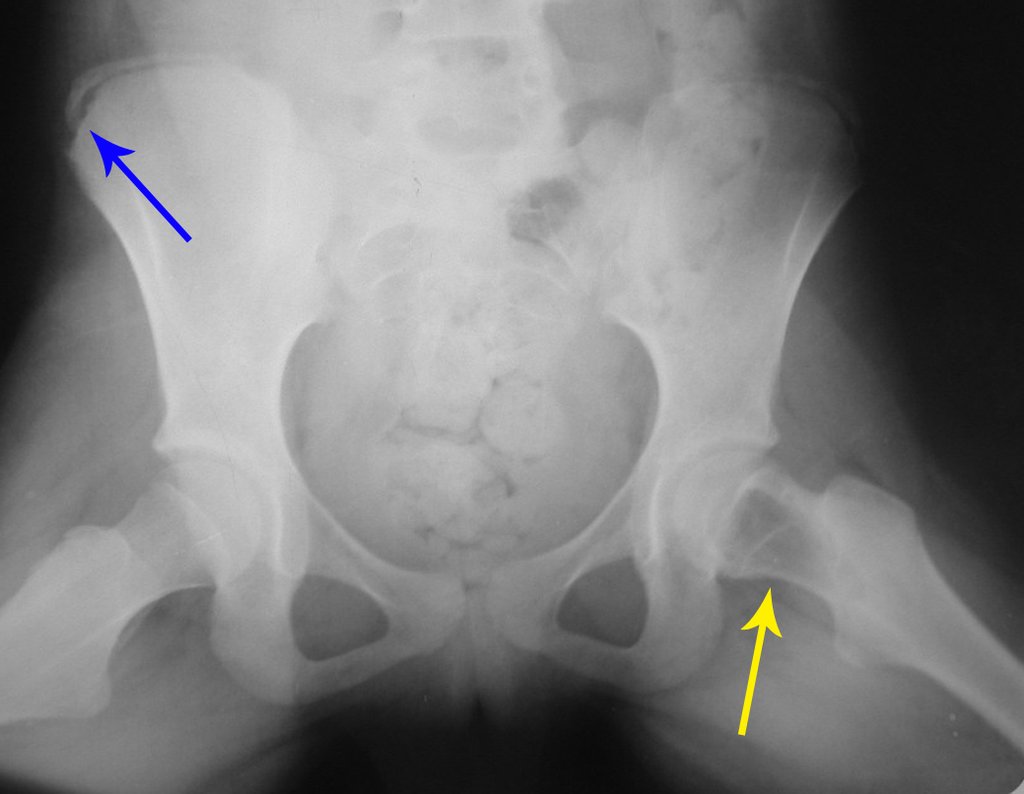
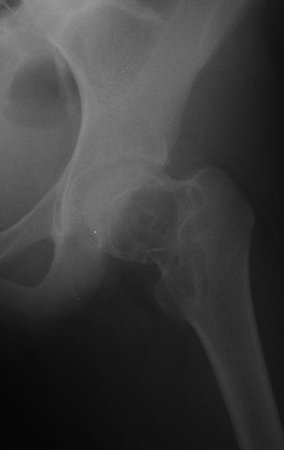
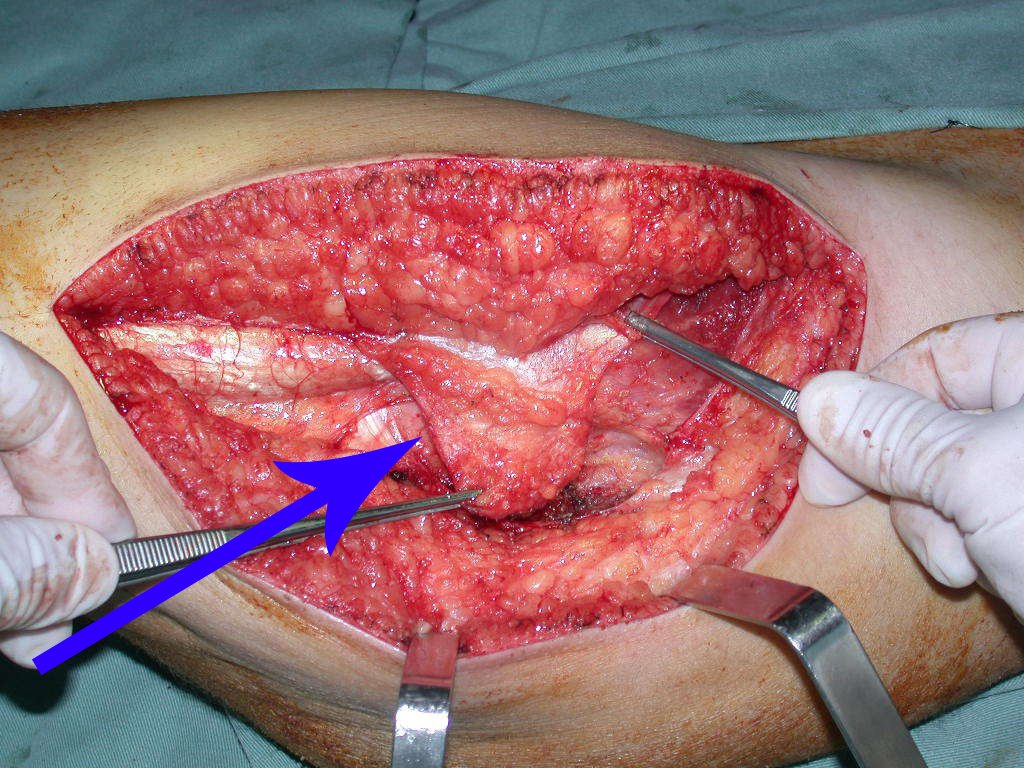
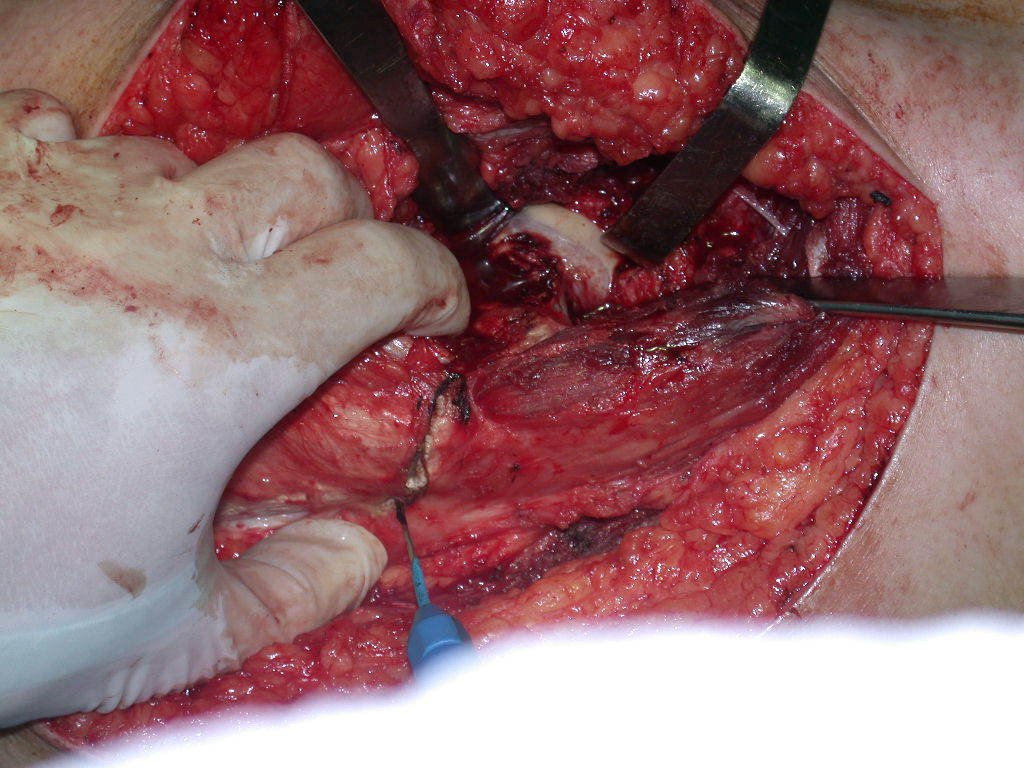
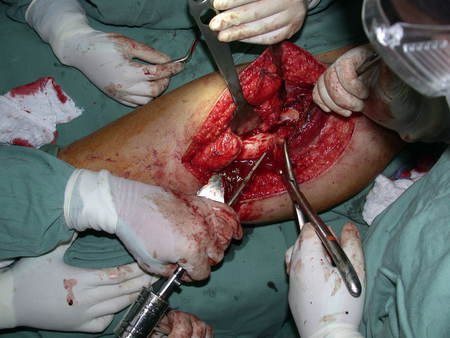
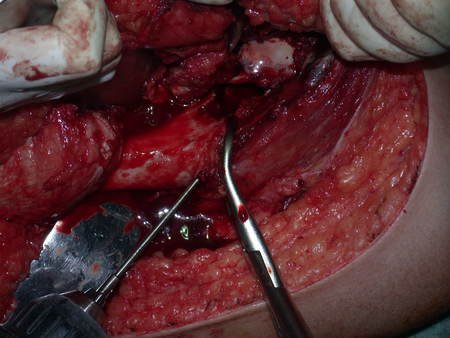
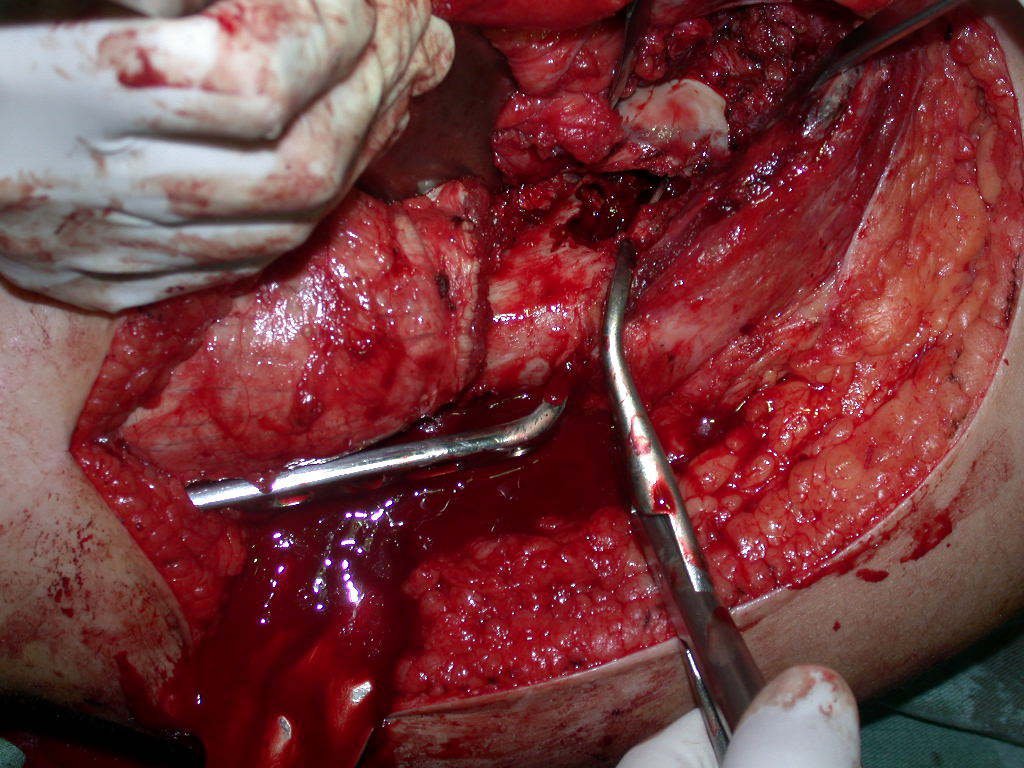
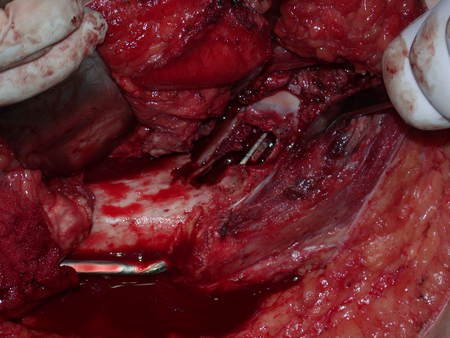
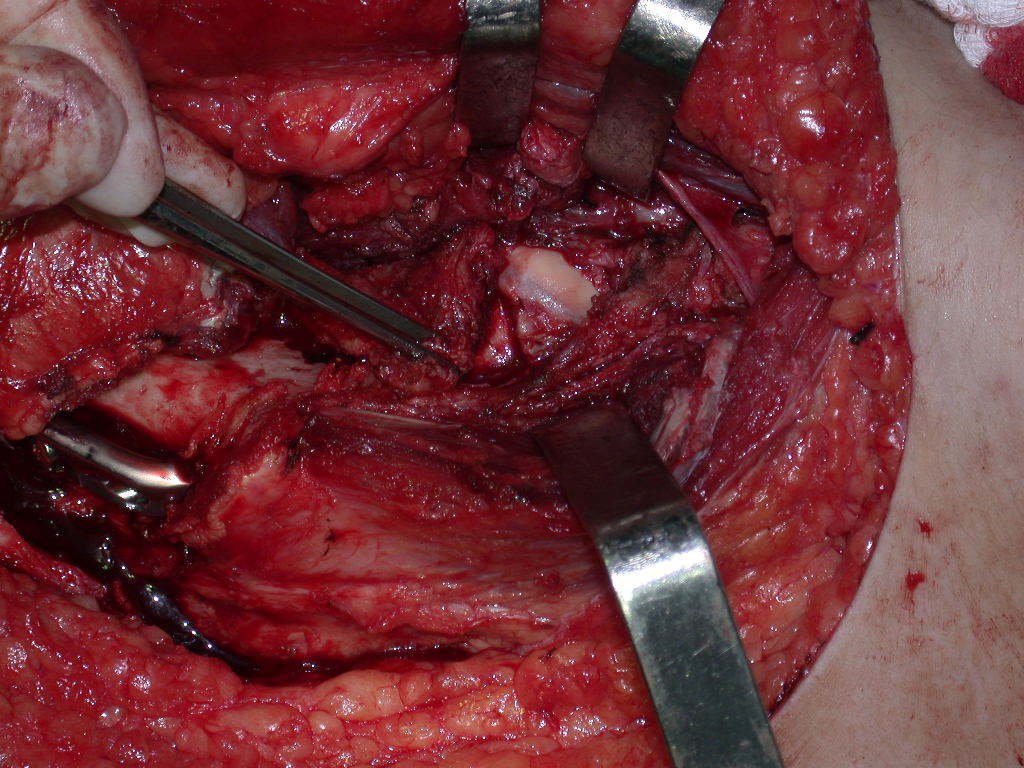
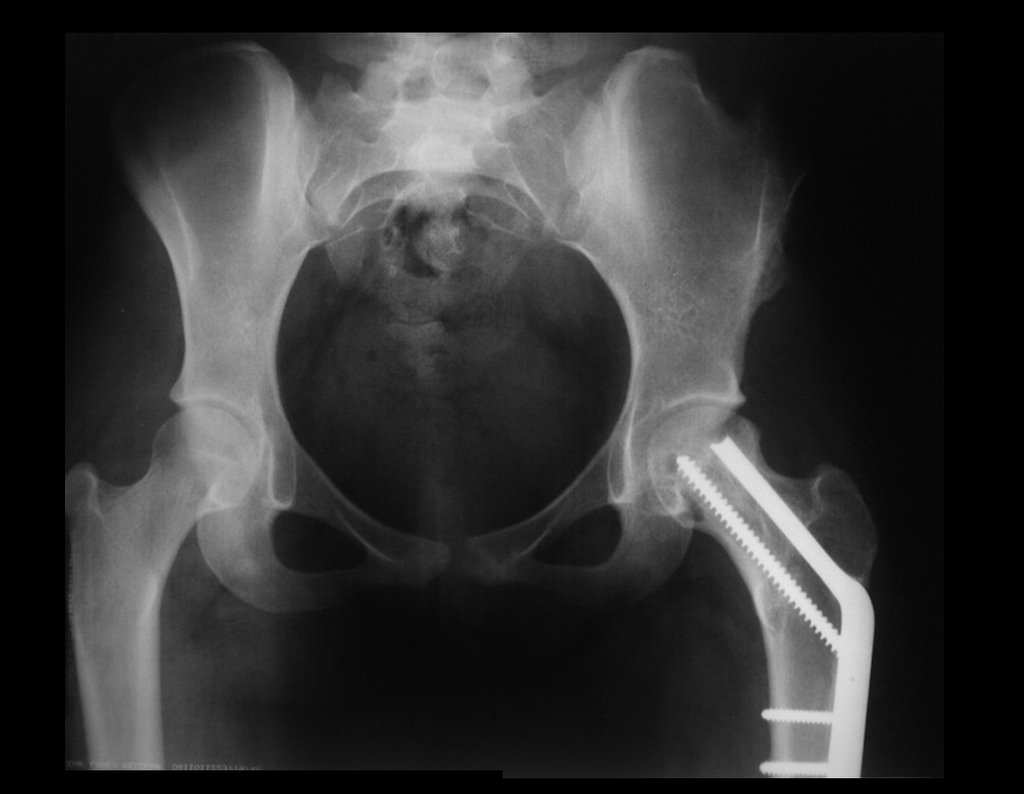
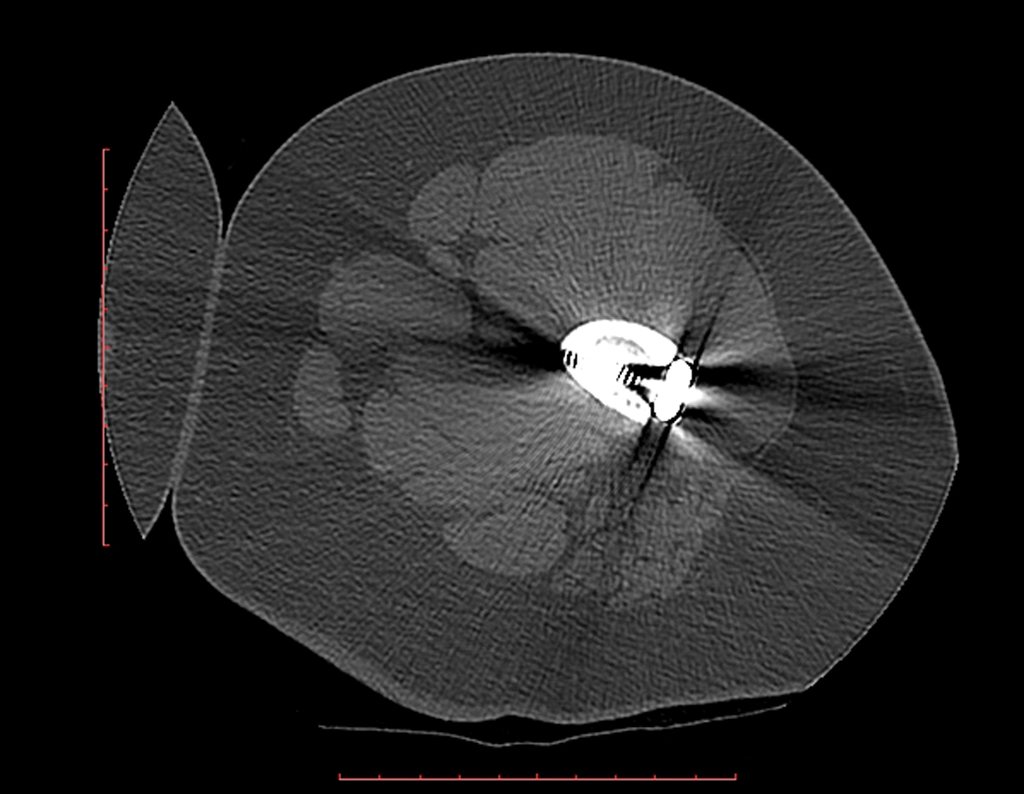
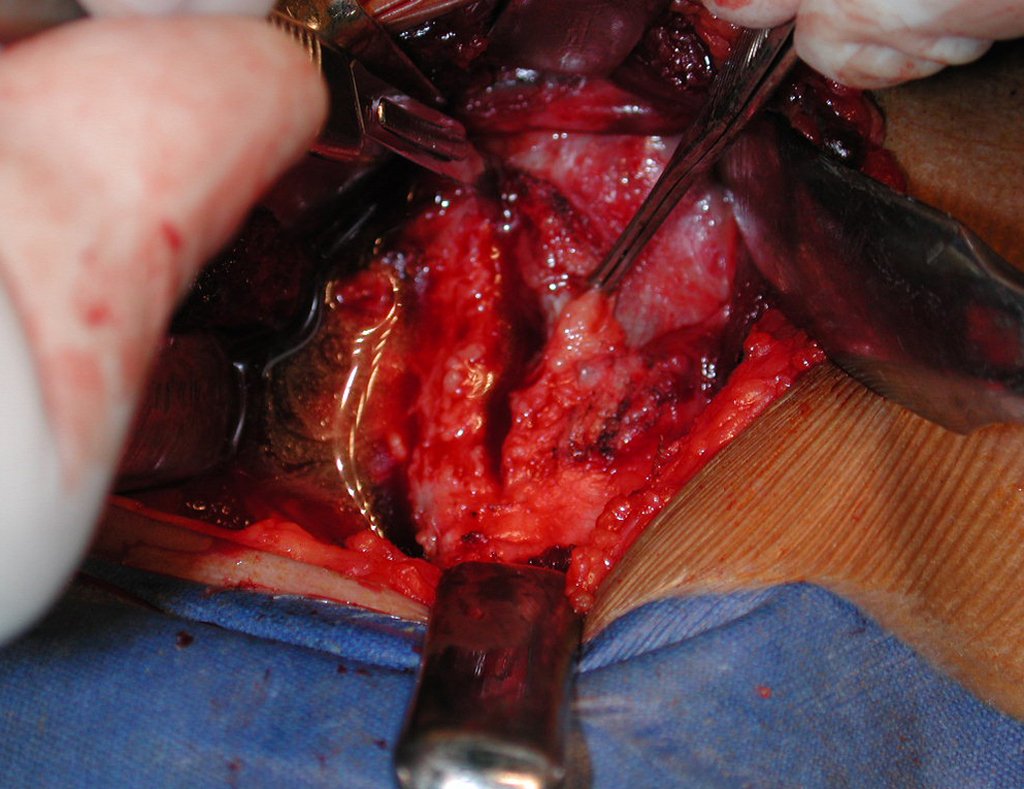
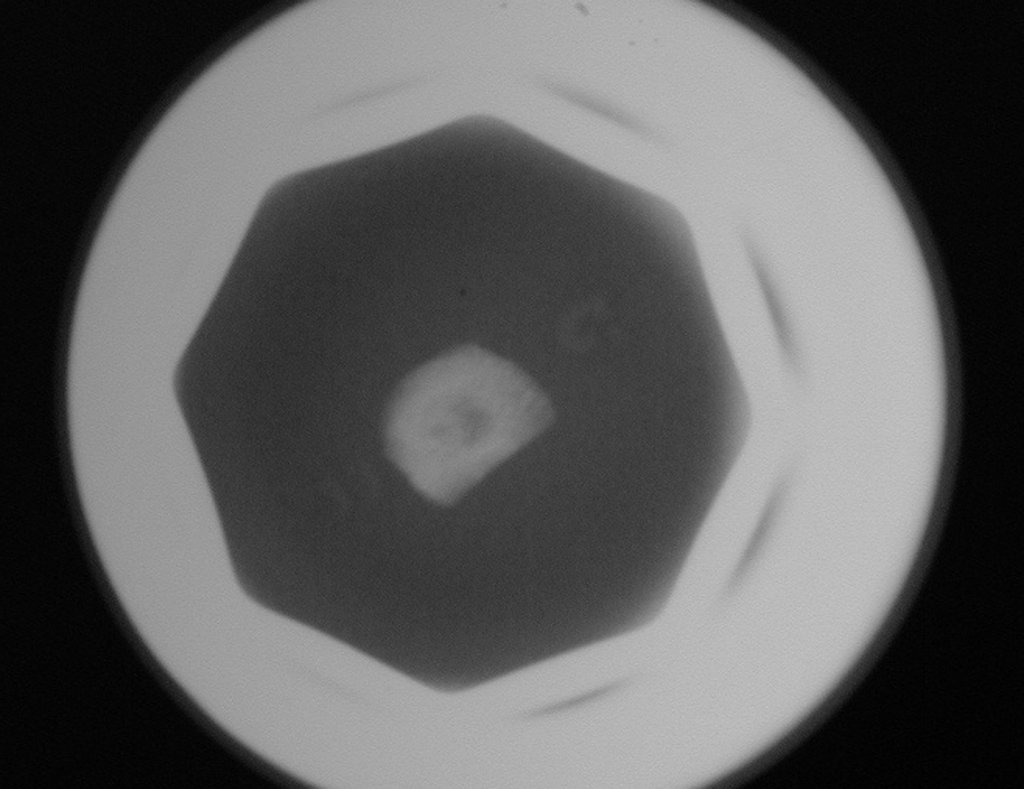
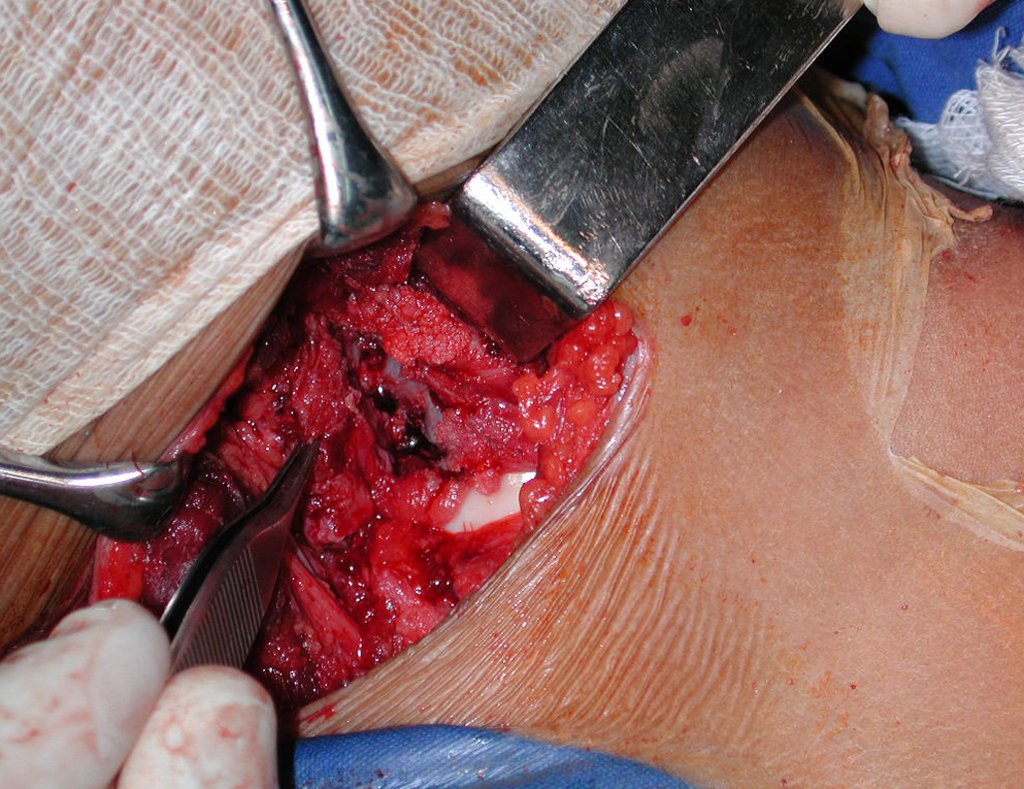
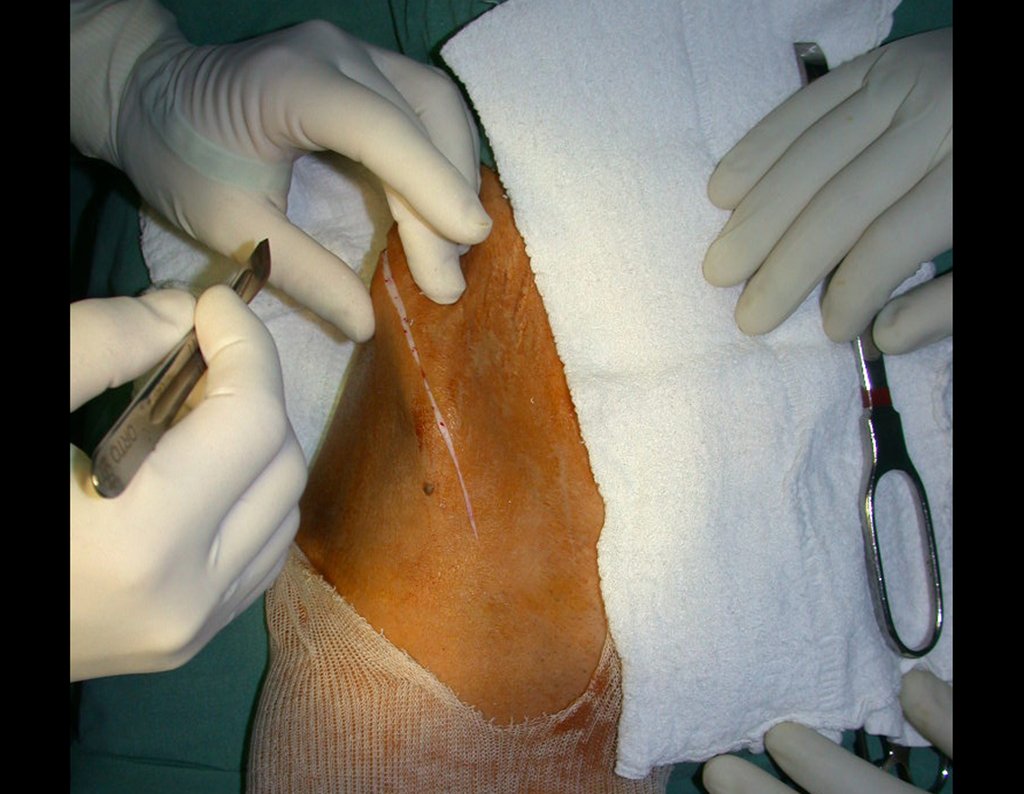
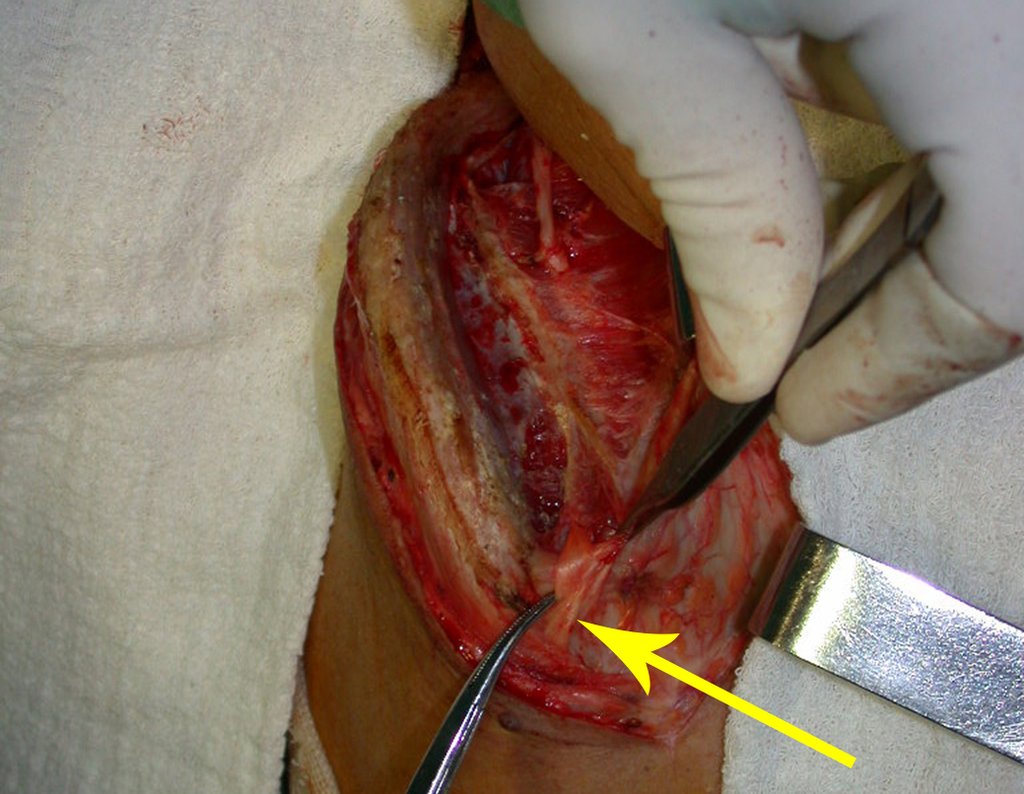
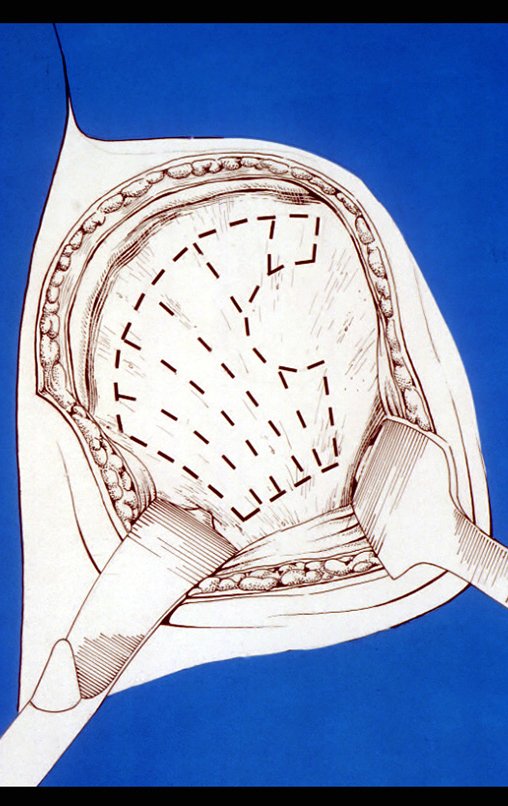
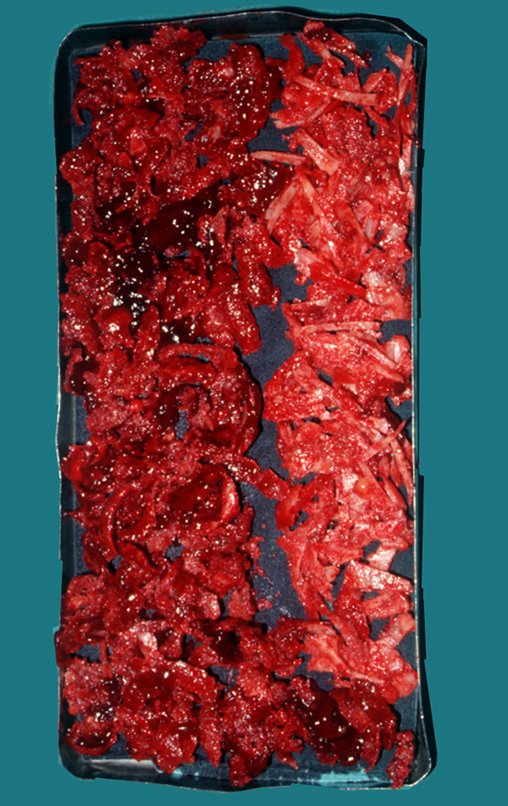
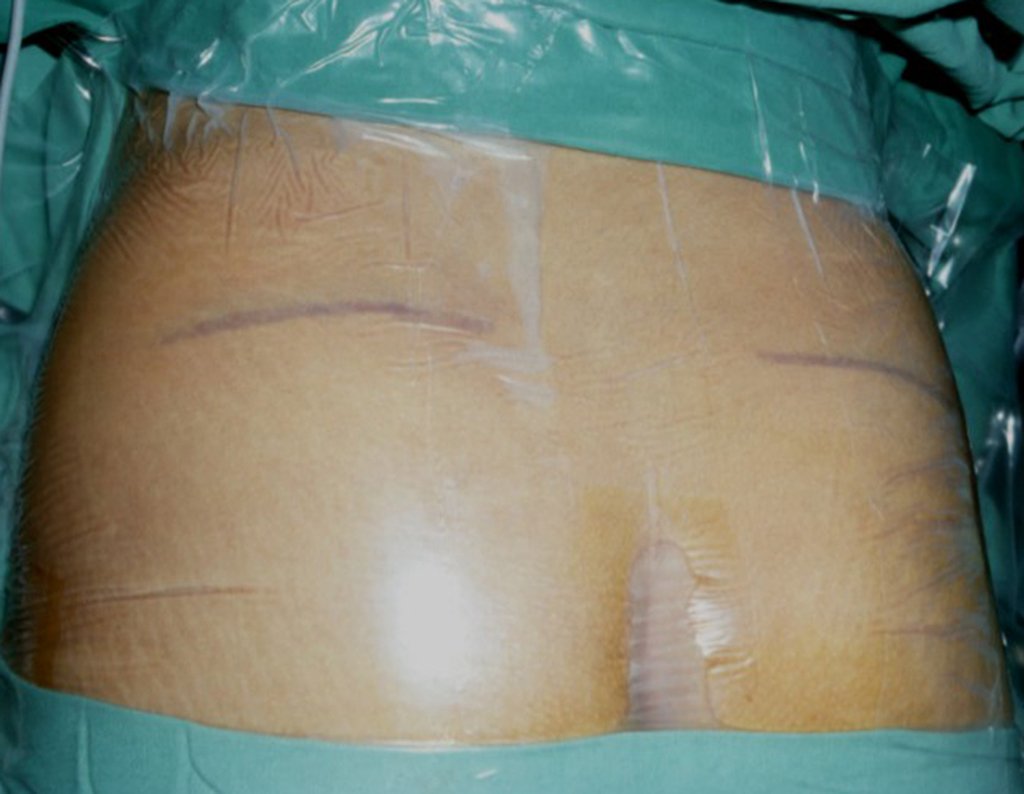
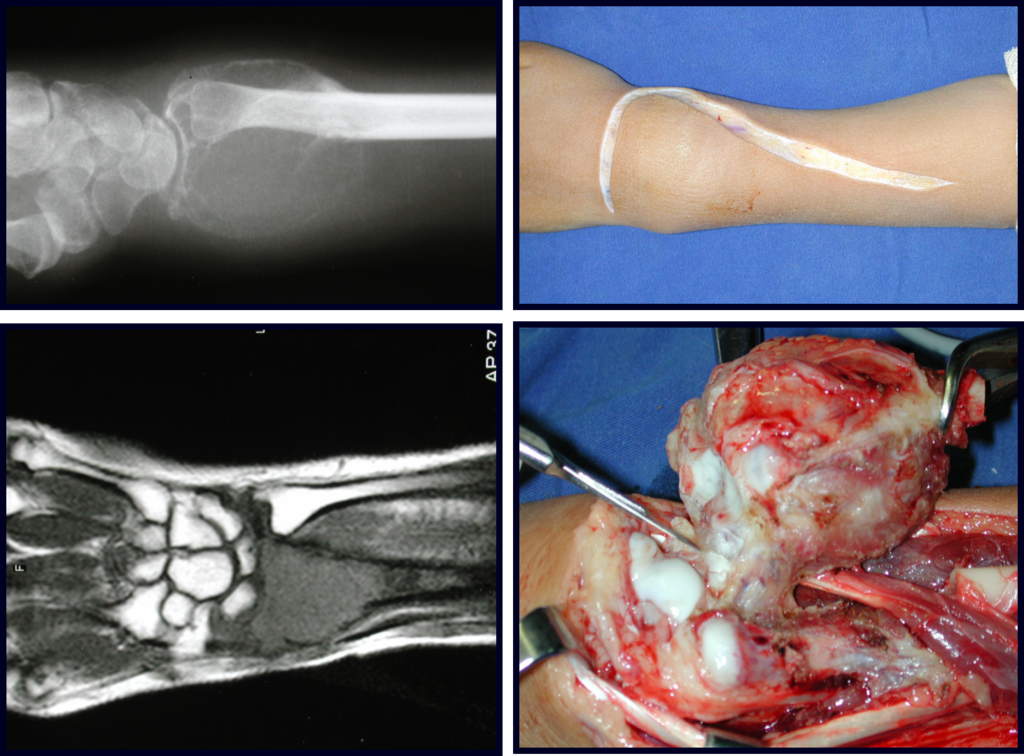
O cisto ósseo aneurismático, também chamado de cisto hemático multilocular, é lesão de rarefação óssea insuflativa preenchida por líquido serosanguinolento, entremeada por espaços variáveis em tamanho e separados por septos de tecido conectivo contendo trabéculas de osso ou tecido osteóide e células gigantes ostoclásticas (fig 1).
A origem e etiologia deste processo ainda são desconhecidas, apesar de já ter sido descrita por Jaffe e Lichtenstein desde 1942. Estudos citogenéticos sugerem haver correlação entre esta lesão e fenômenos de translocação do cromossoma 17.
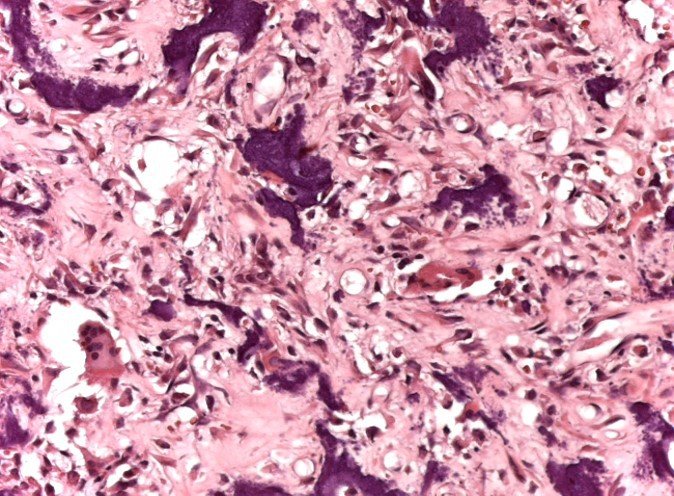
A presença de células gigantes do tipo osteoclastos” sugere que ocorreu um processo de reabsorção óssea localizada, acompanhado de acúmulo de sangue e septado ora por tecido conjuntivo ora por tecido osteóide com trabéculas ósseas.
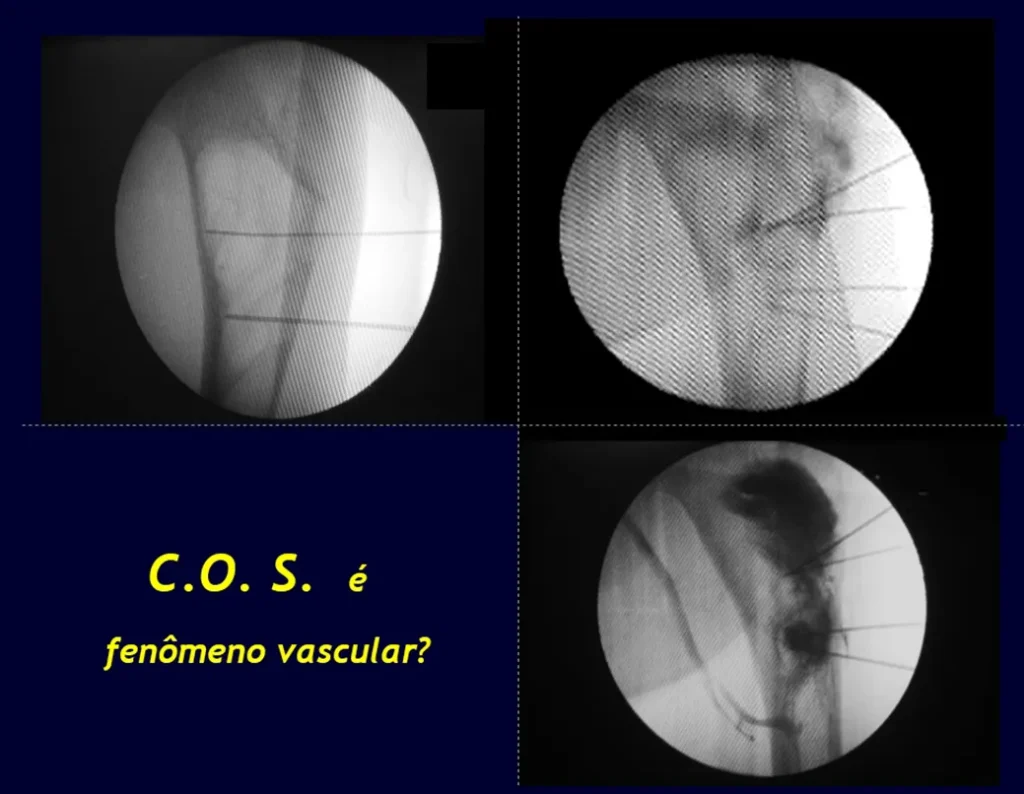
Estas cavidades cheias de sangue não apresentam irrigação sanguínea que possa ser evidenciada por arteriografia ou infusão de contraste intracístico e consequentemente não têm caráter pulsatil. Estas lojas não se encontram vazias portanto não são cistos e nem tampouco representam qualquer forma de aneurisma. O termo “cisto ósseo aneurismático” não é adequado para esta afecção.
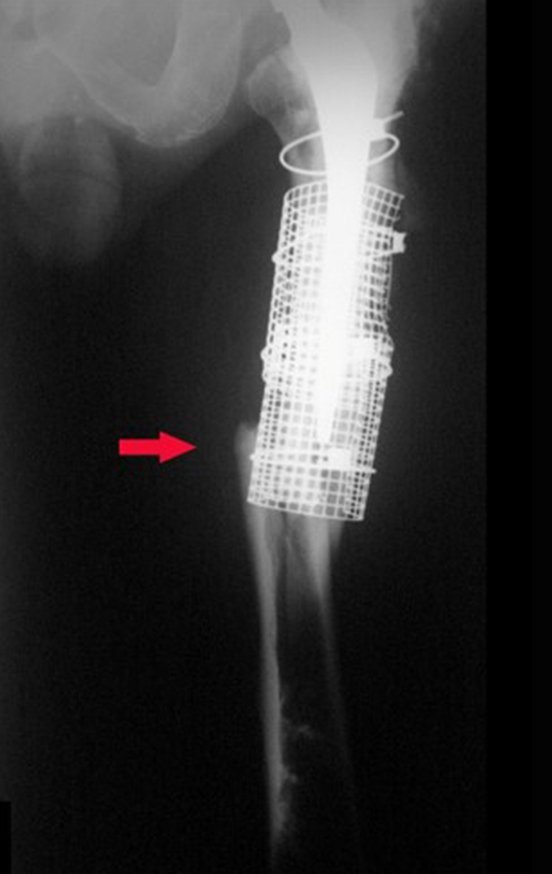
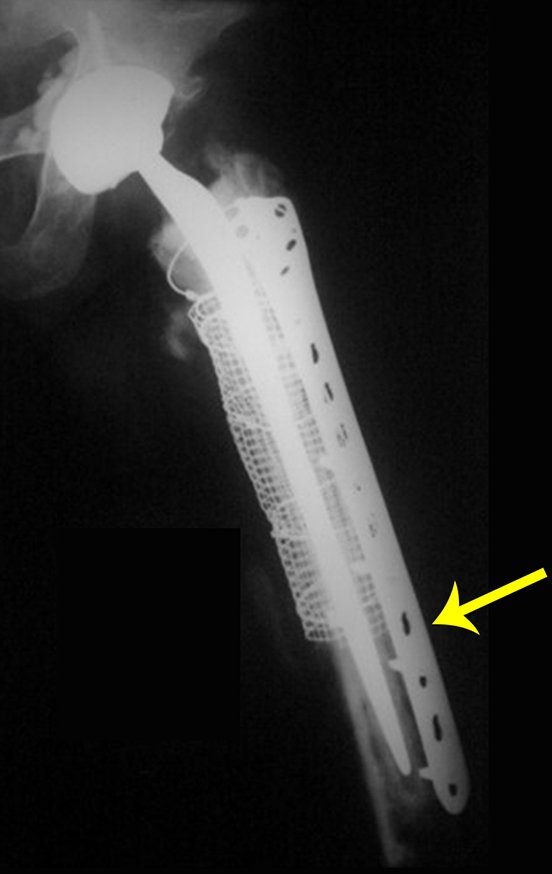
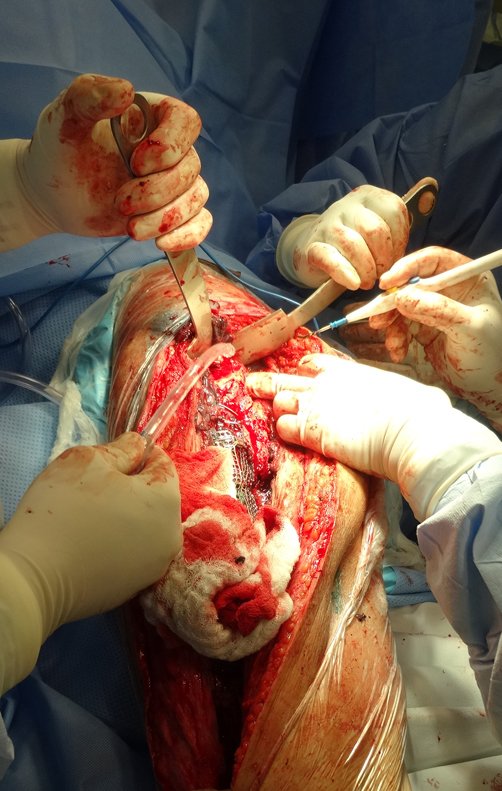
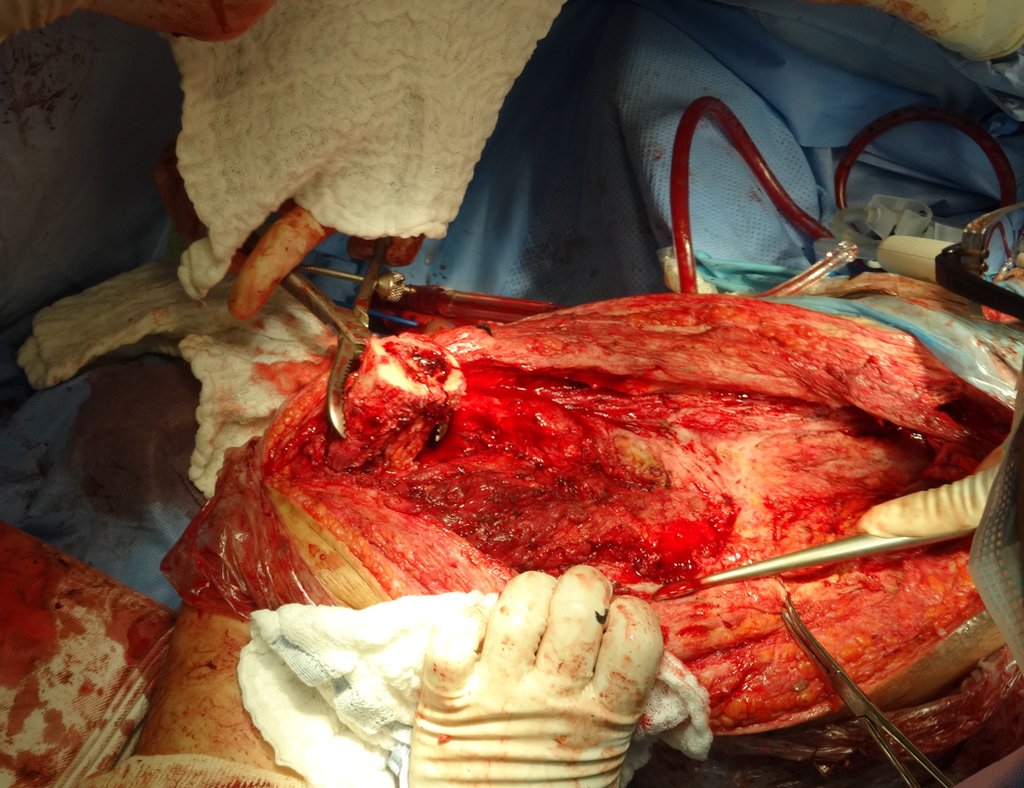
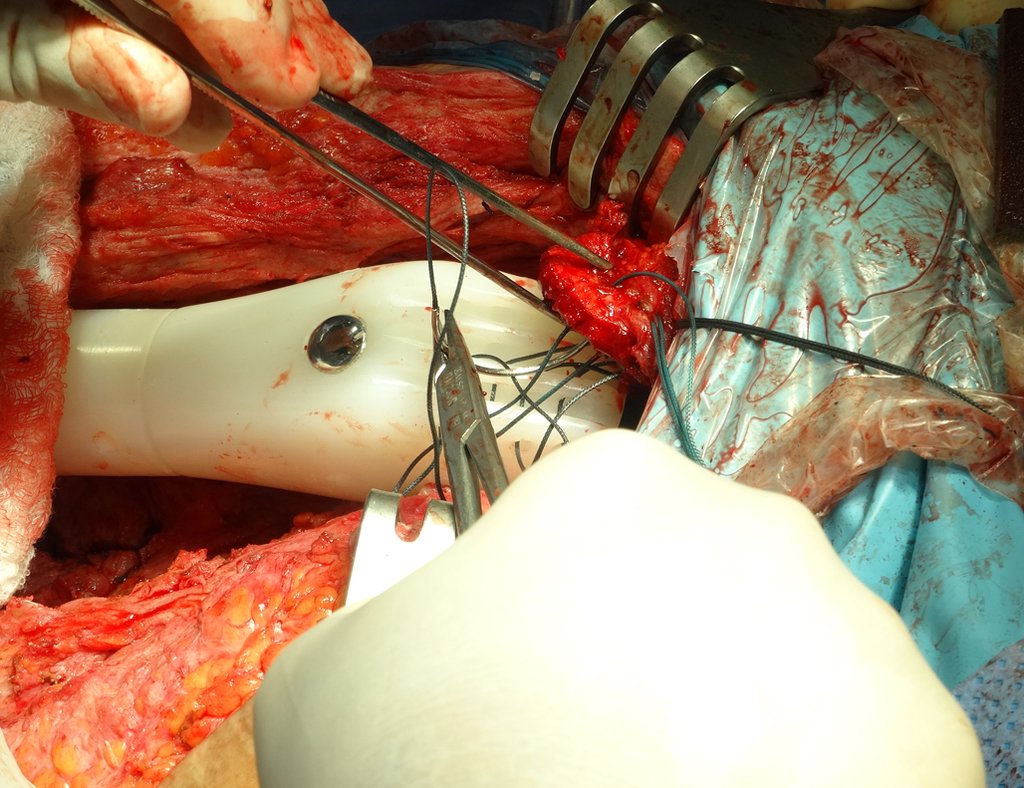
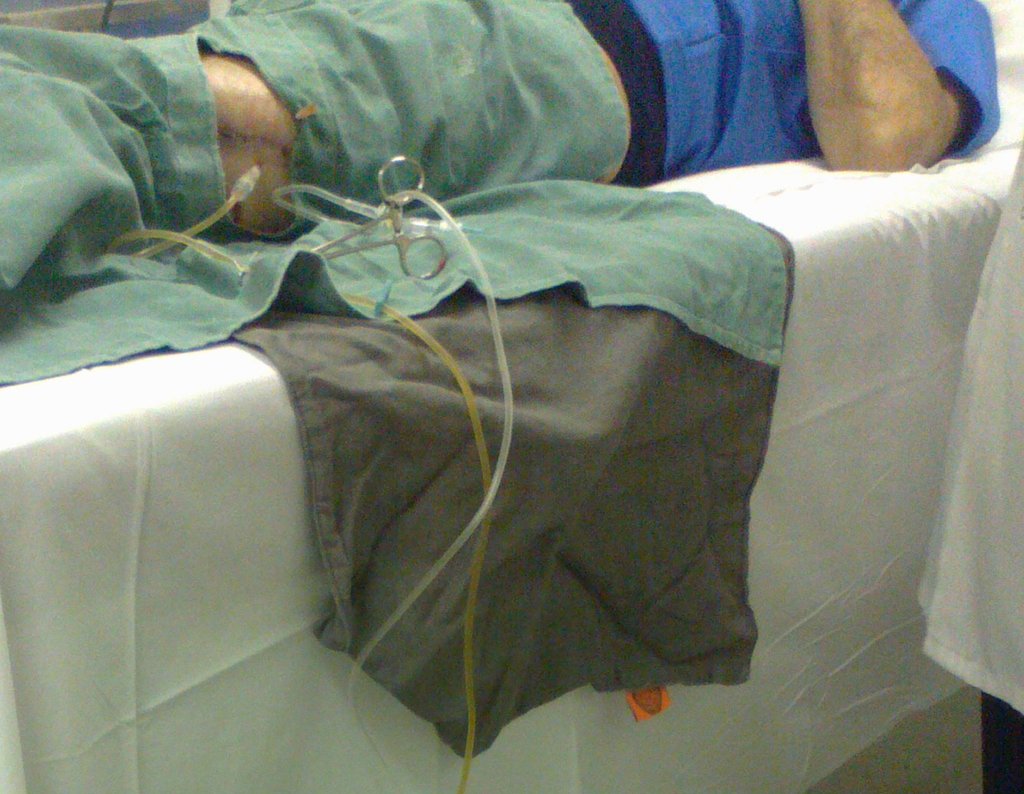
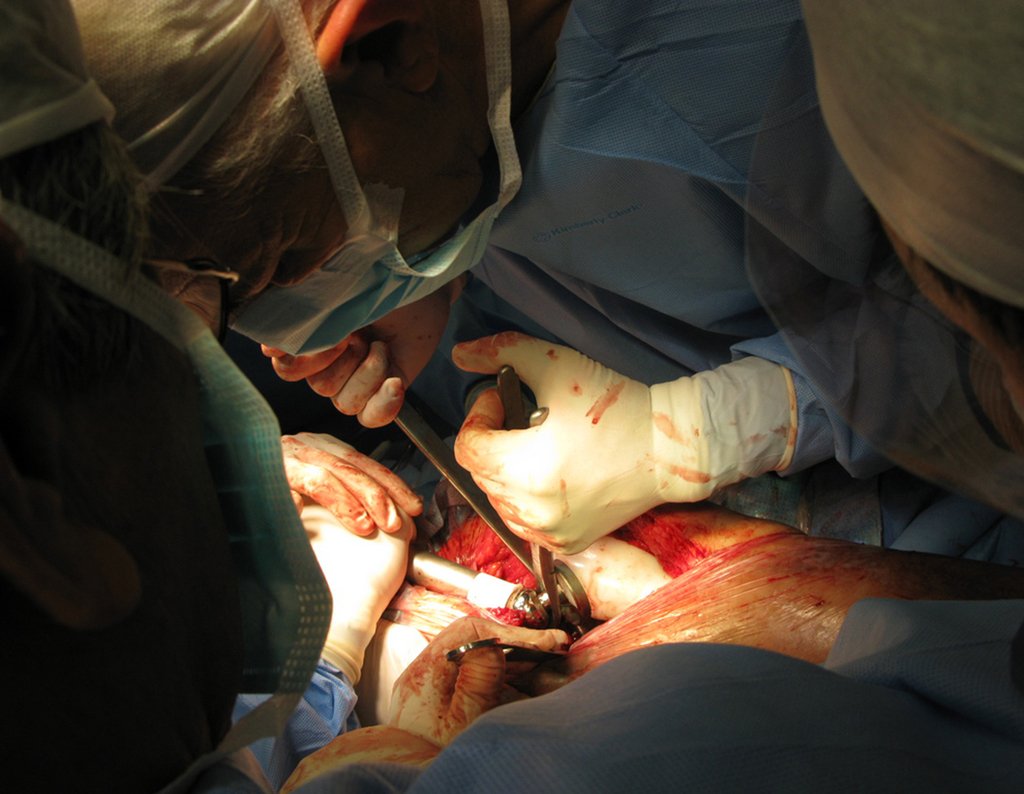
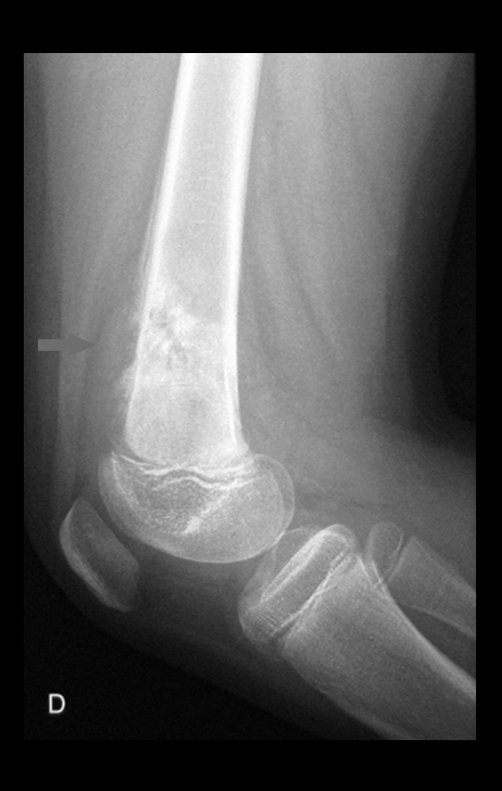
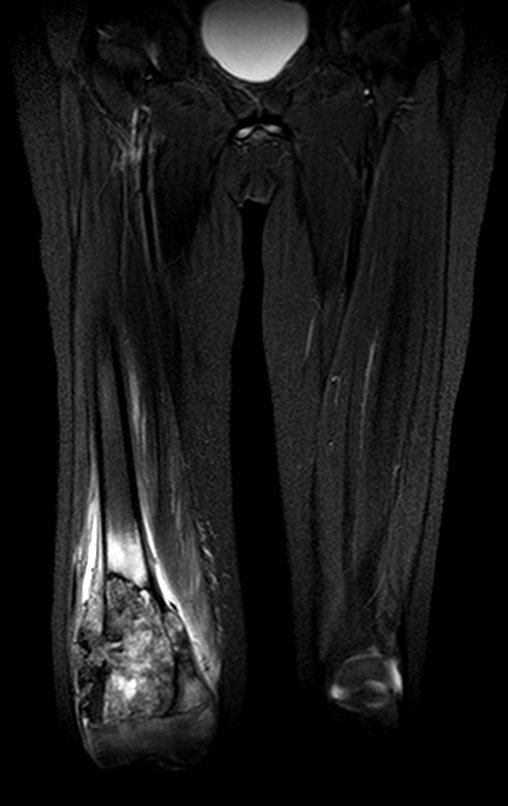
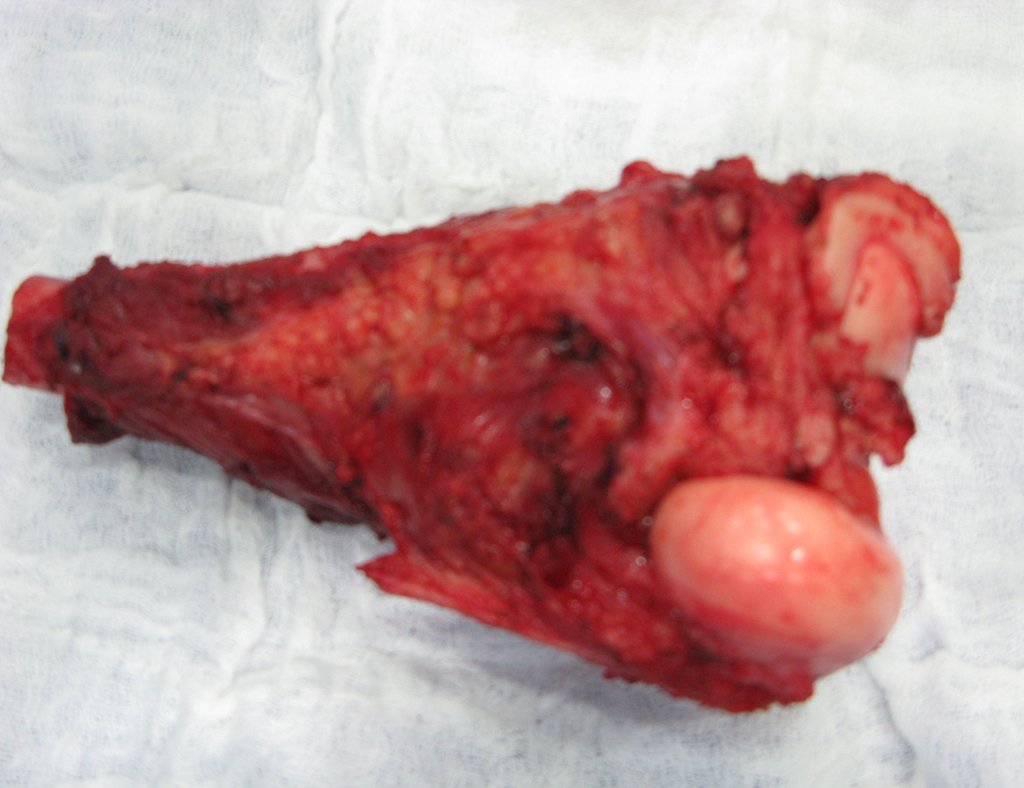
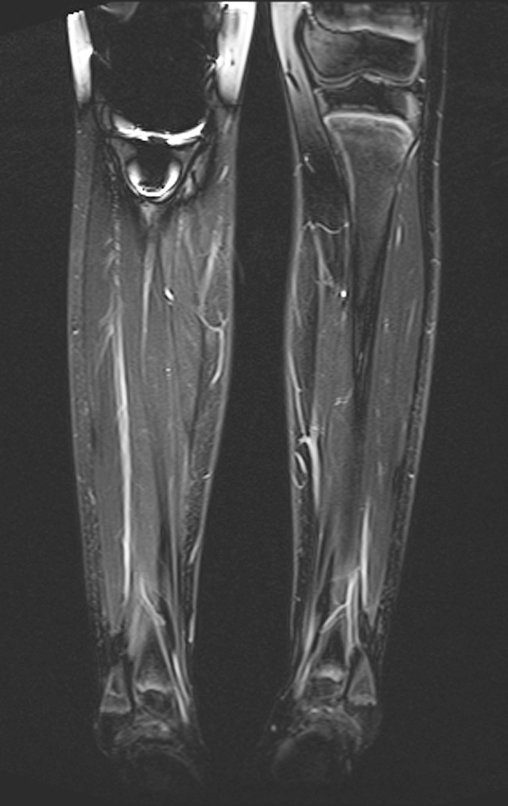
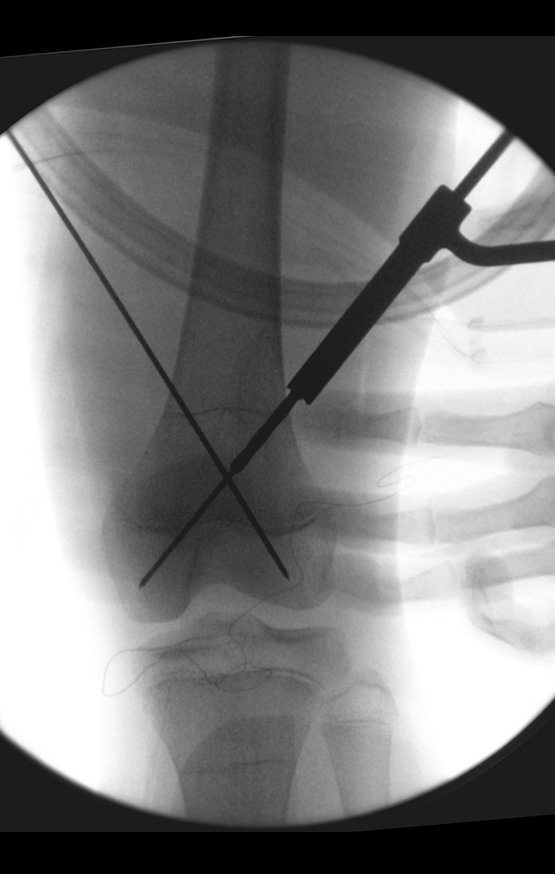
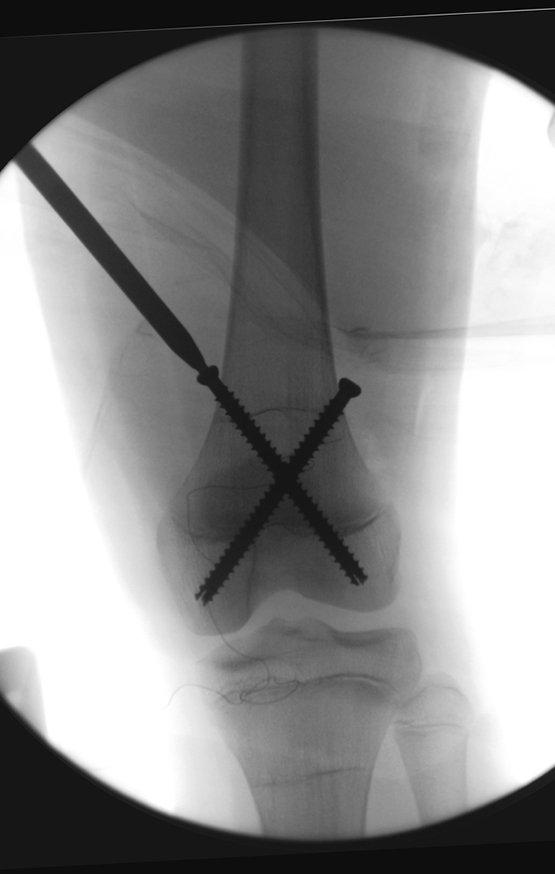
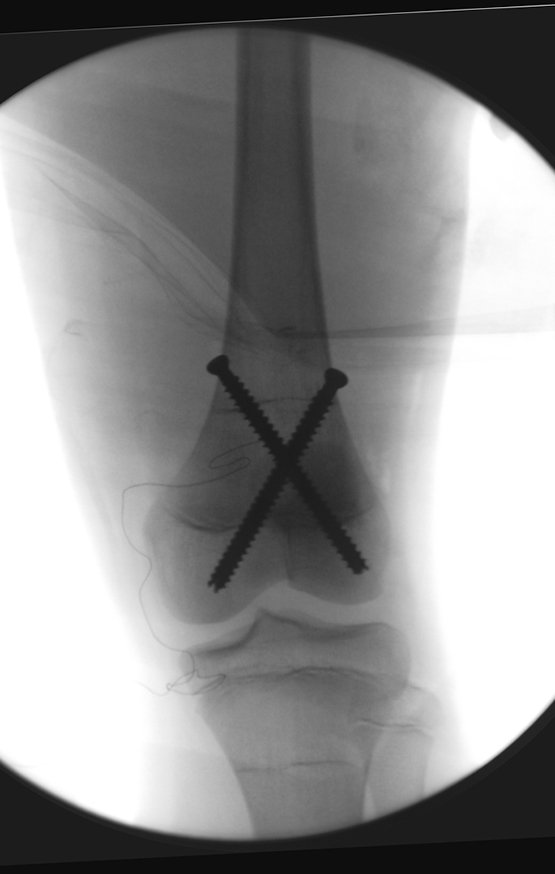
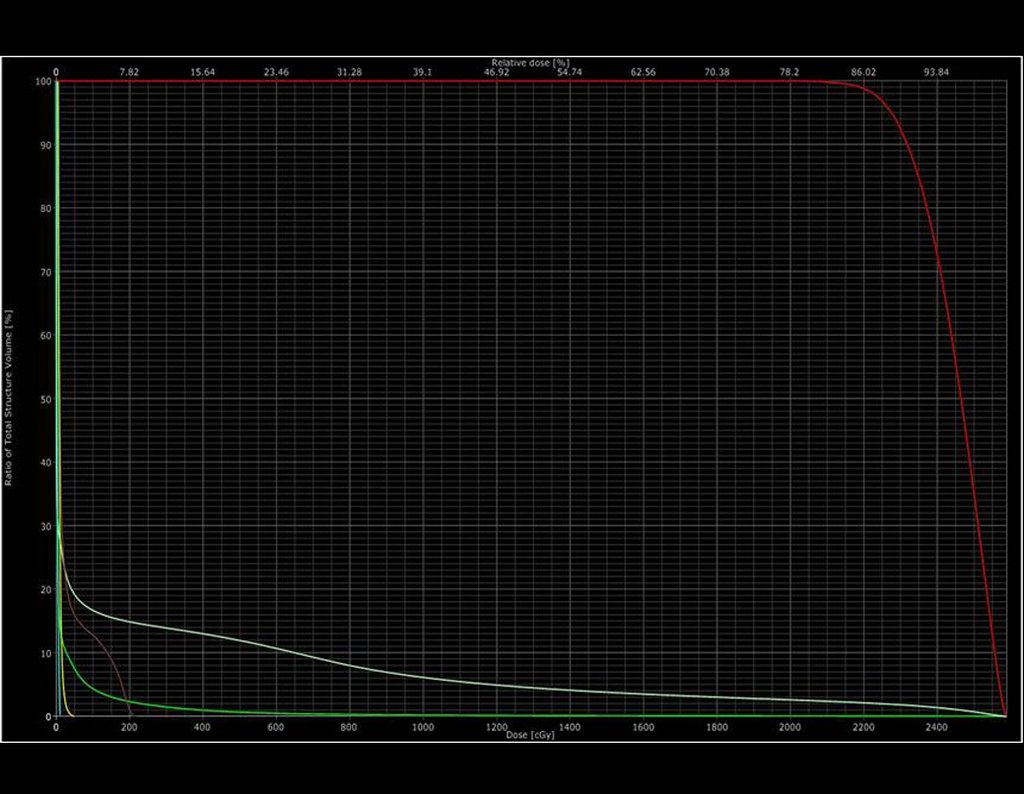
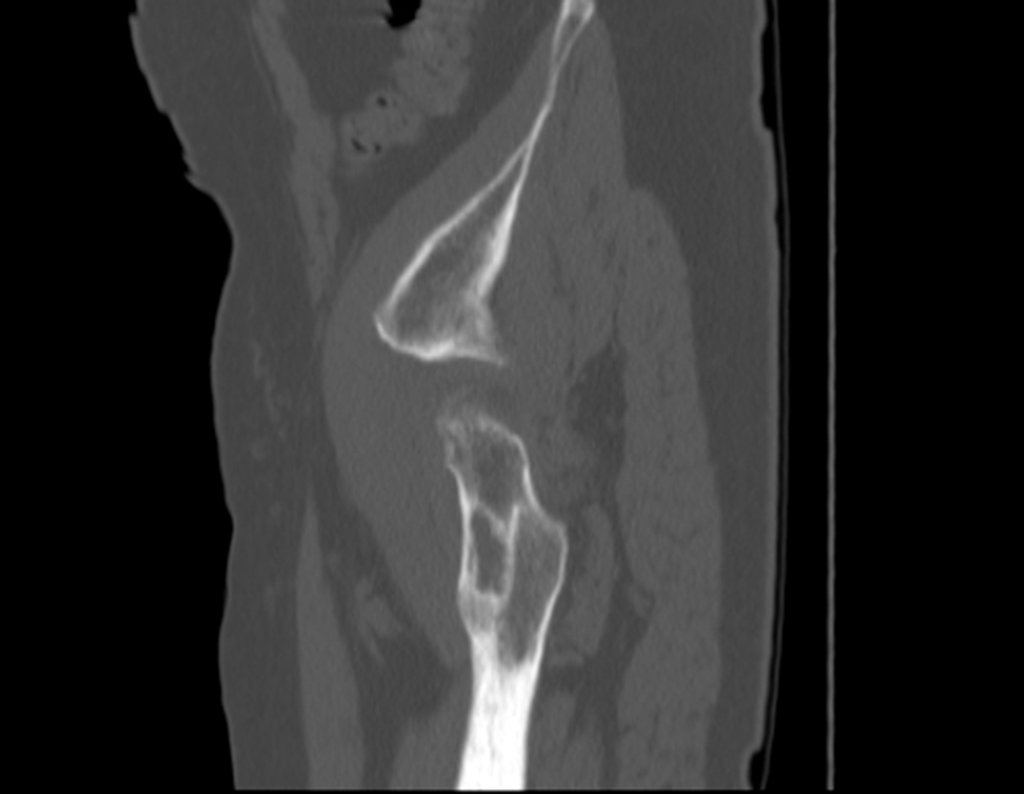
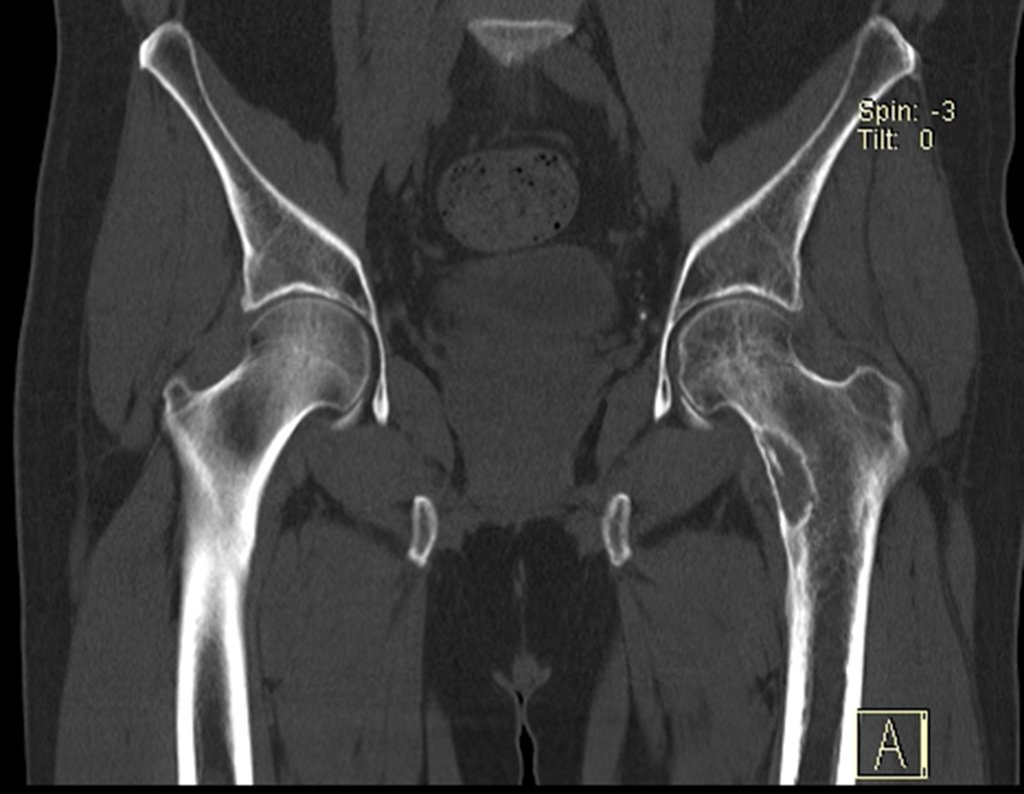
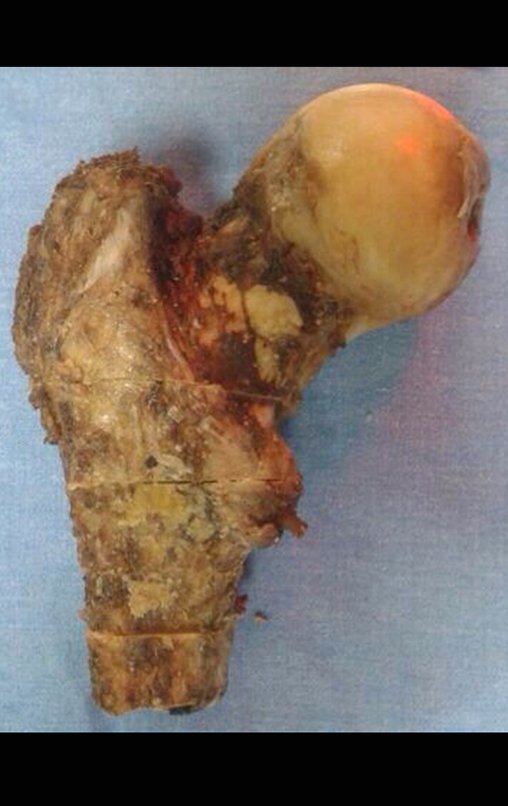
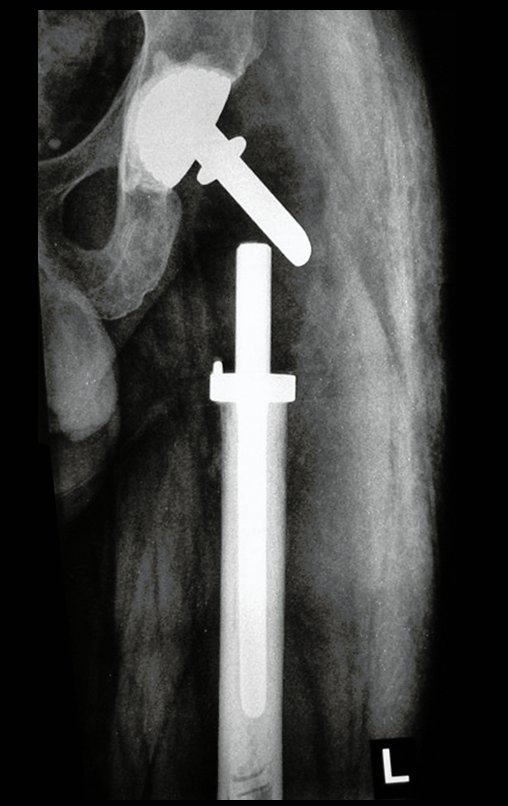
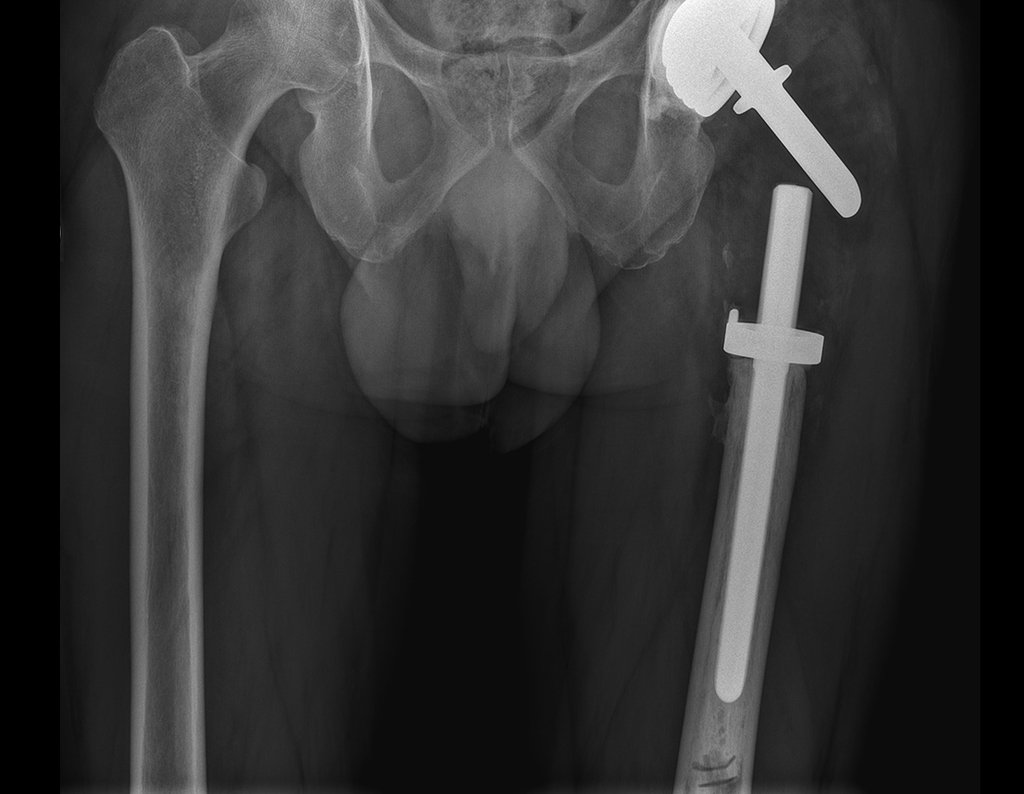
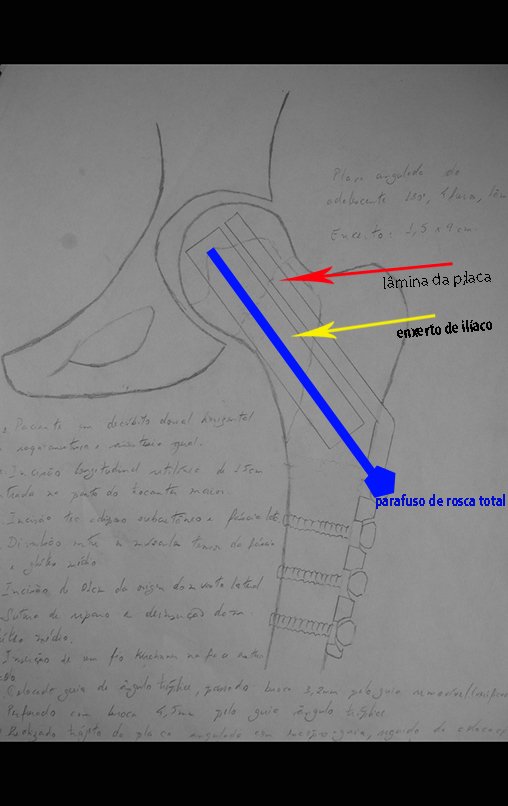
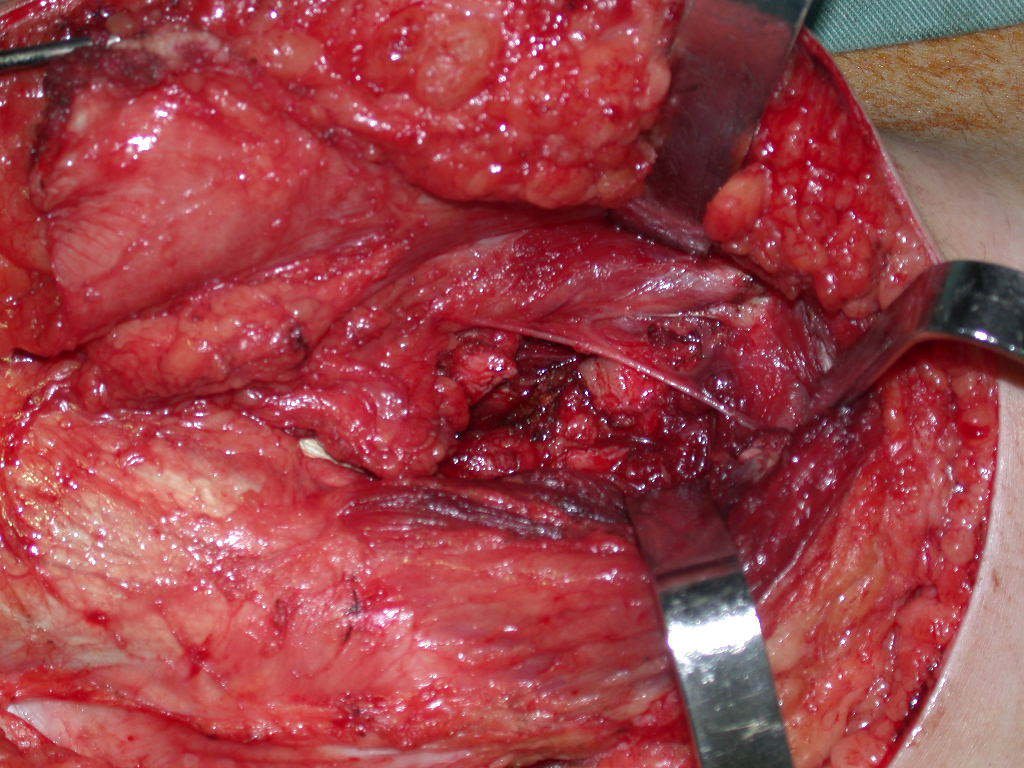
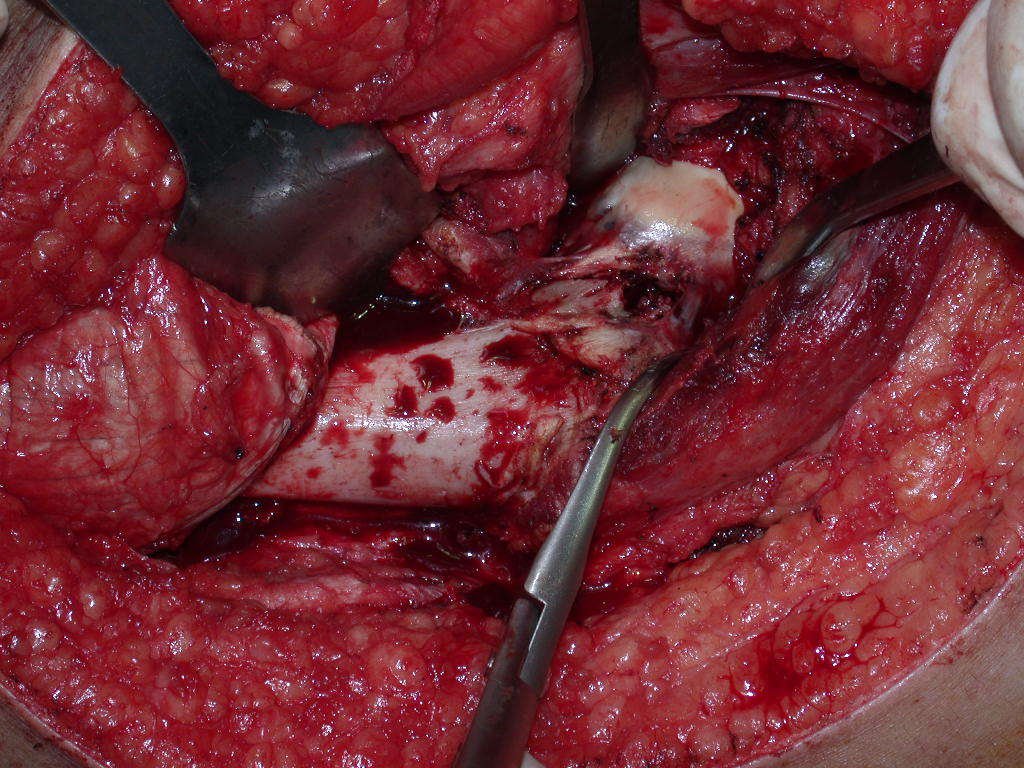
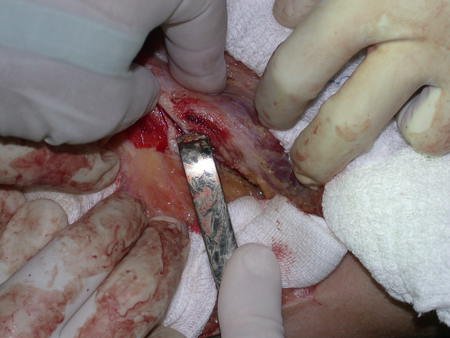
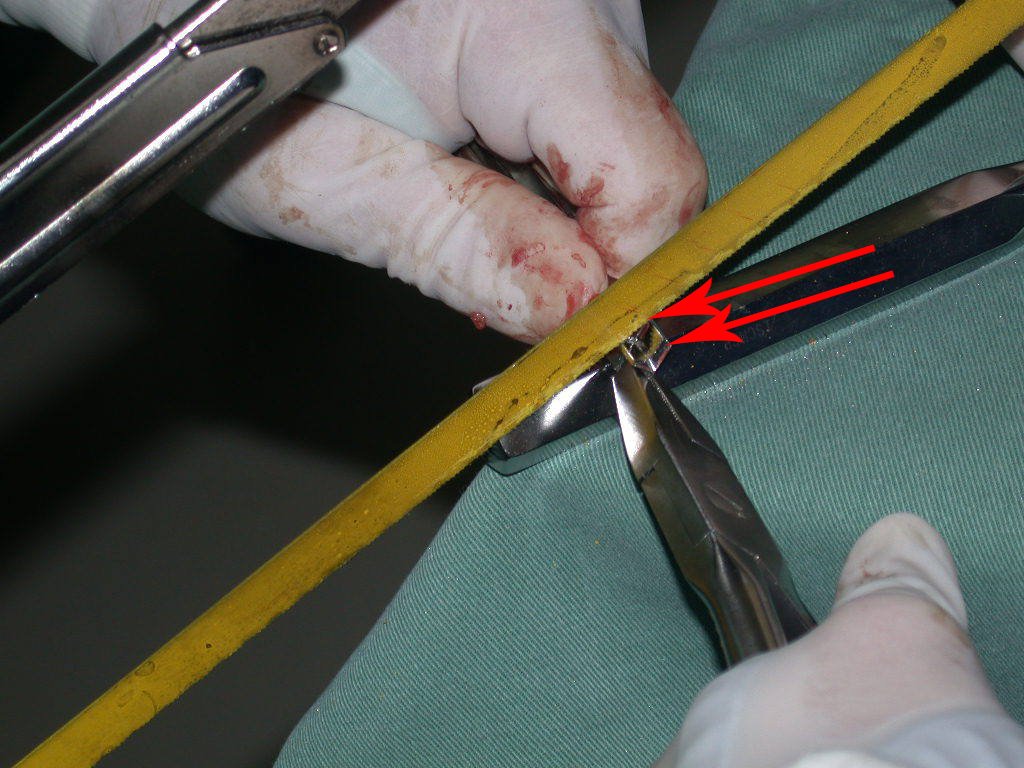
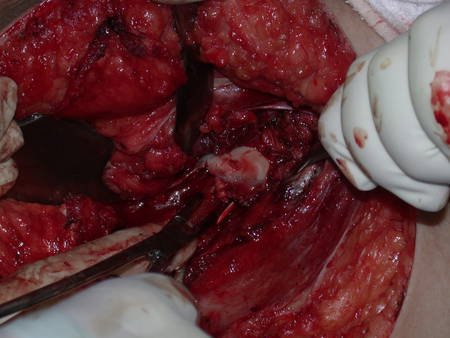
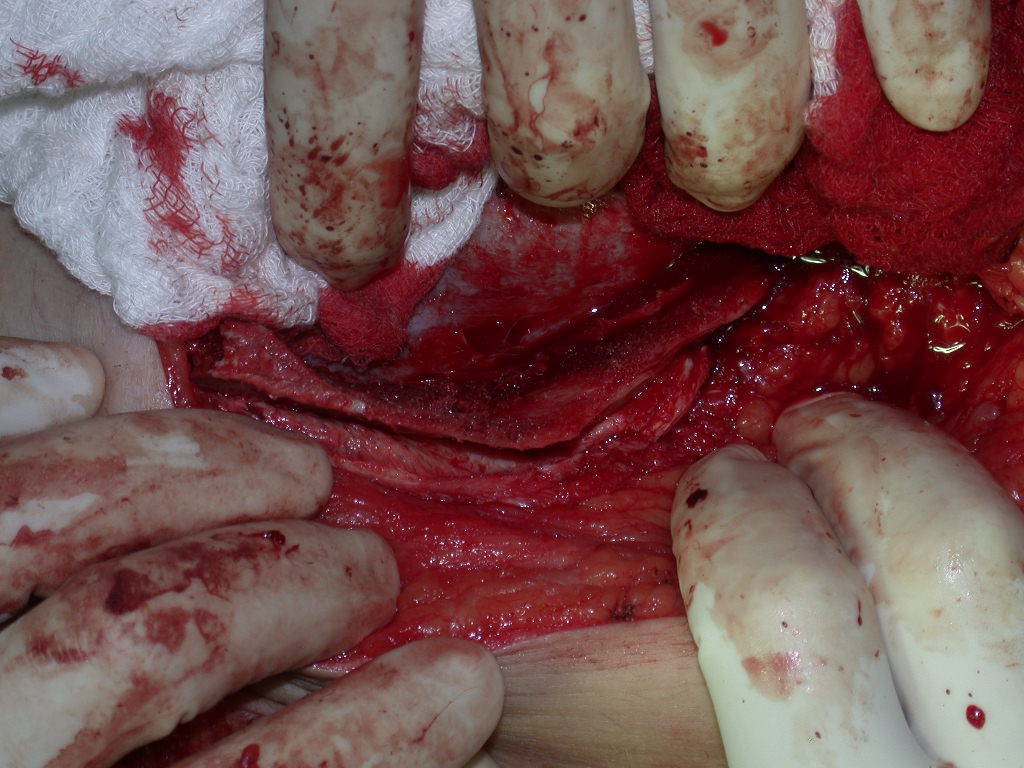
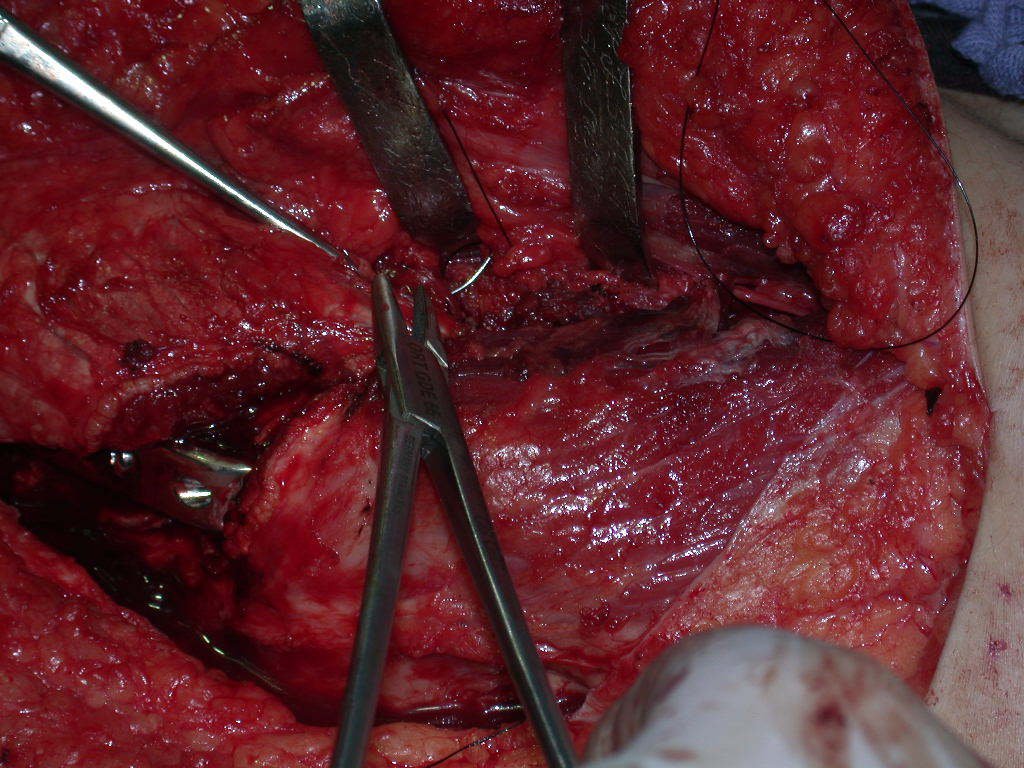
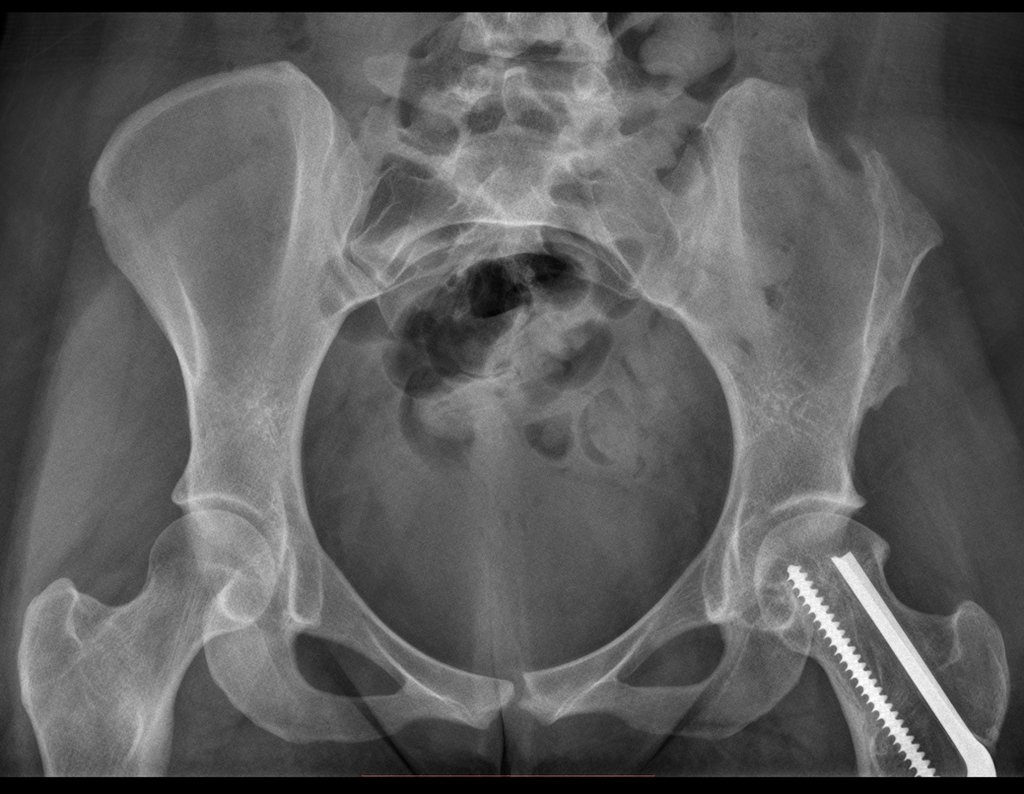
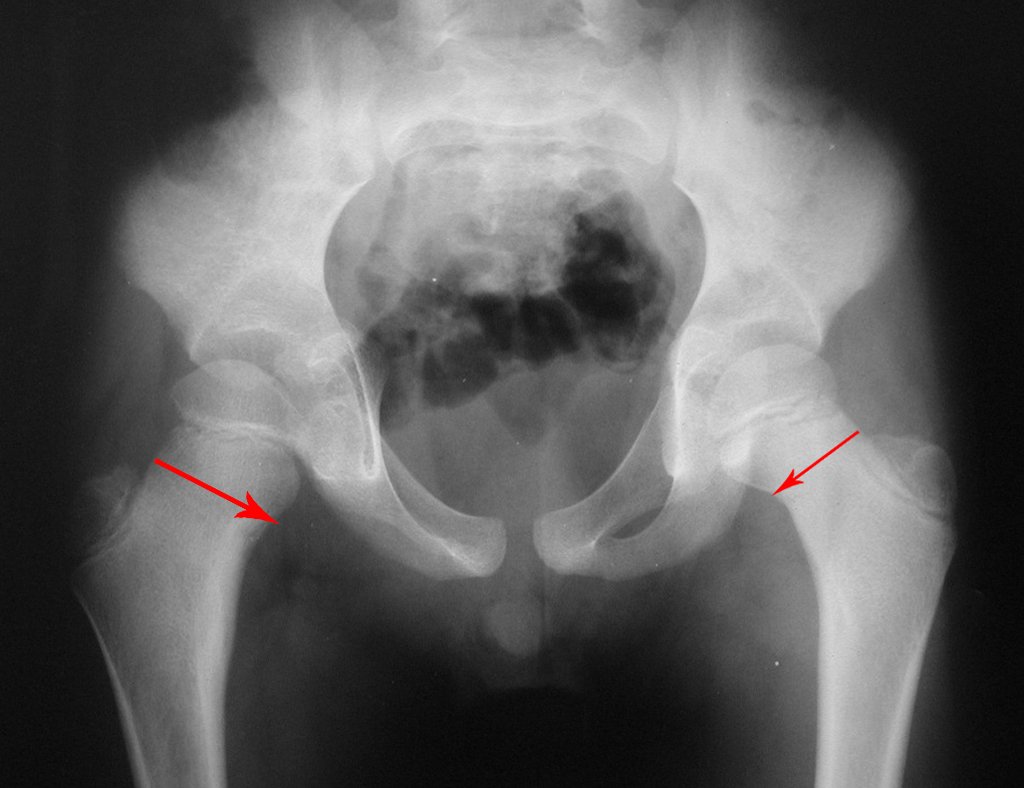
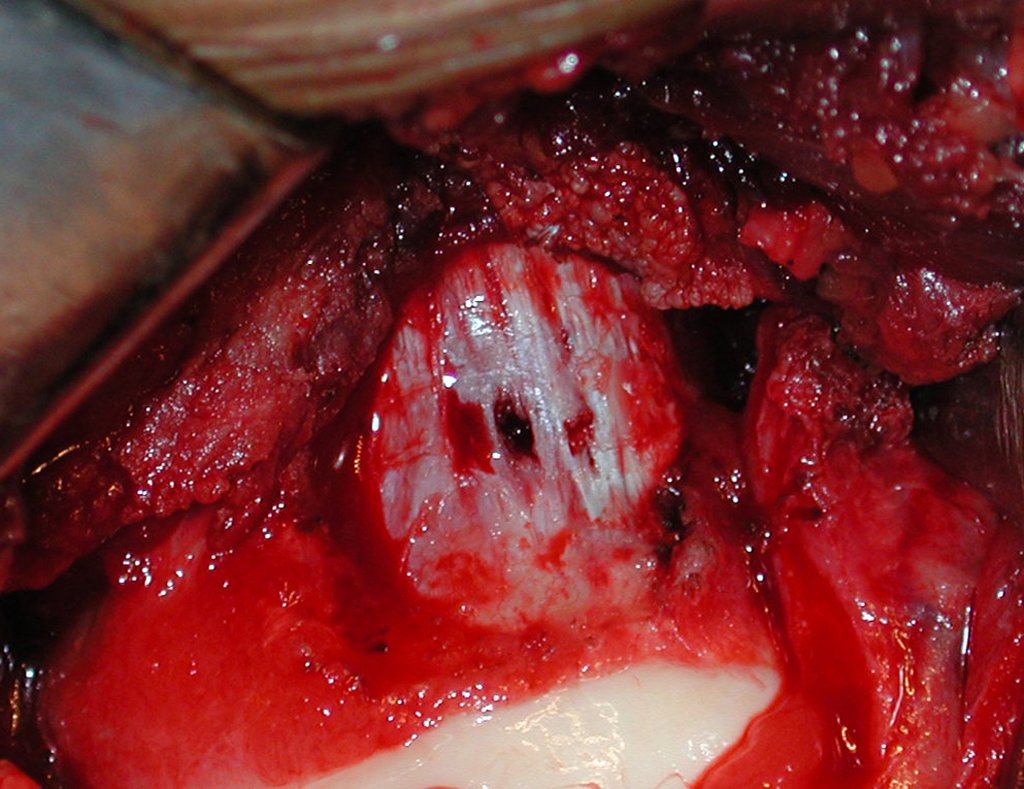
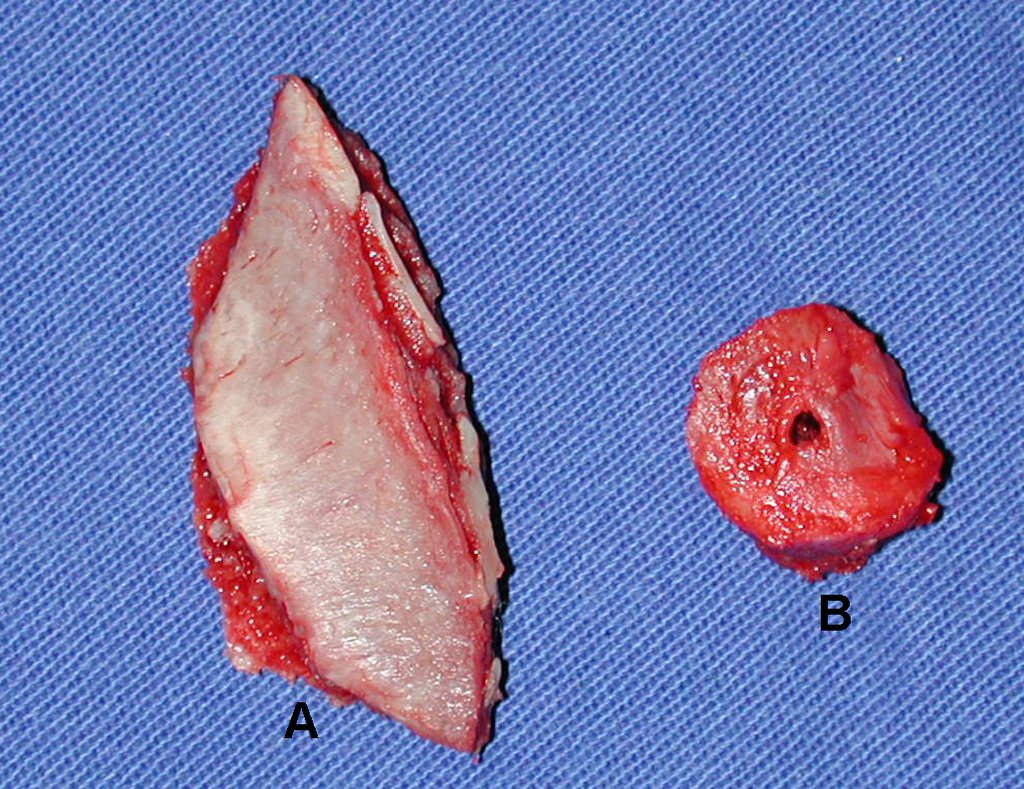
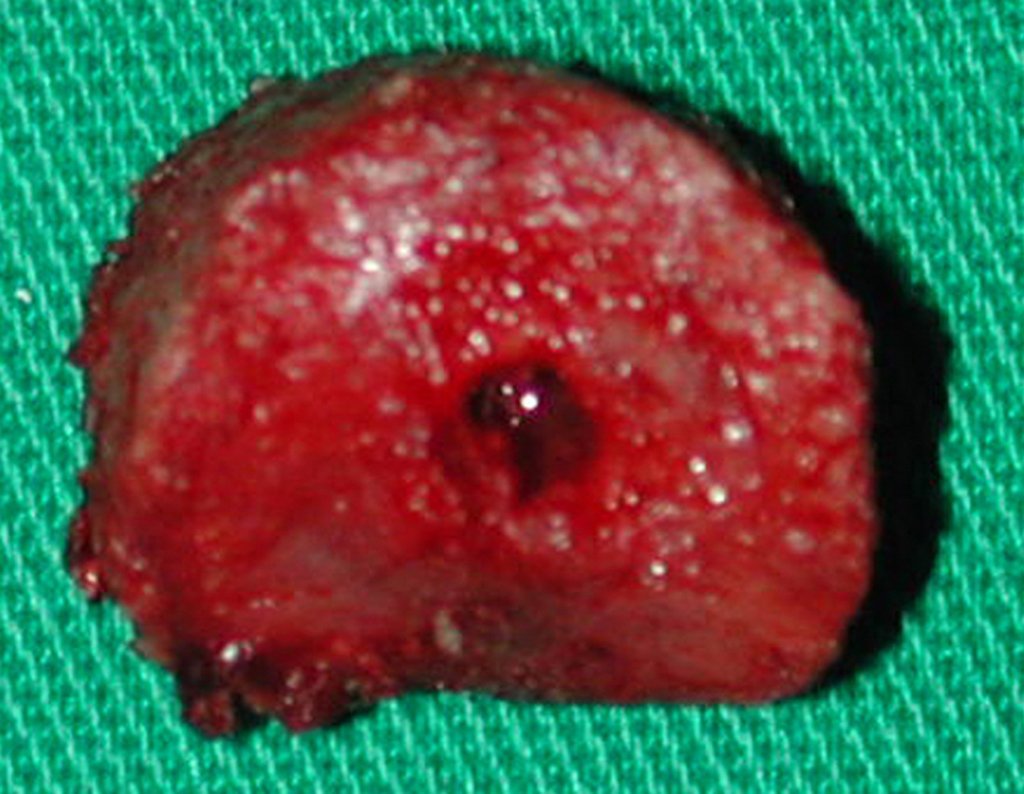
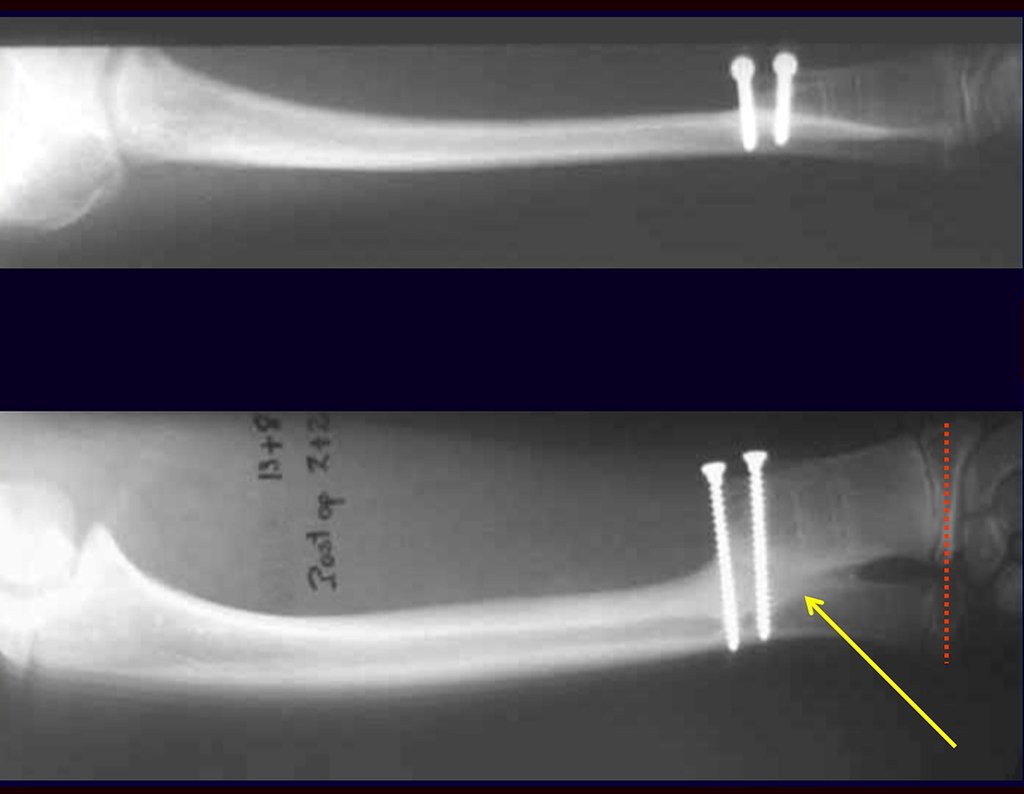
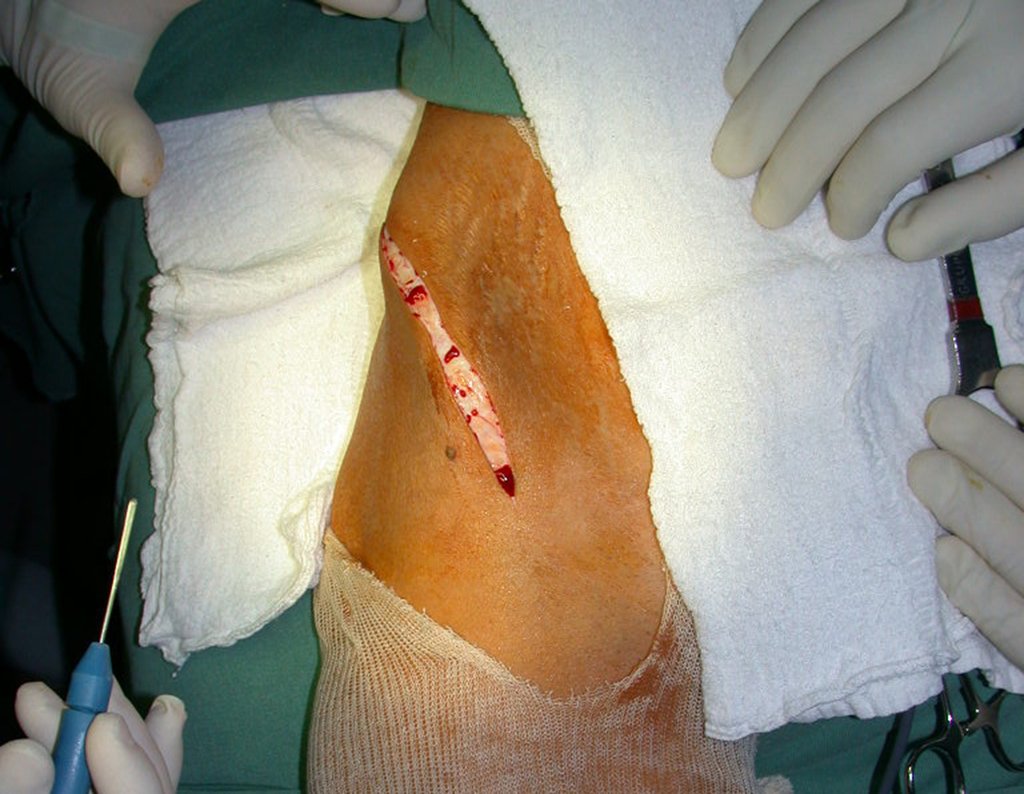
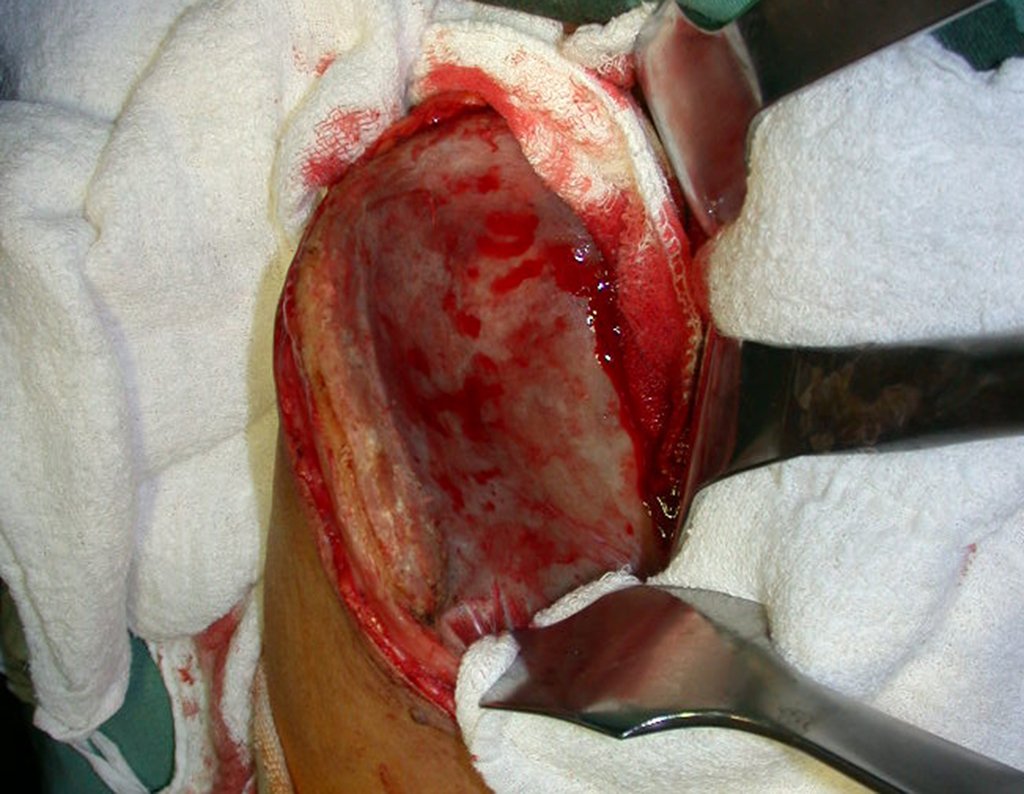
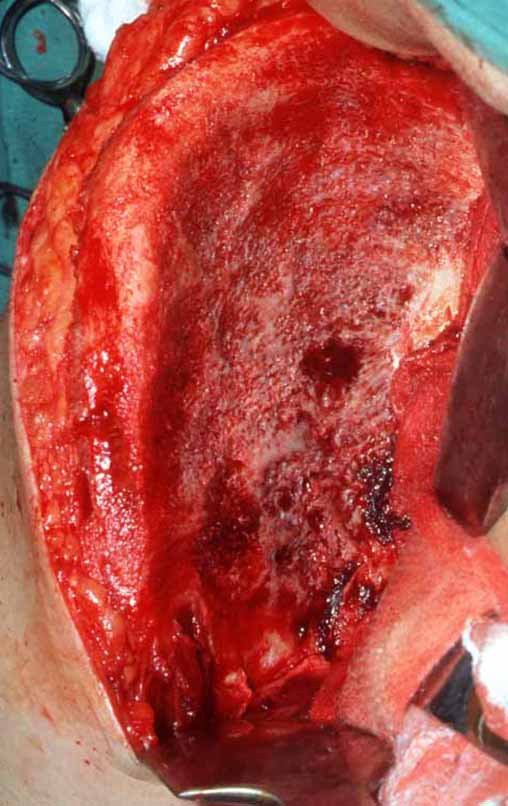
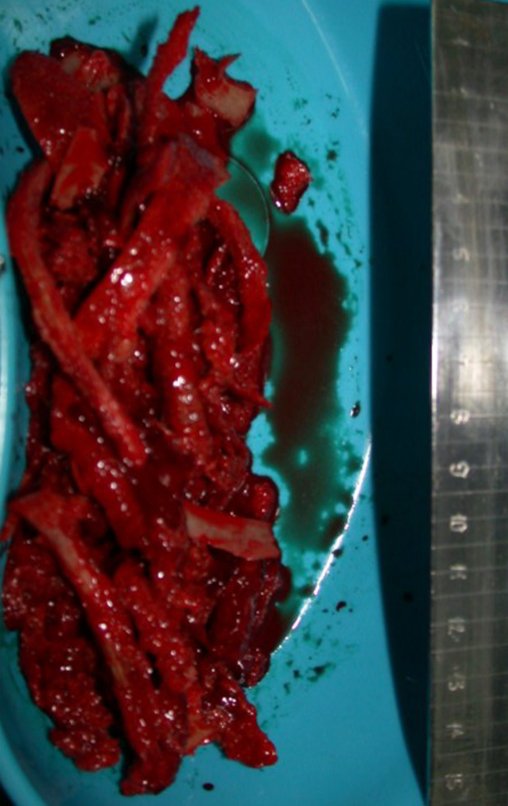
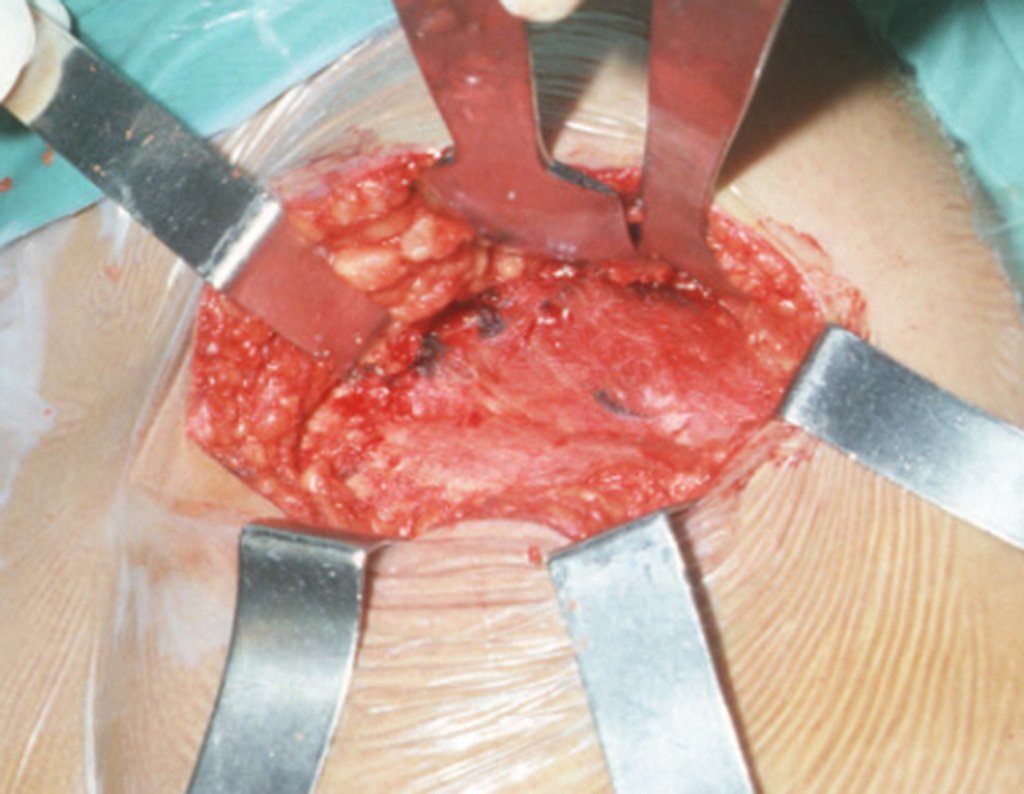
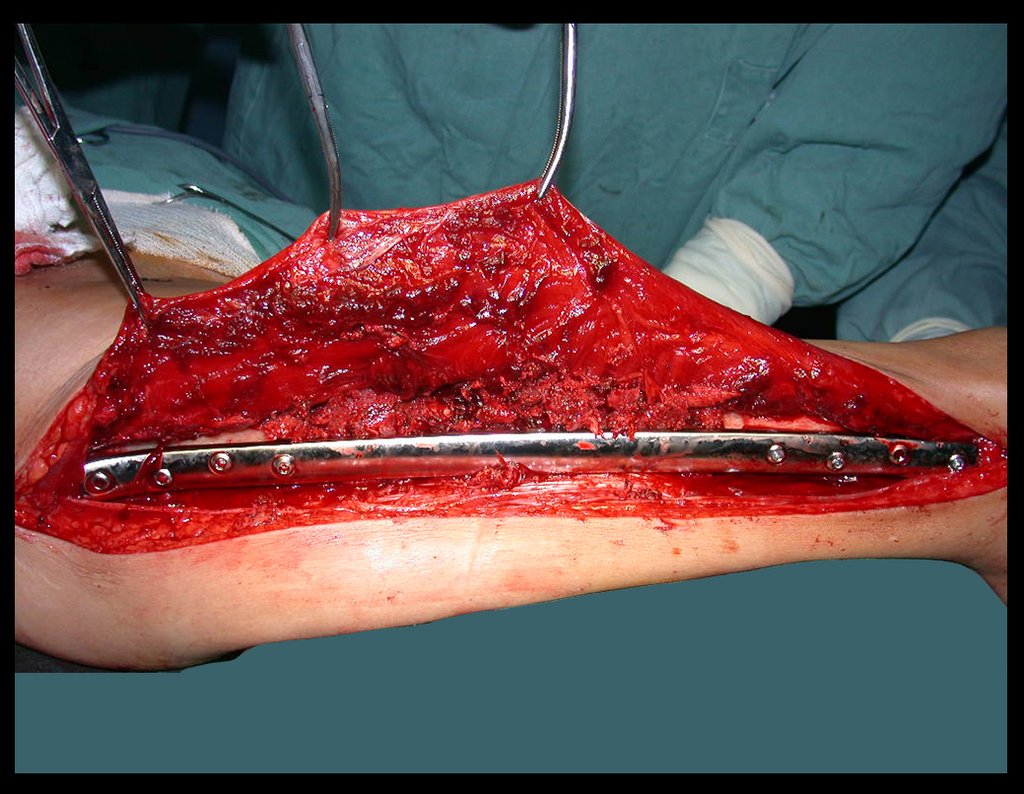
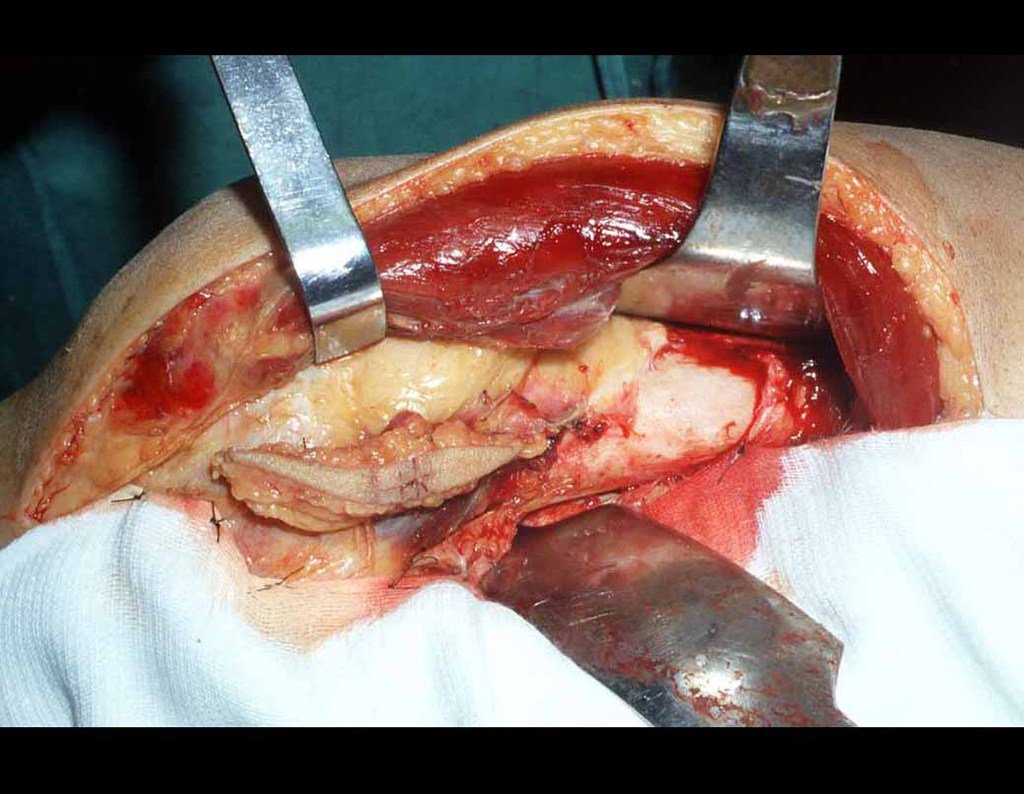
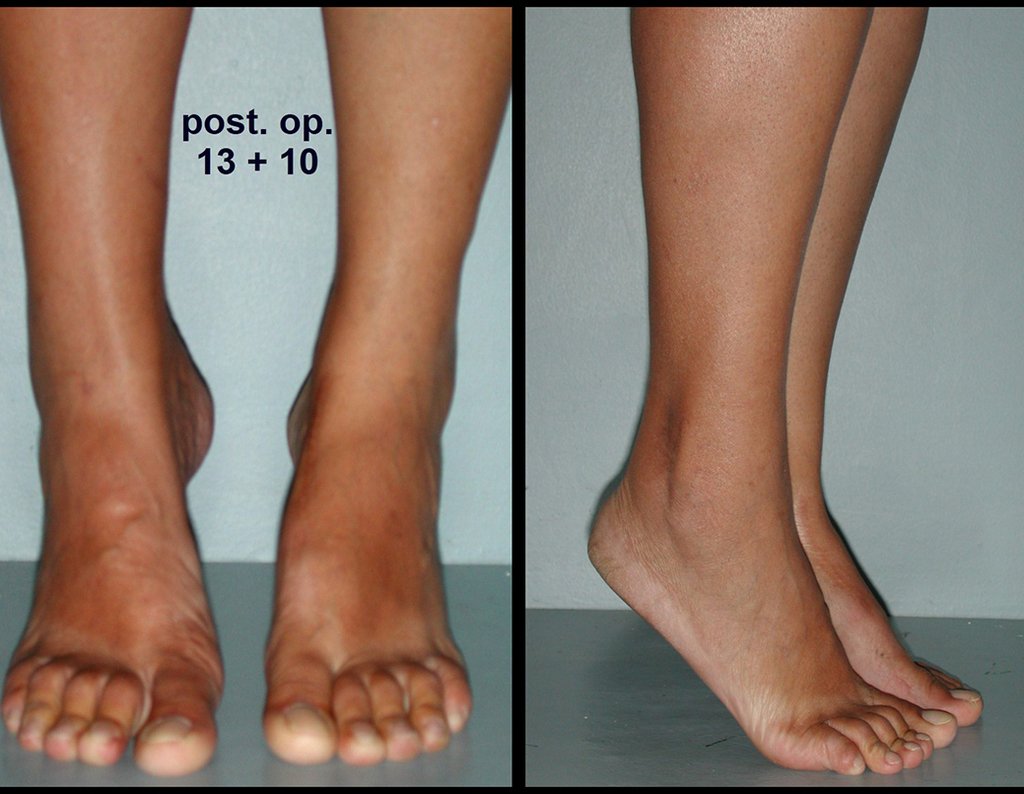
Trata-se portanto de lesão benigna e segundo Enneking pode classificar-se como benigna ativa ou agressiva. A presença de áreas de fibrose e ossificação reparadora esta relacionada a regressão do cisto ou resultado de fratura prévia (fig 2).
As lojas ocorrem em número e tamanho variados, aglomerando-se e provocando erosão do trabeculado ósseo, que se expandem e insuflam a cortical. Histológicamente observam-se lacunas sanguíneas separadas entre si por septos conjuntivos e células osteoclásticas, sem atipias.
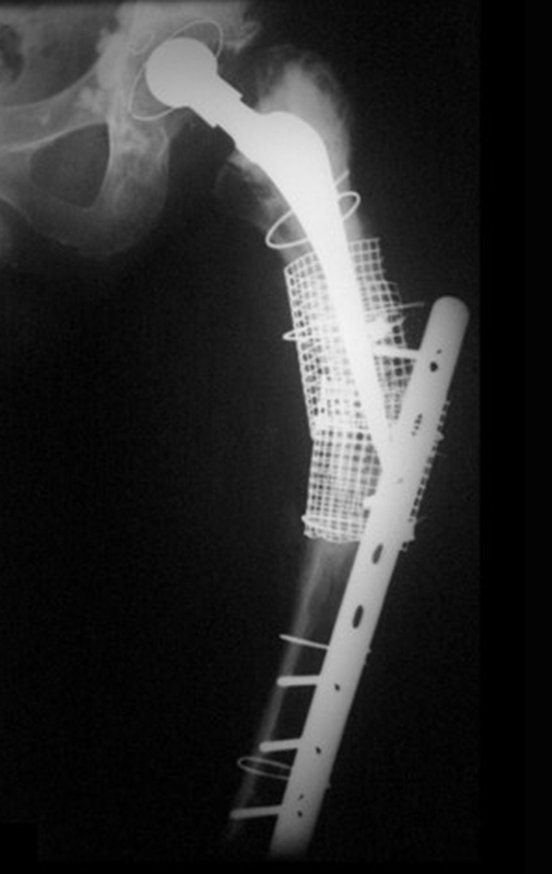
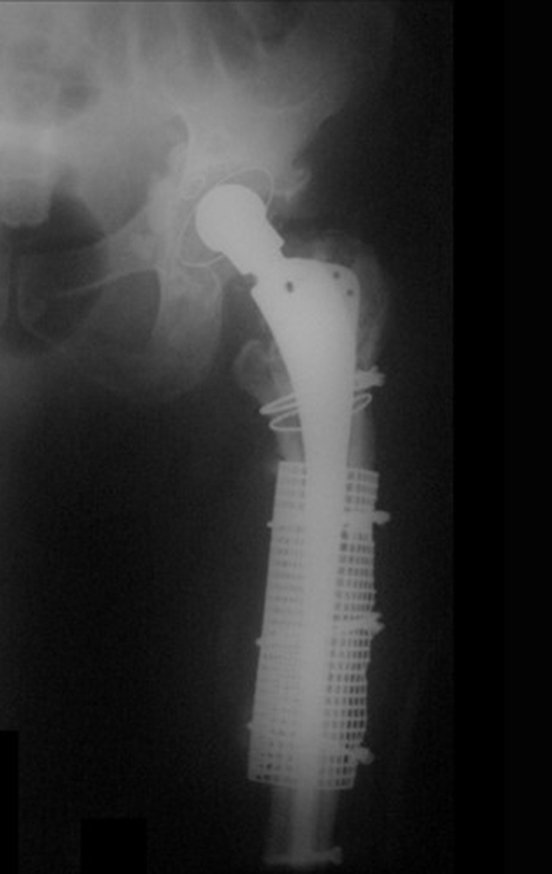
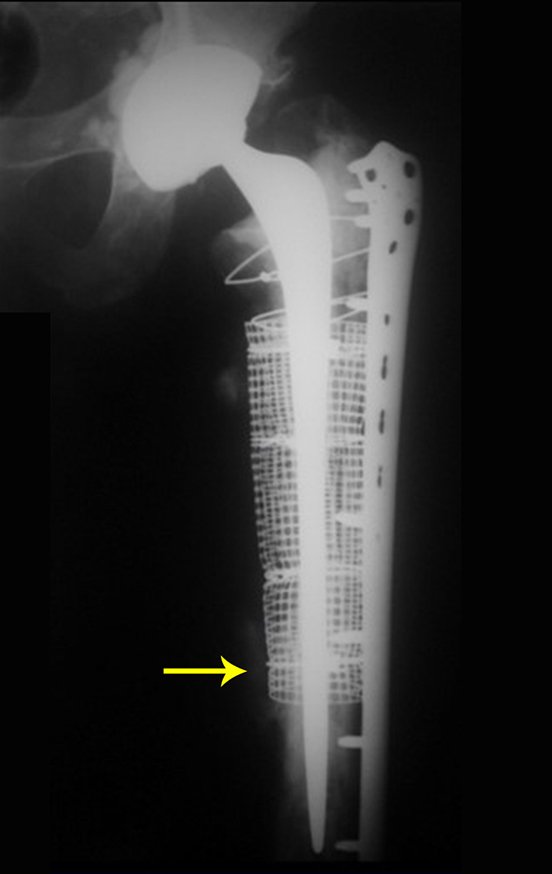
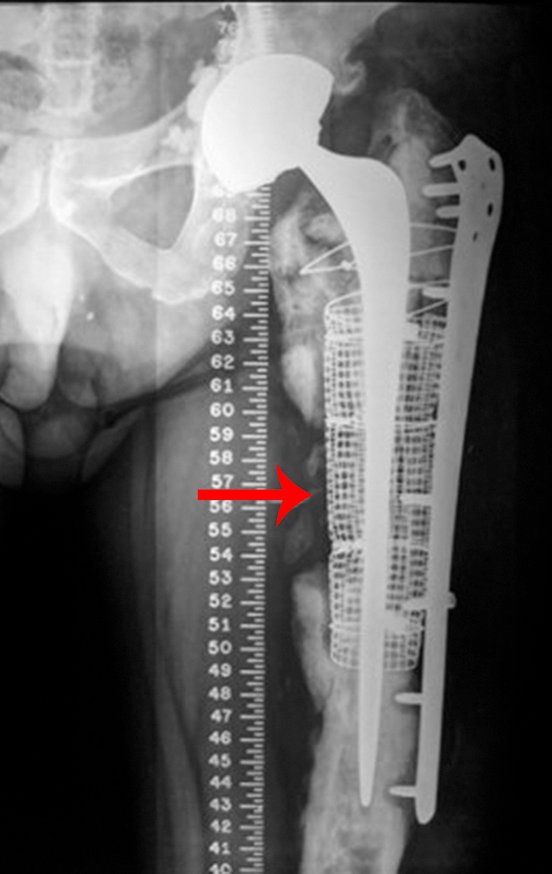
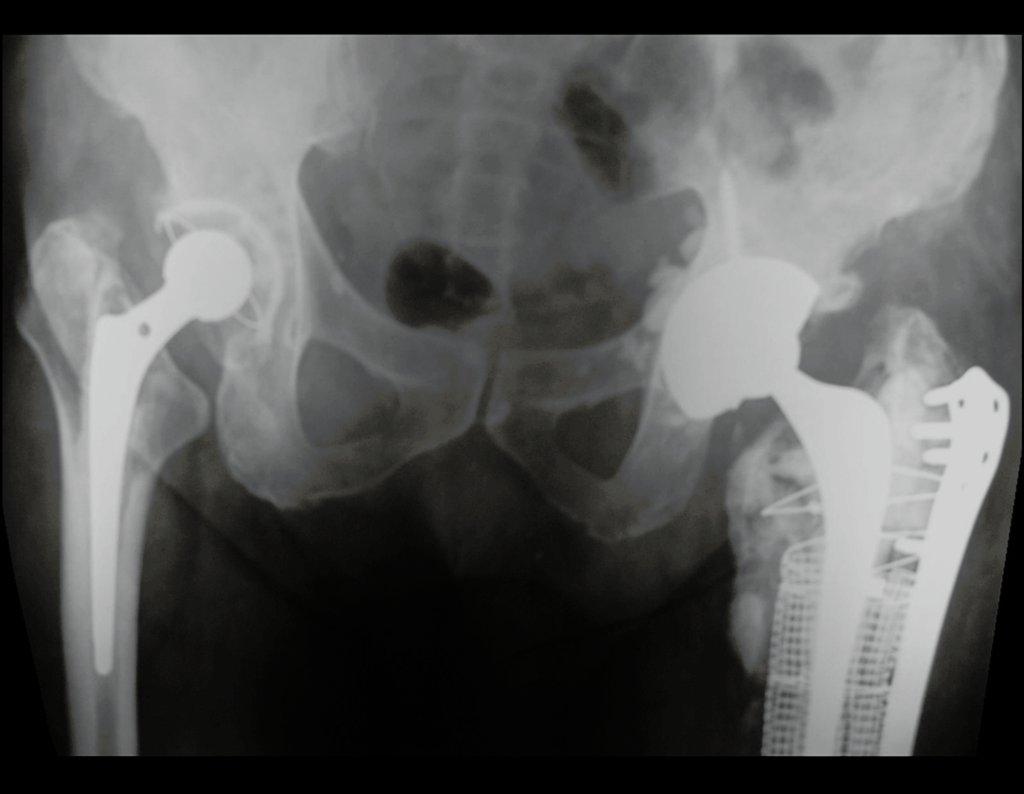
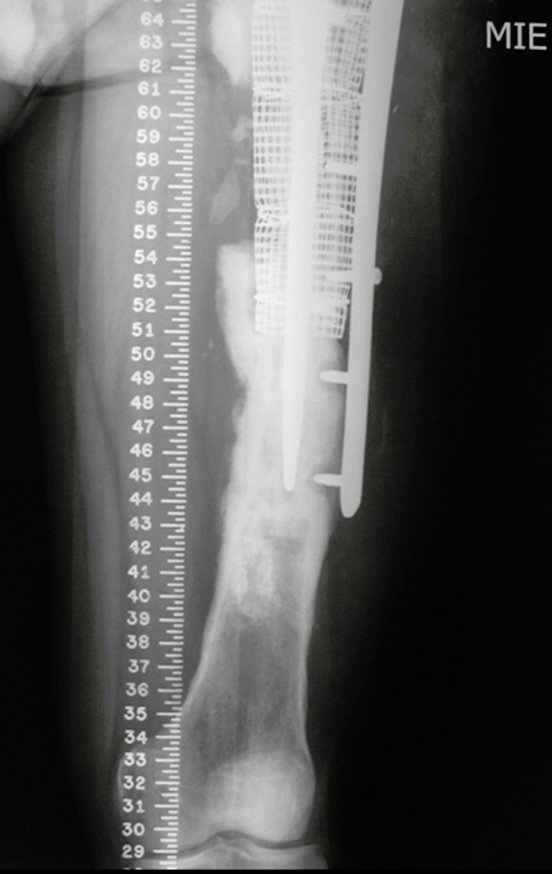
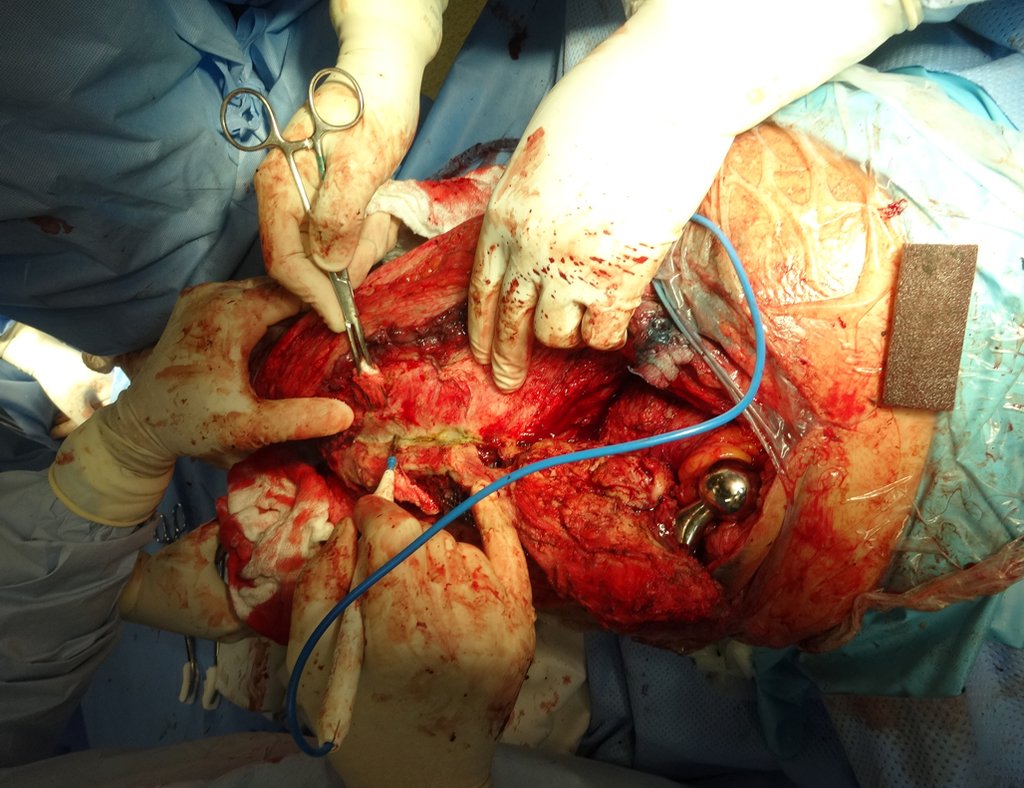
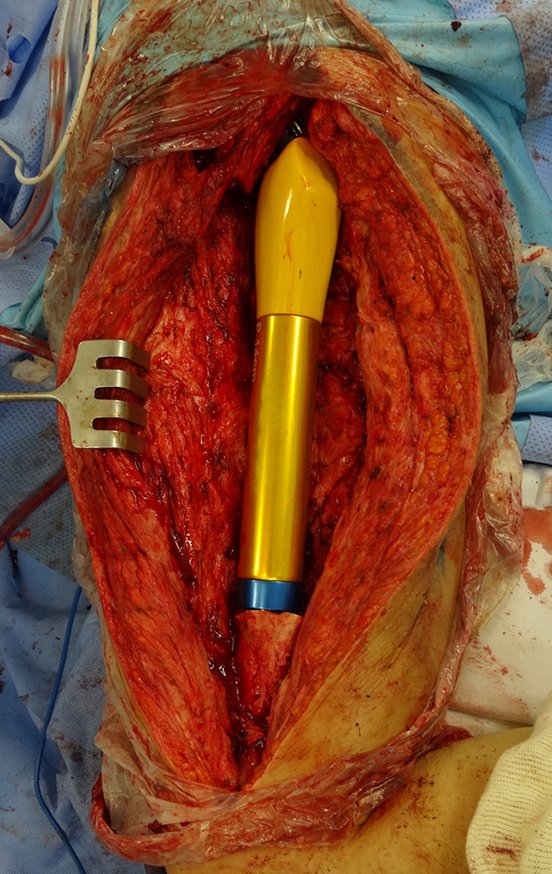
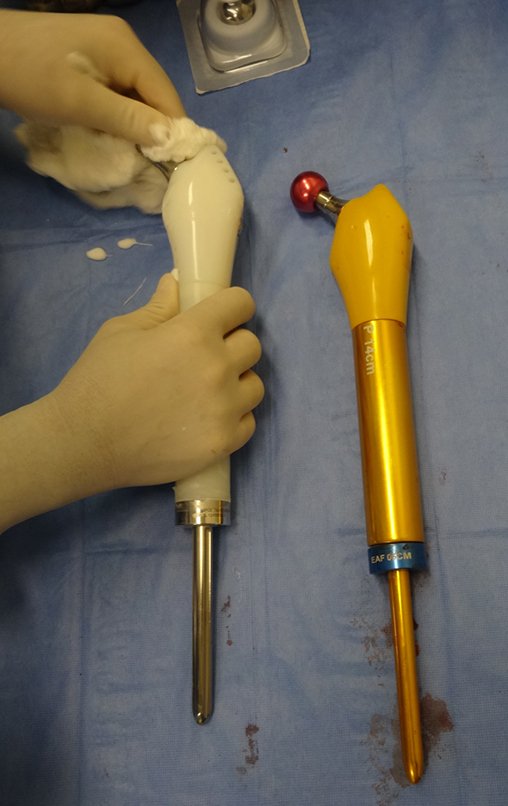
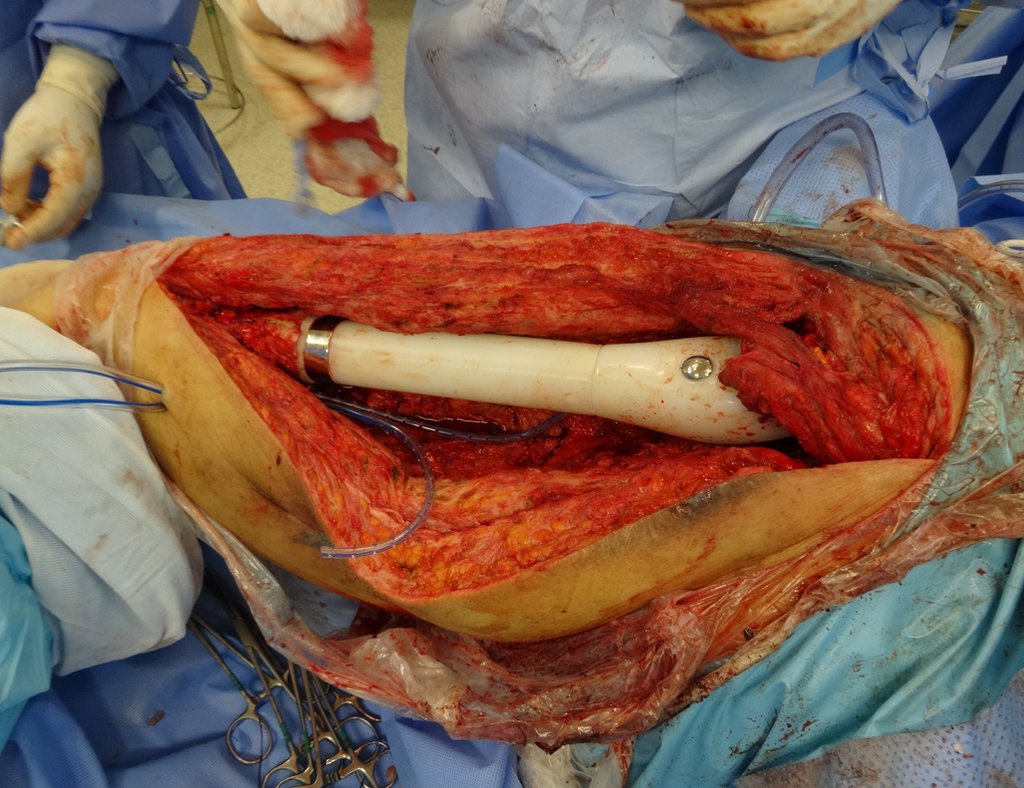
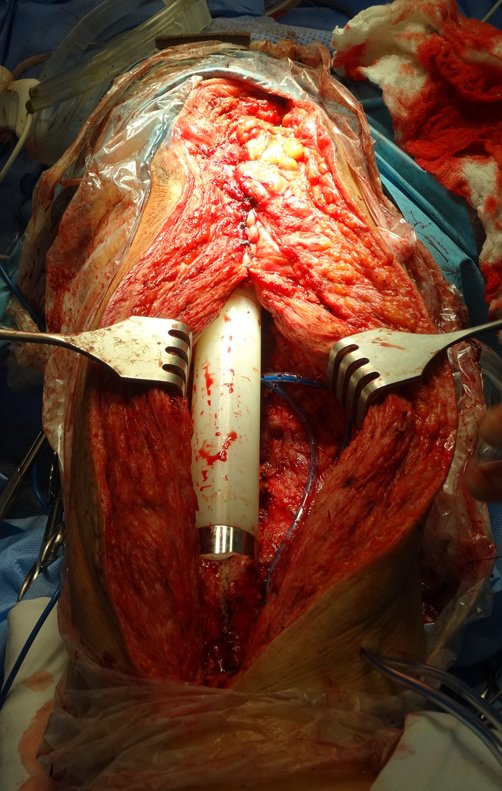
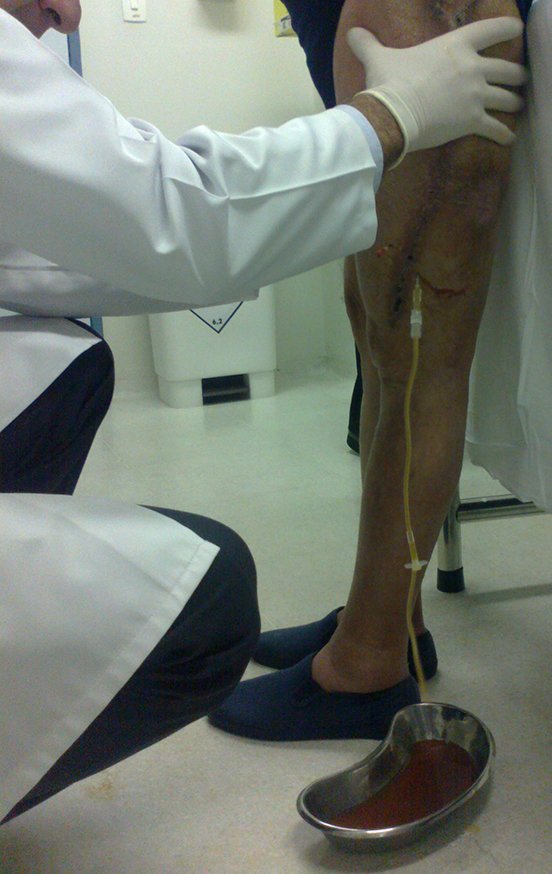
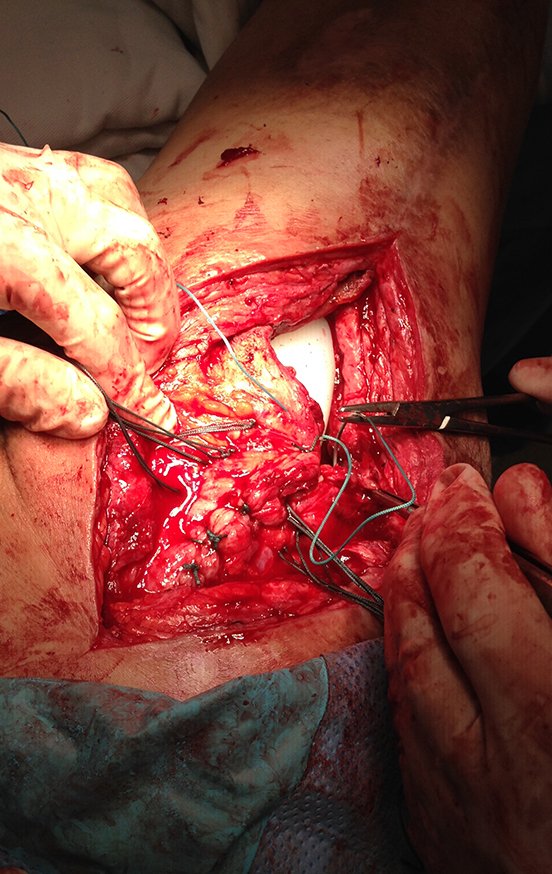
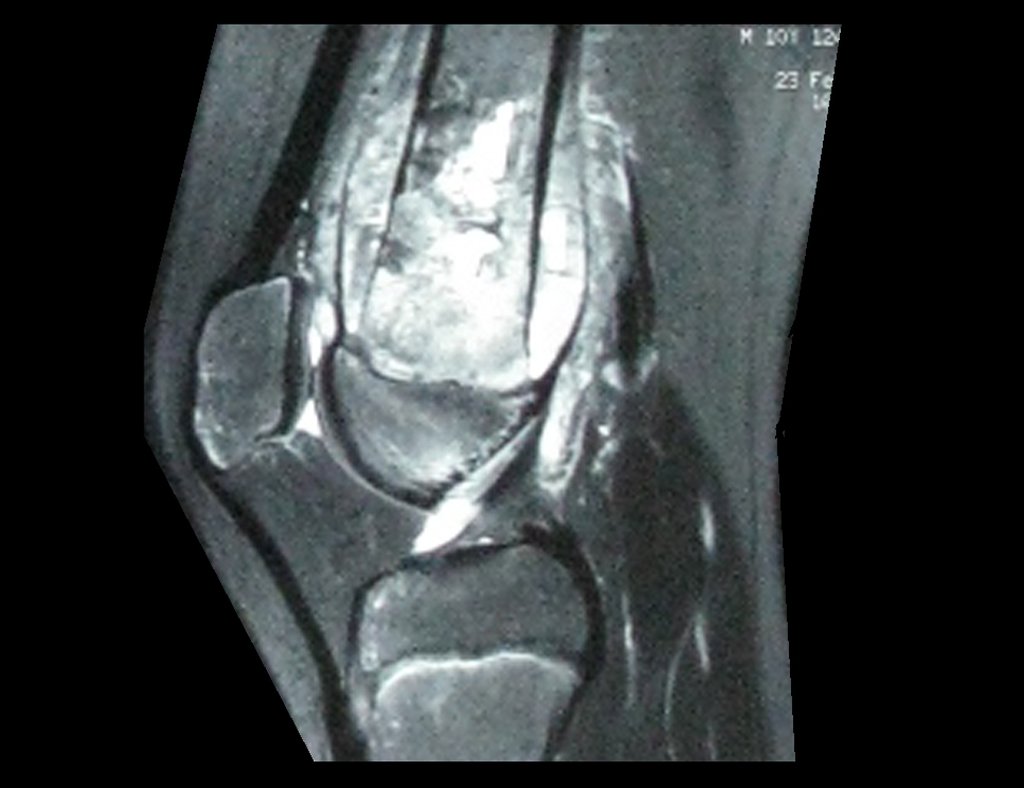
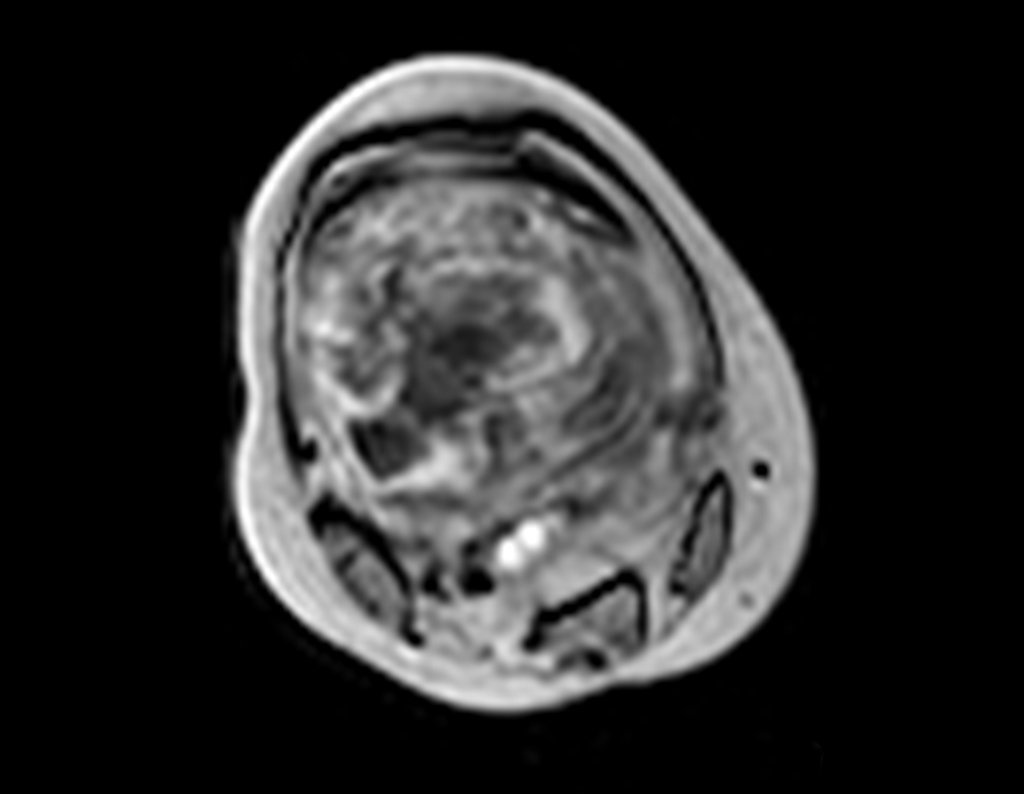
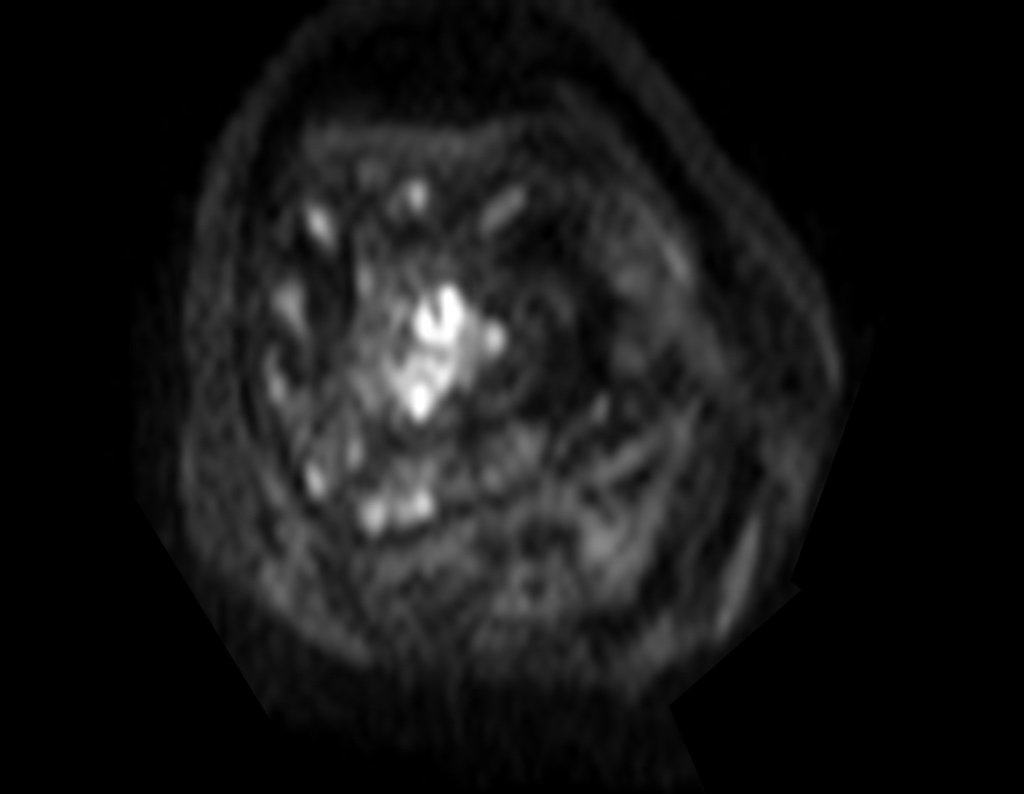
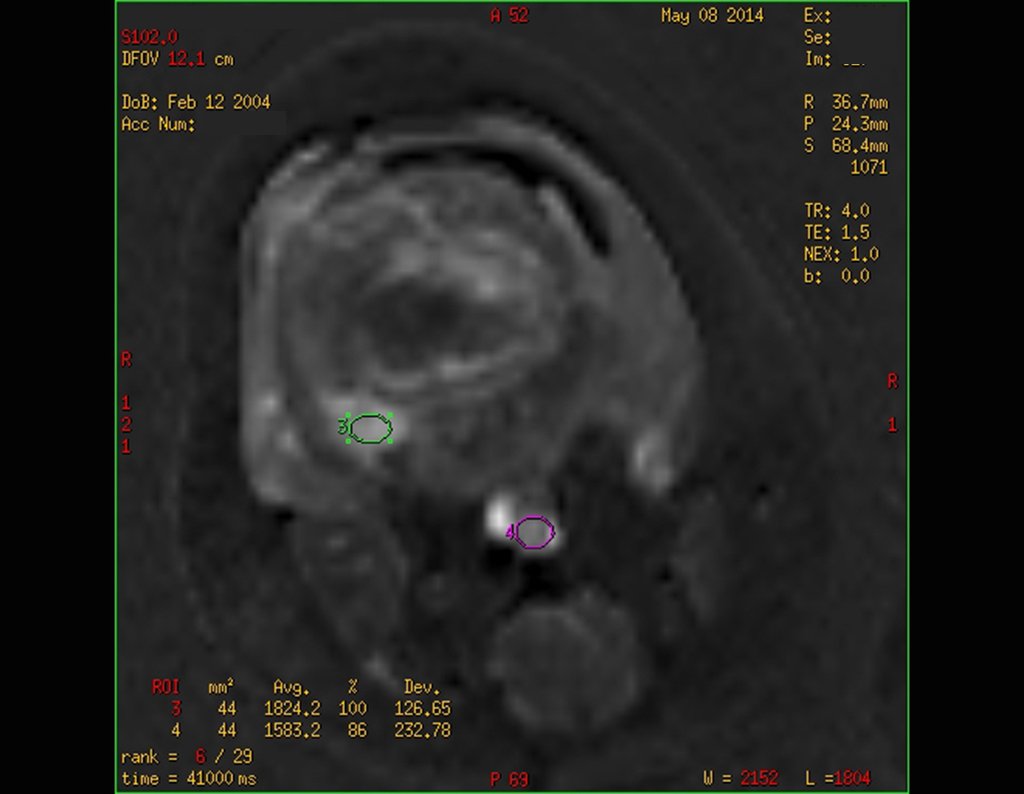
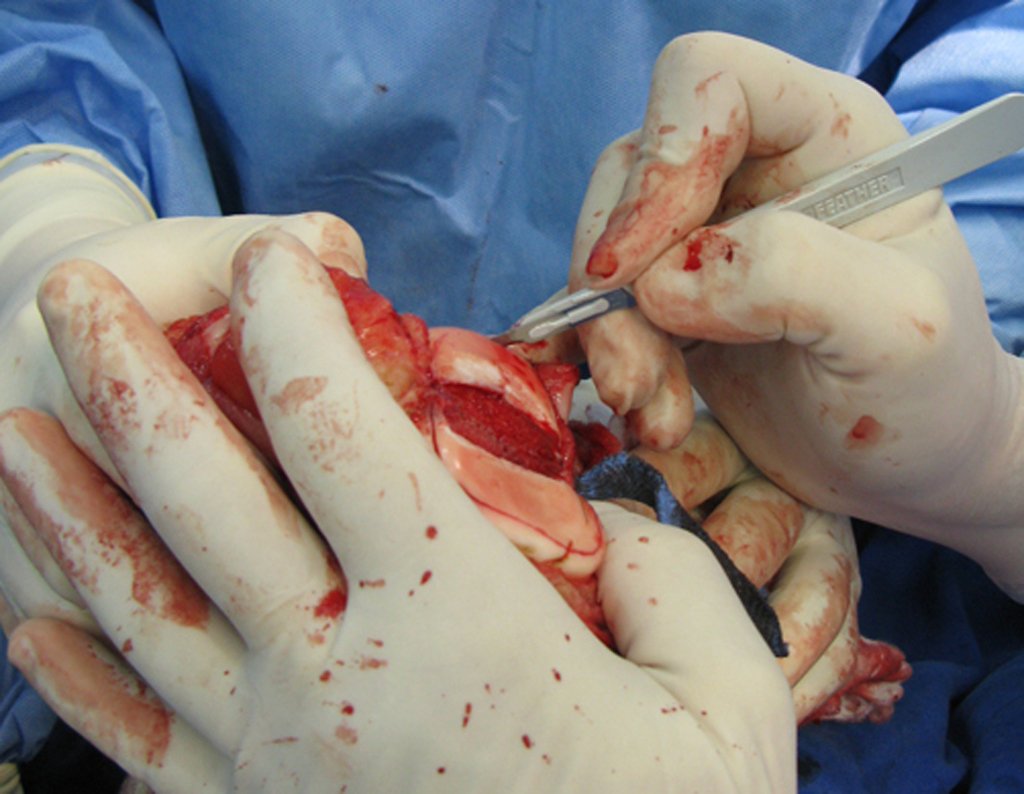
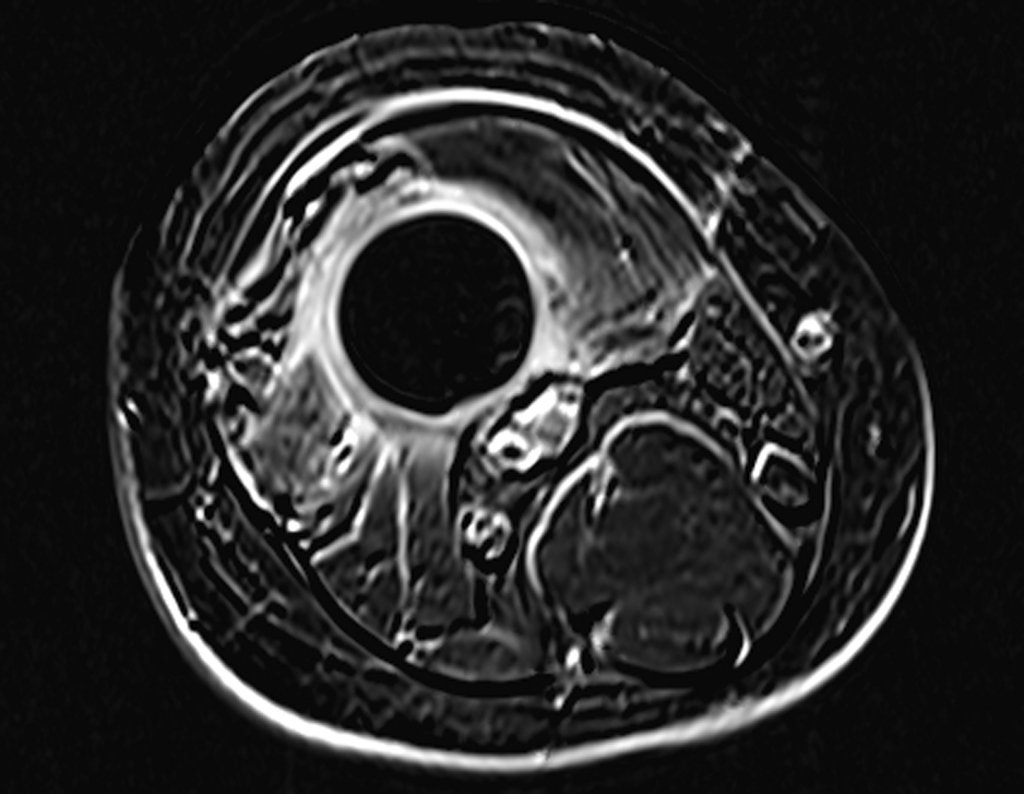
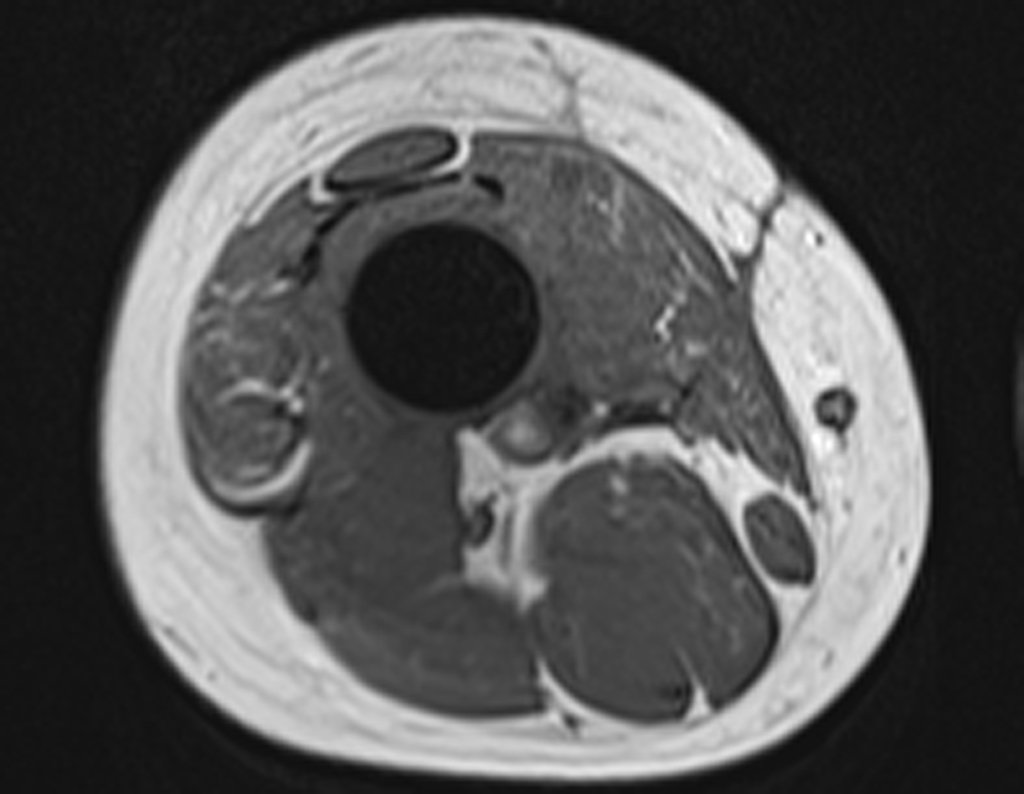
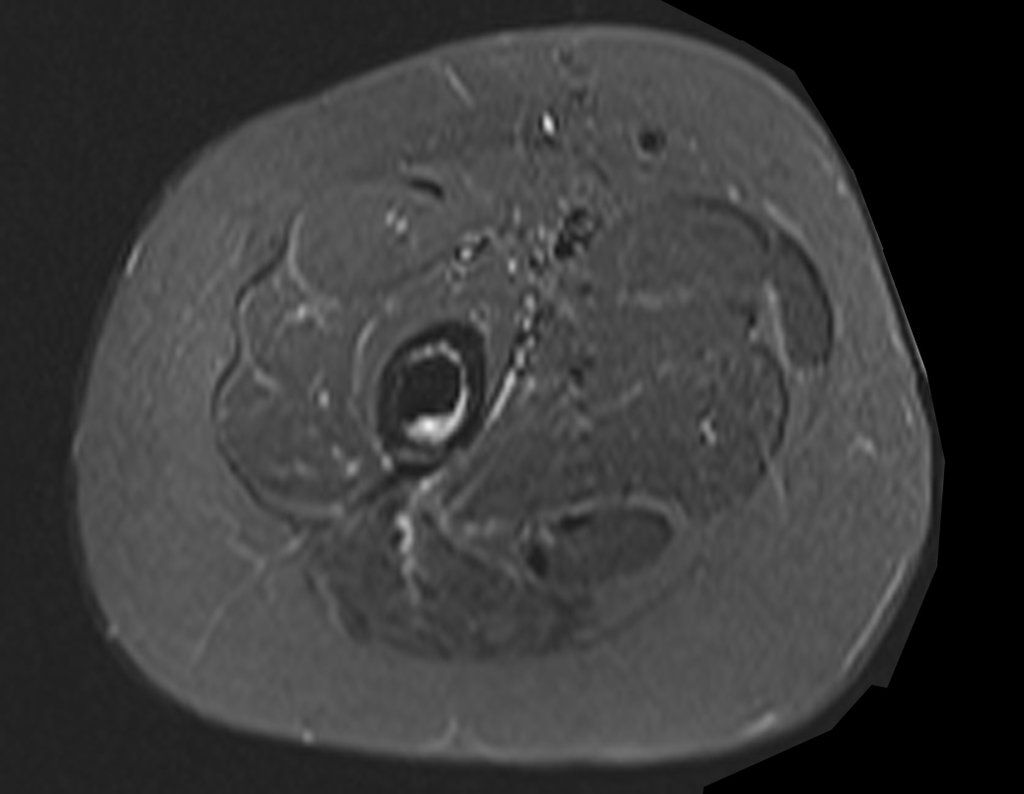
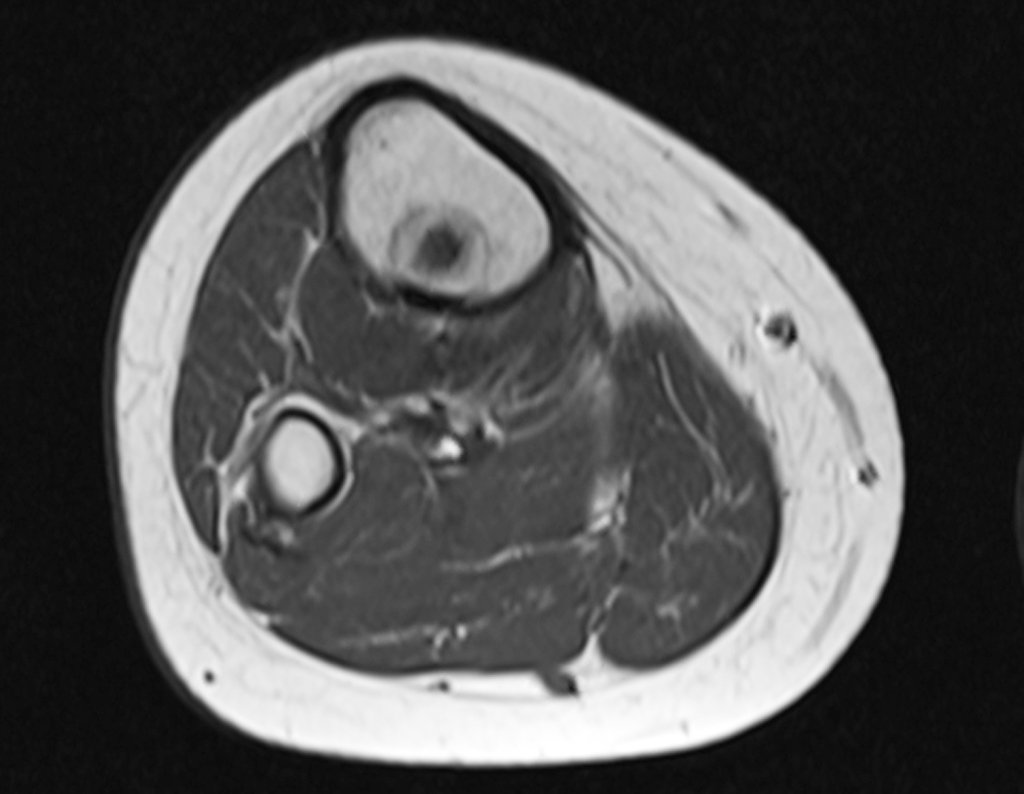
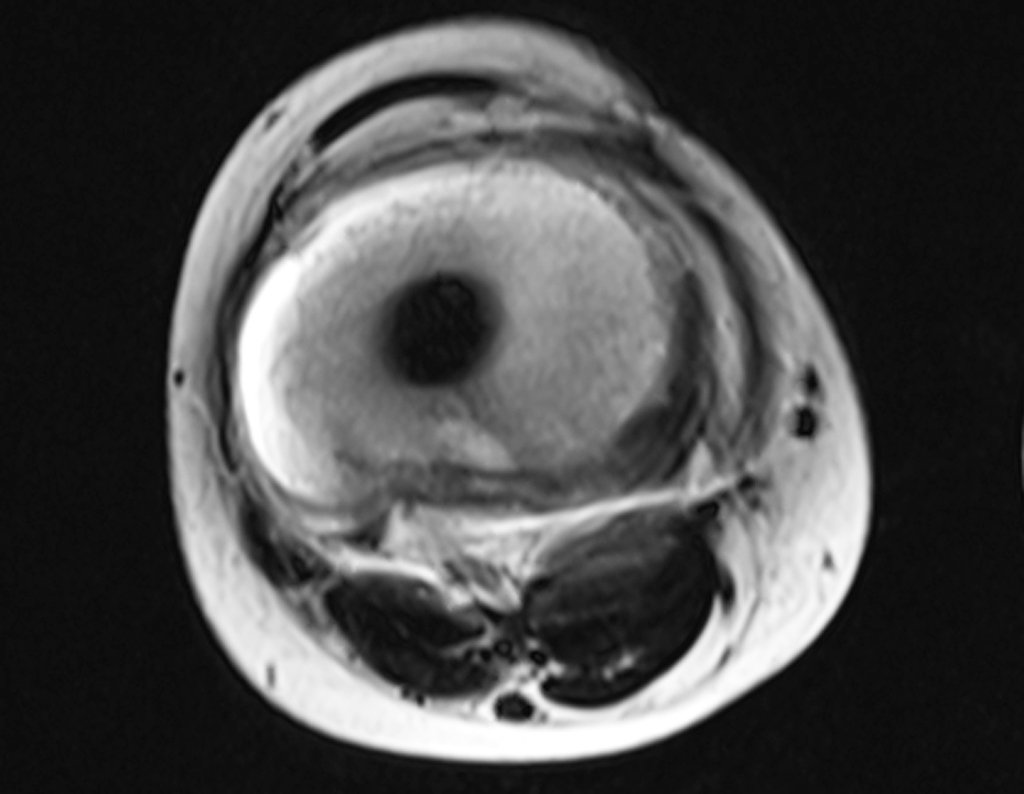
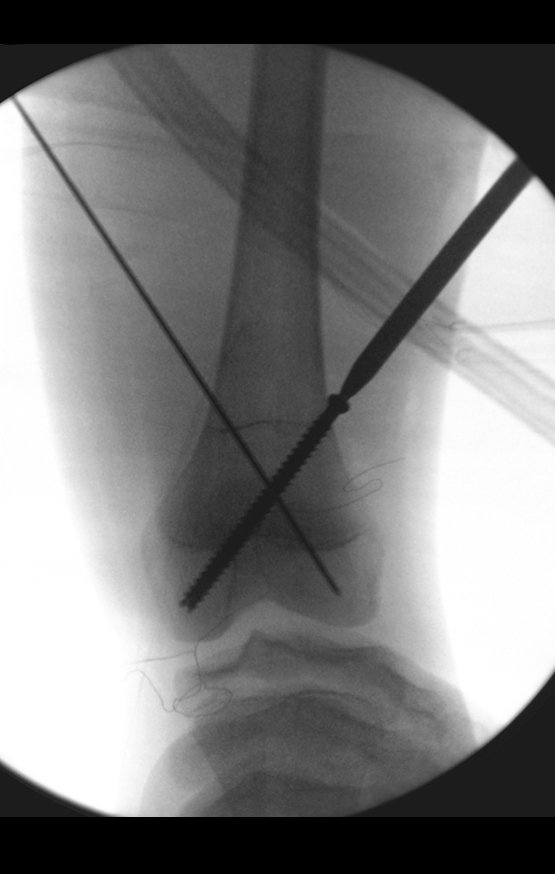
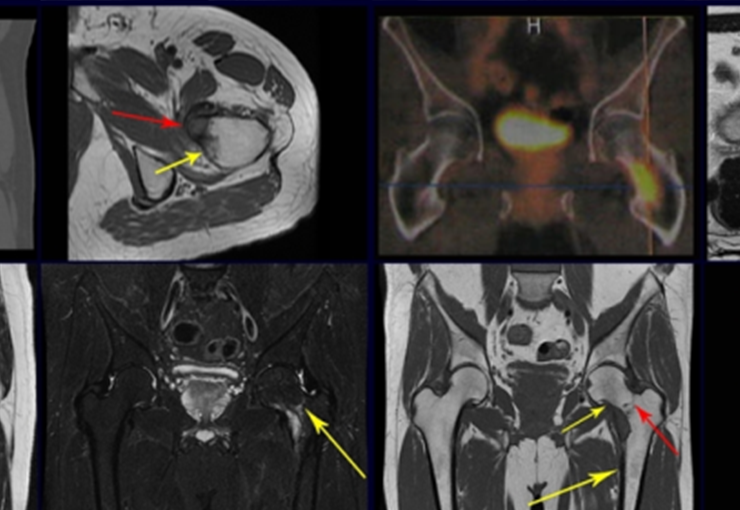
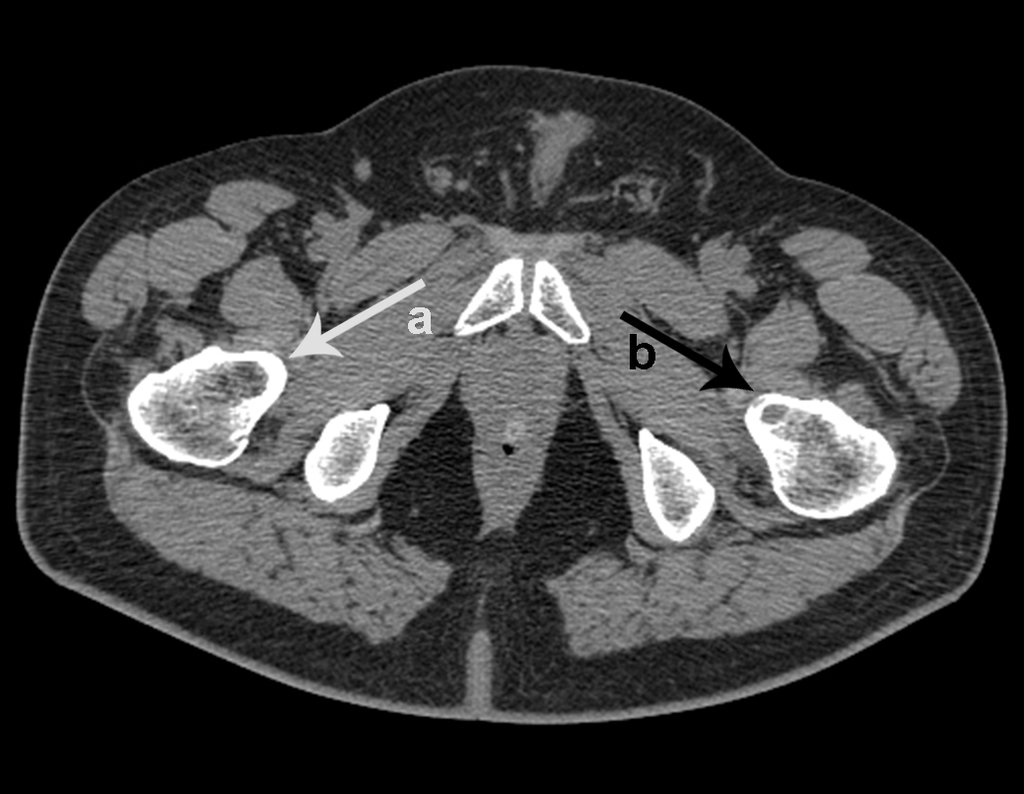
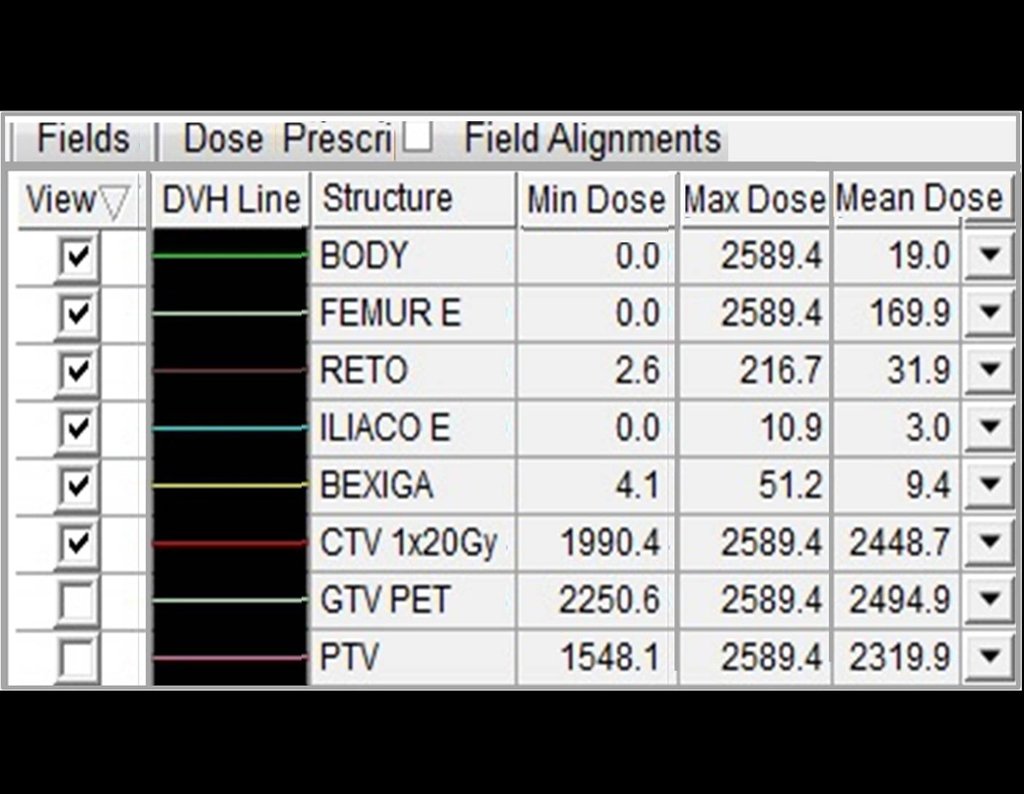
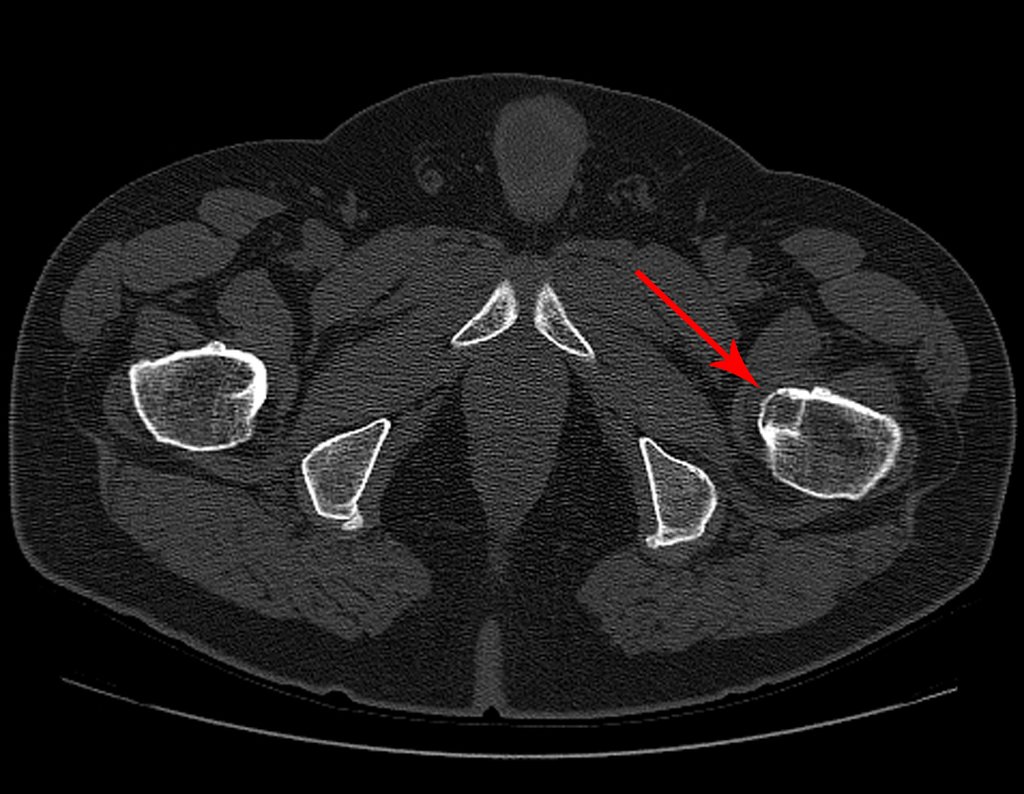
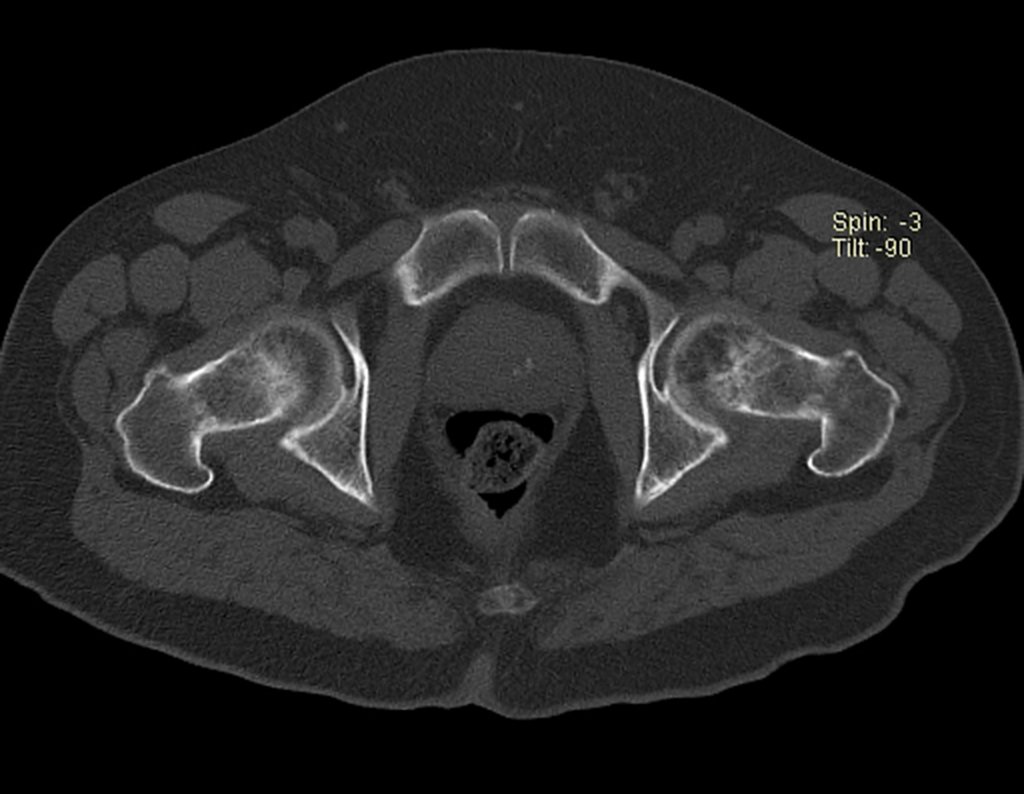
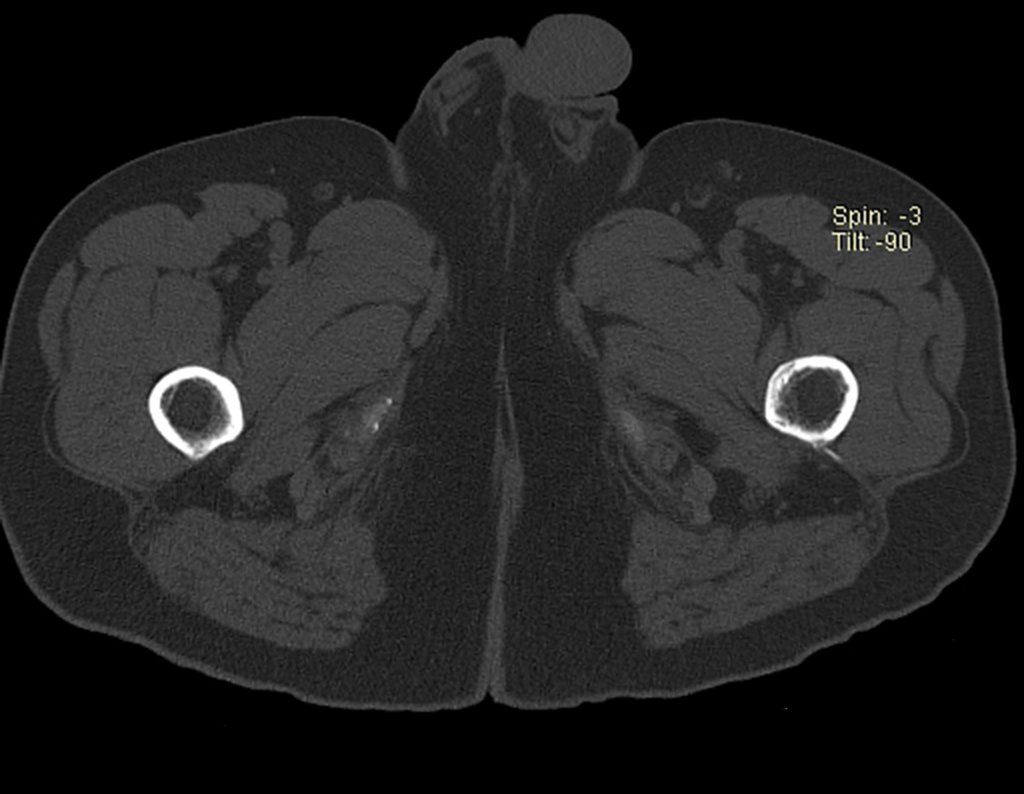
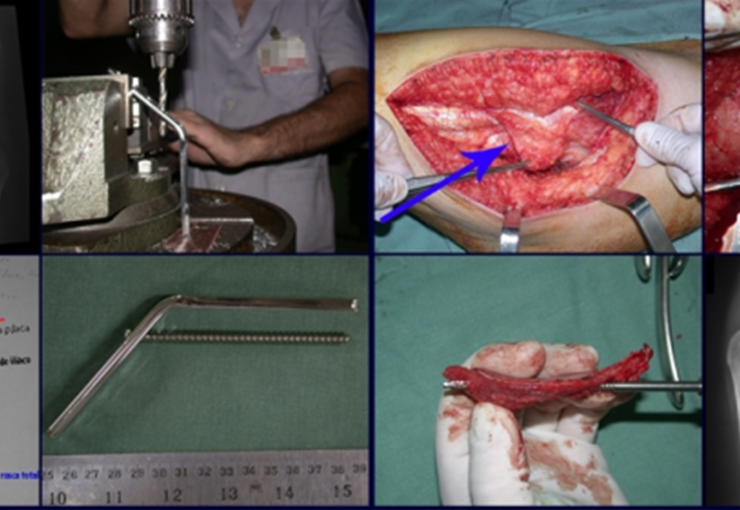
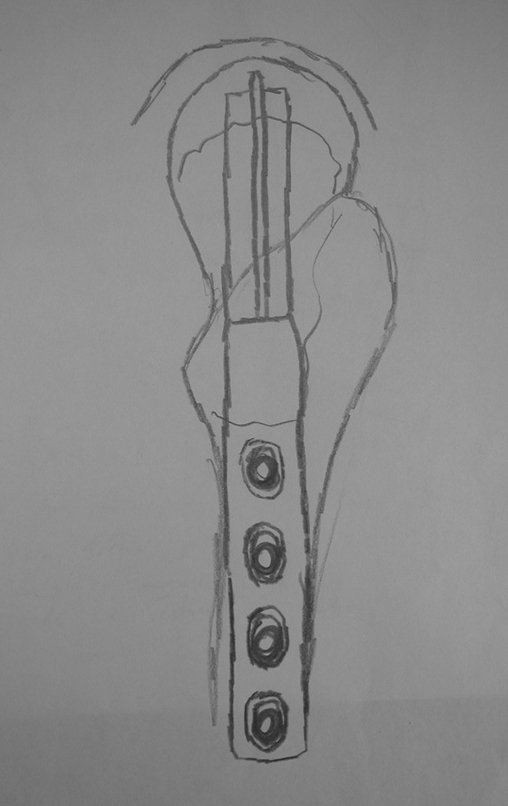
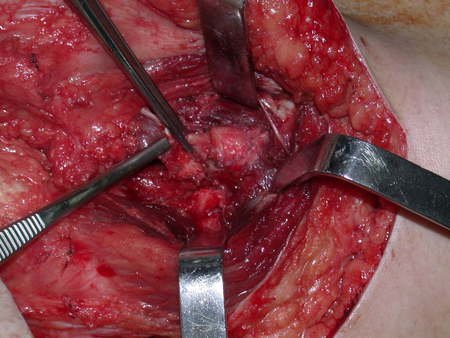
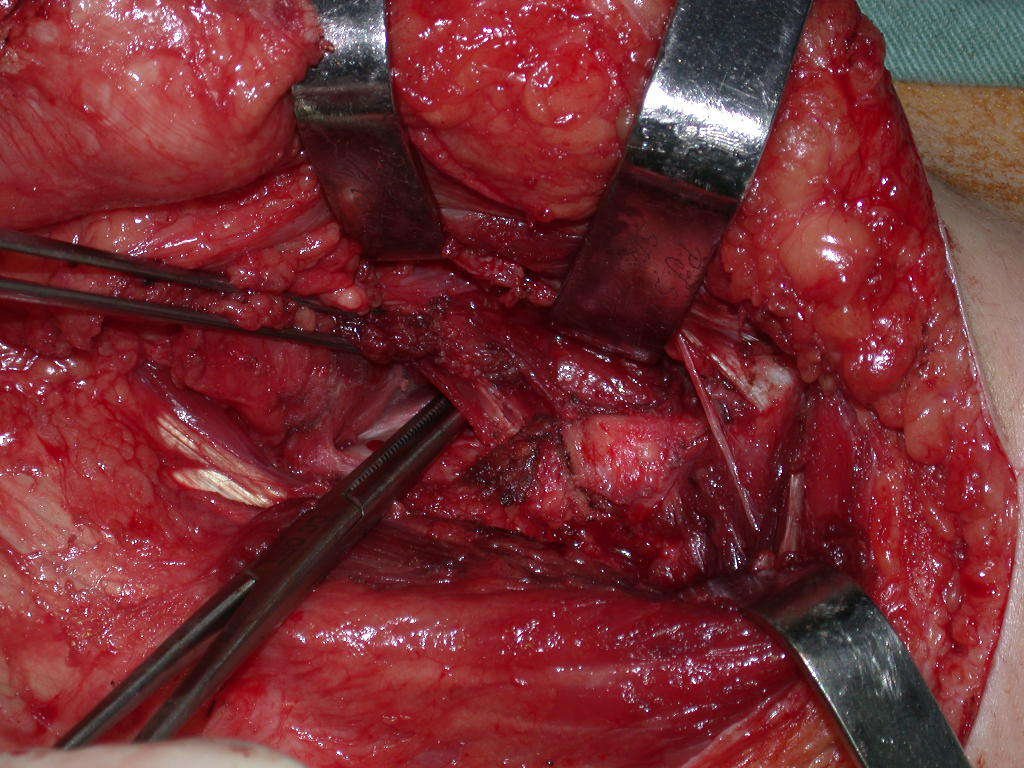
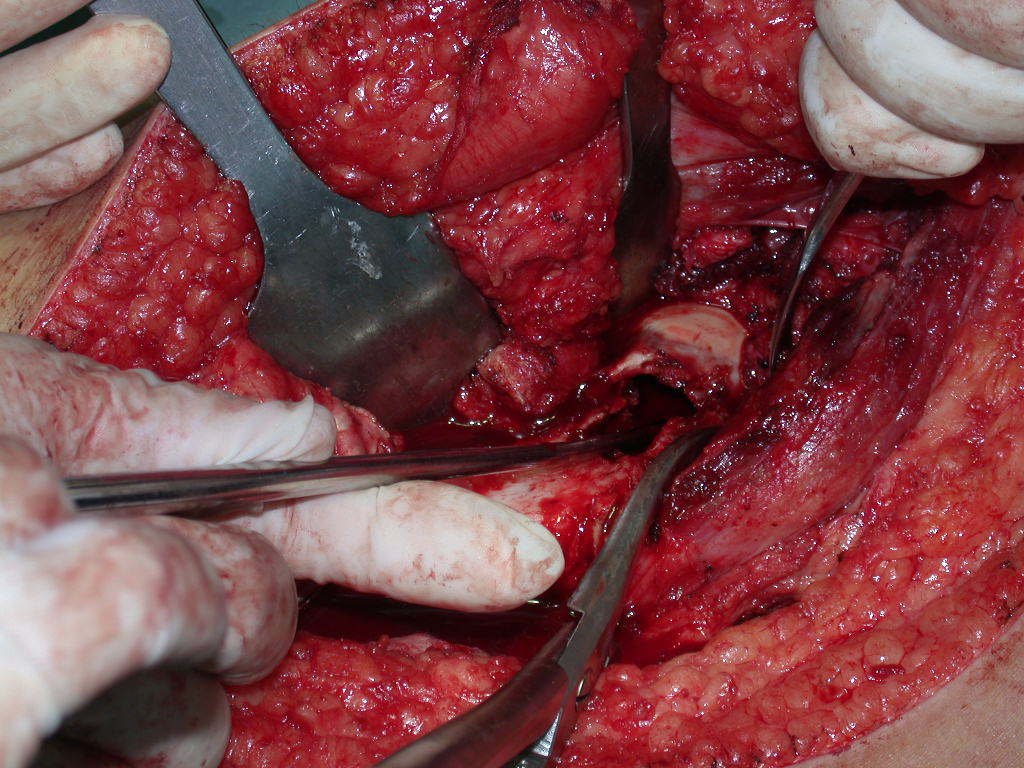
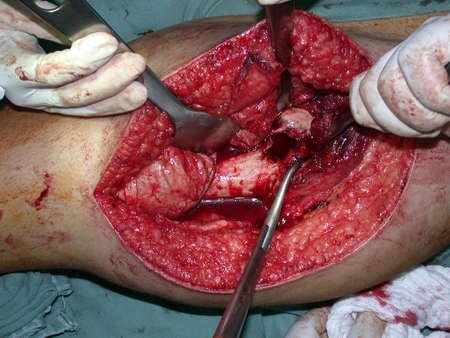
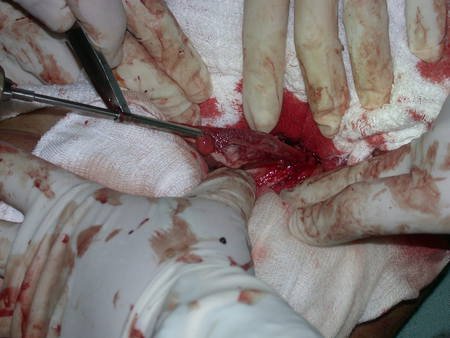
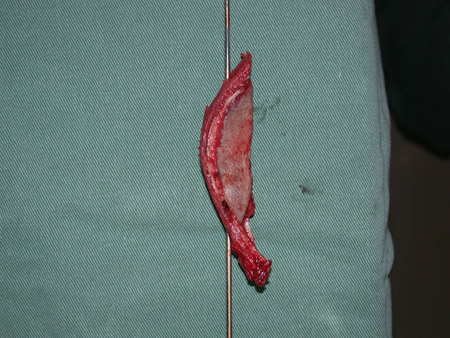
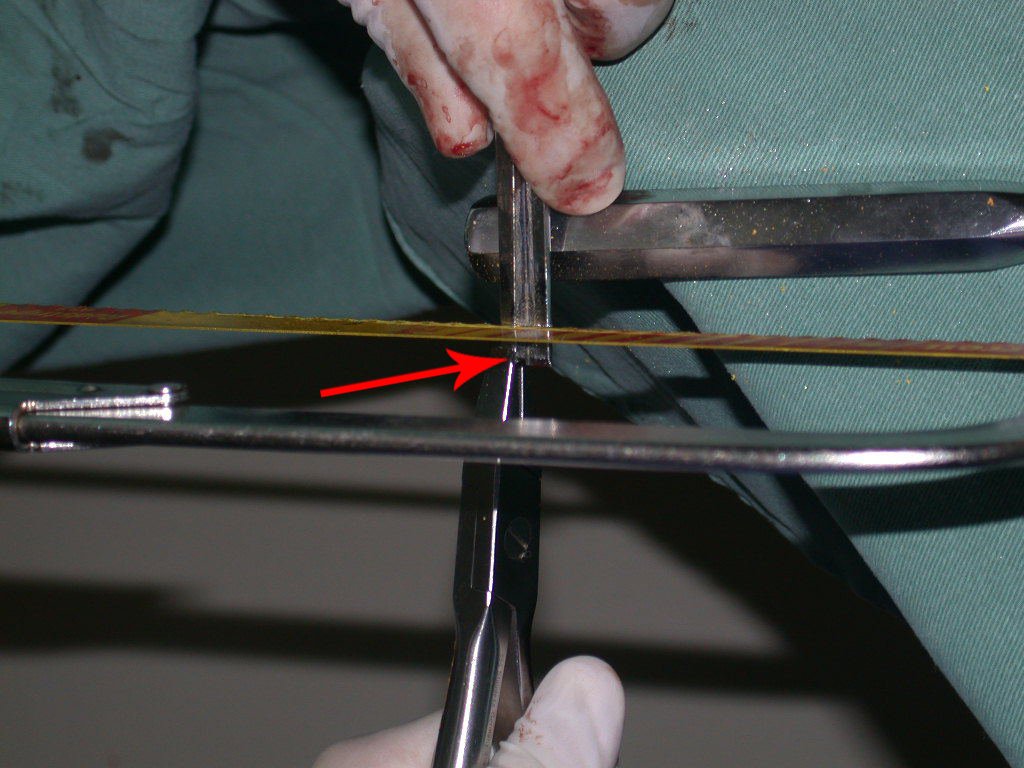
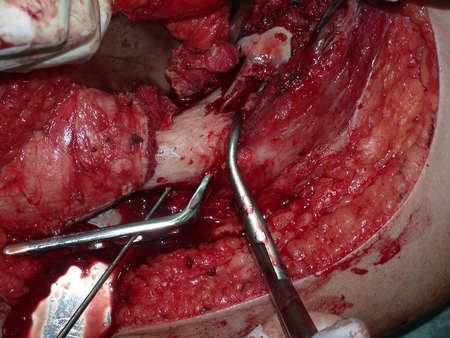
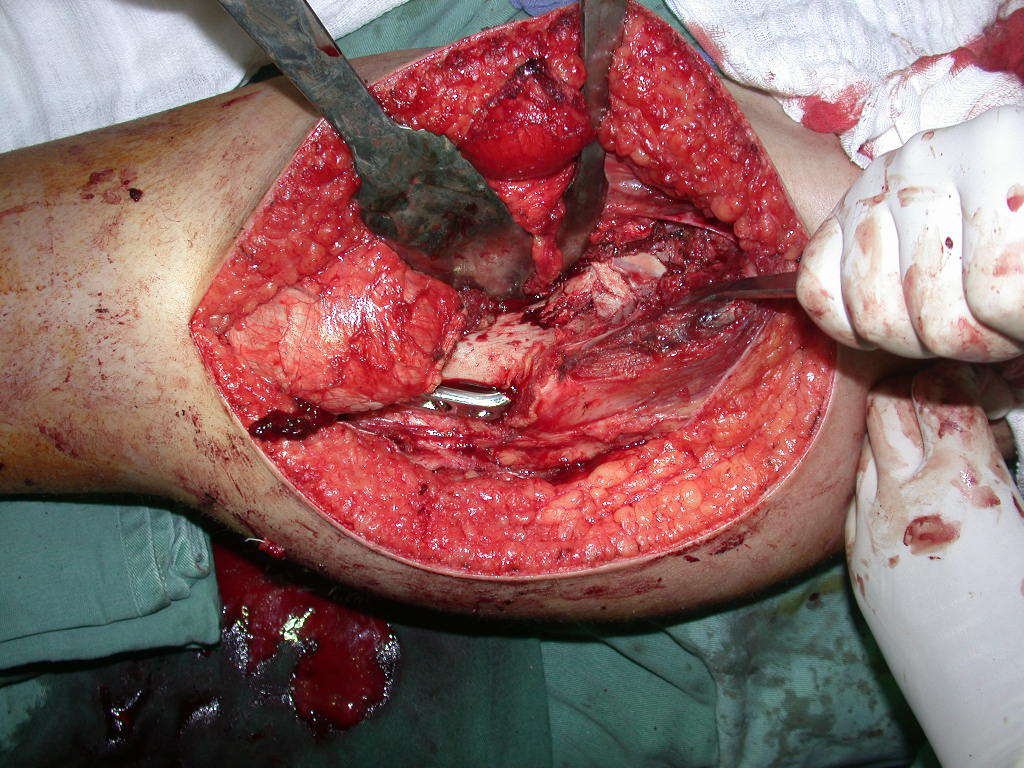
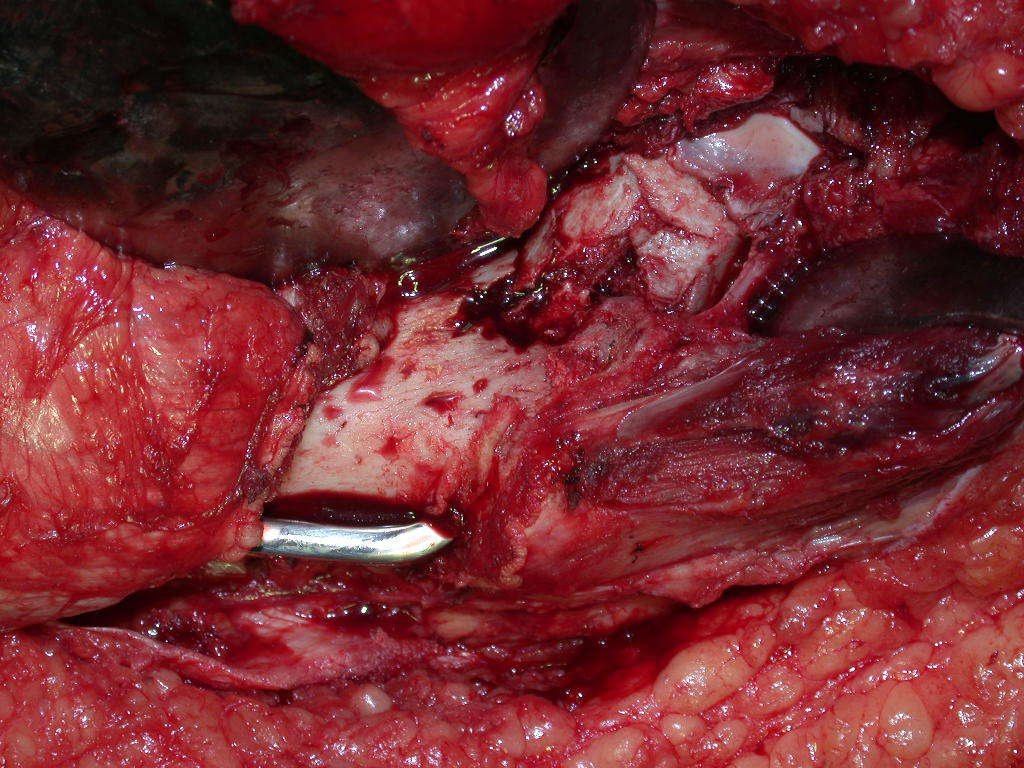
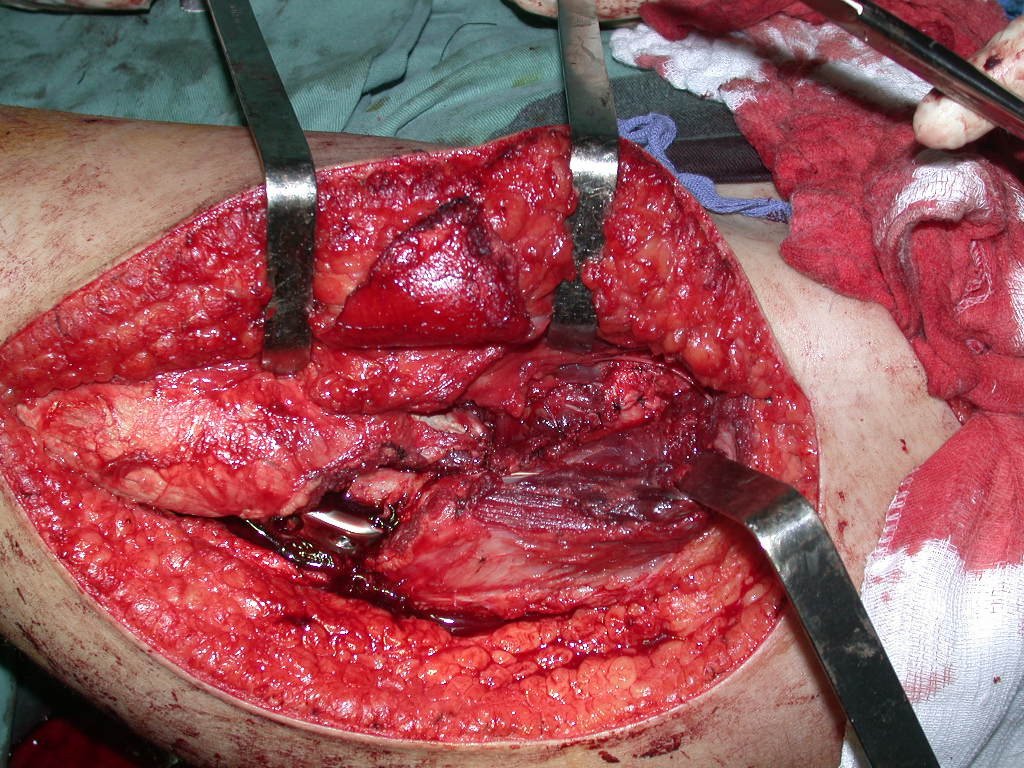
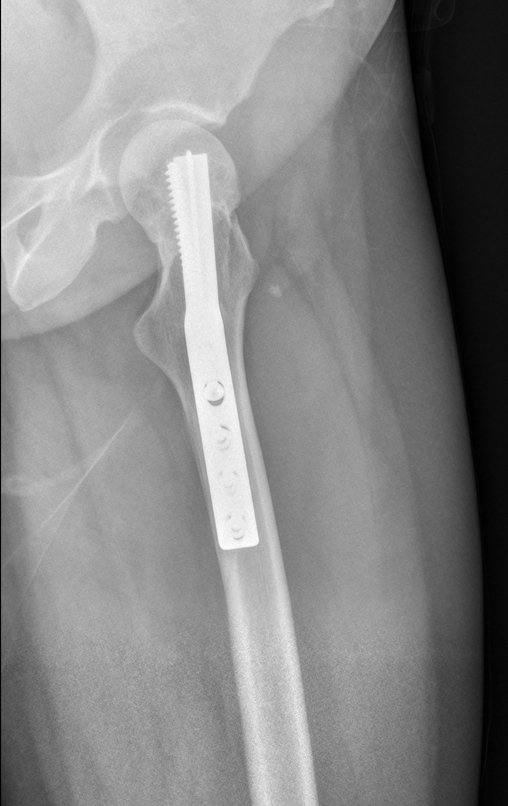
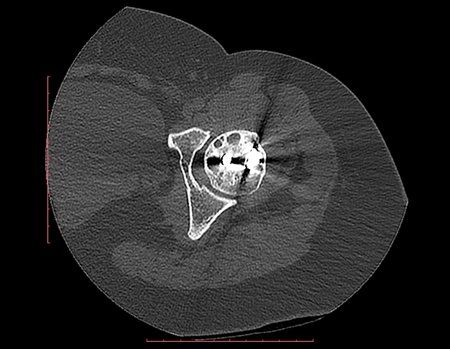
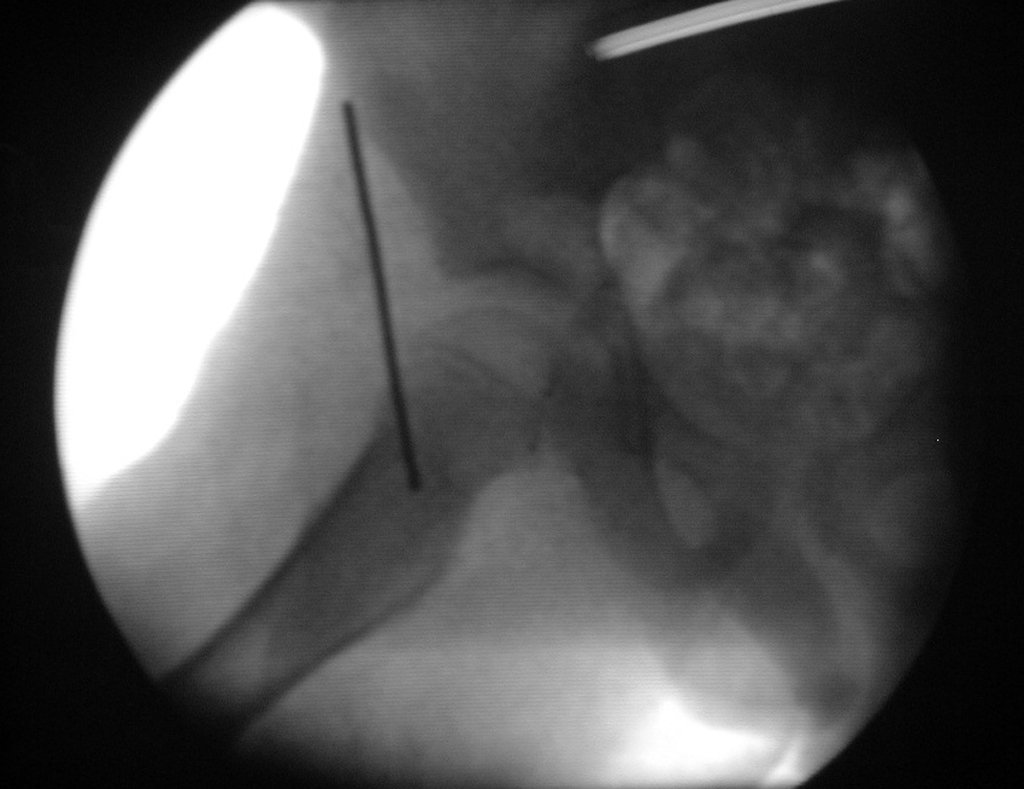
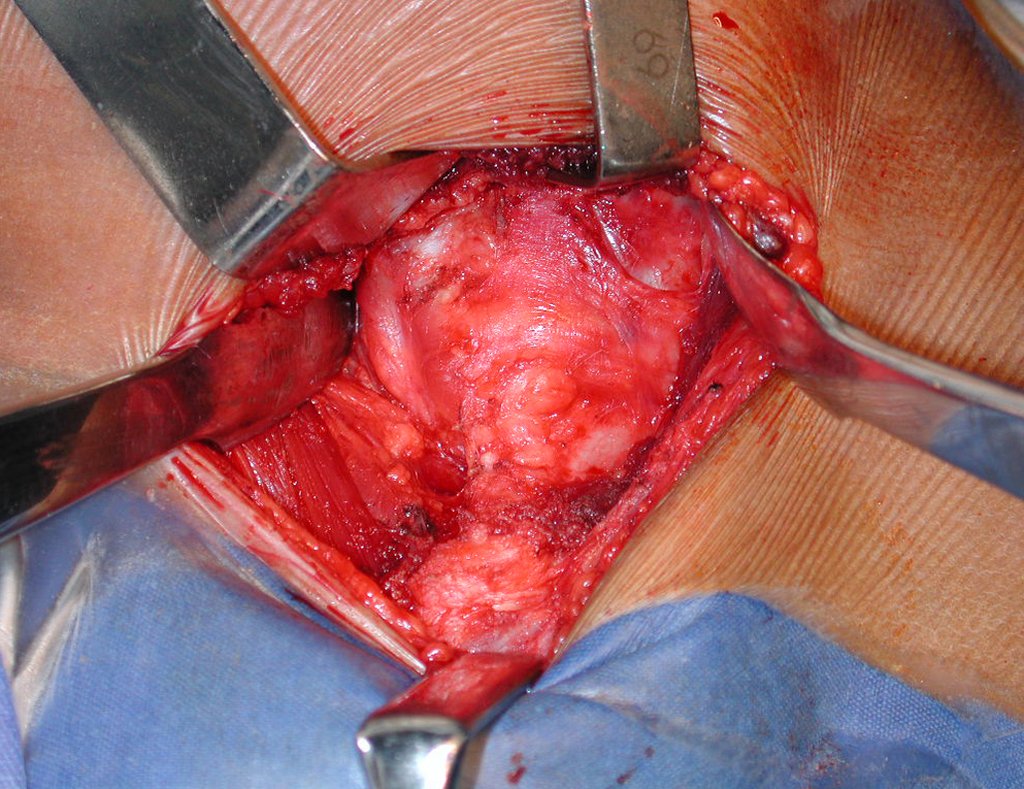
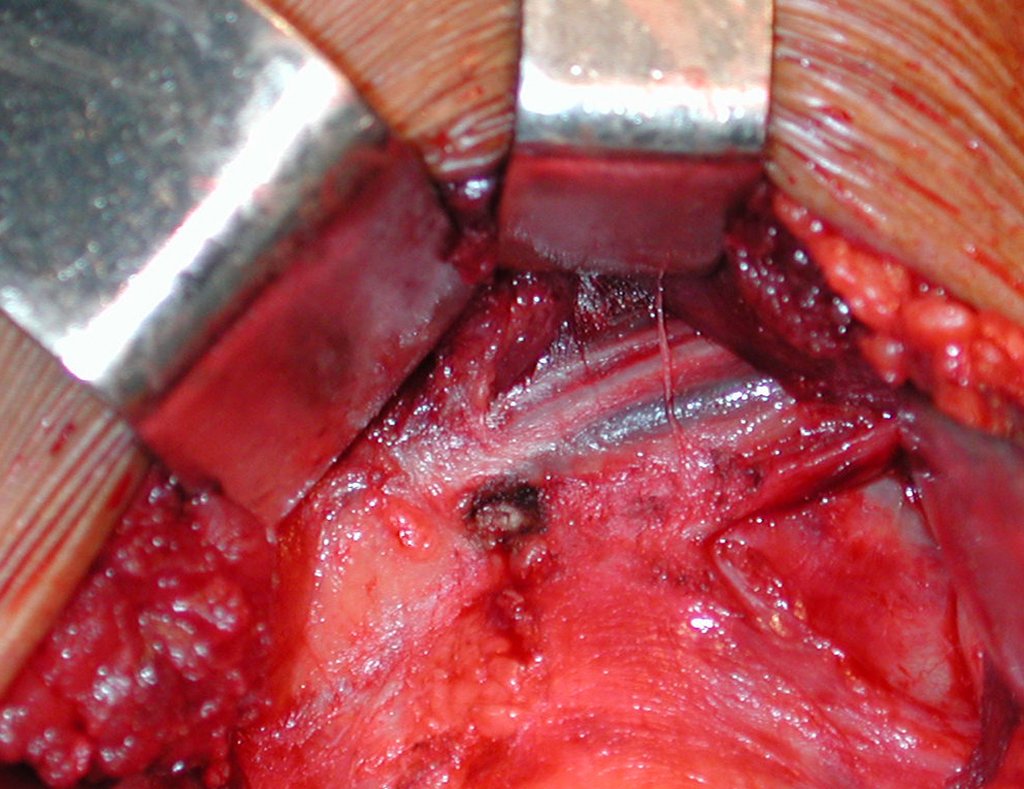
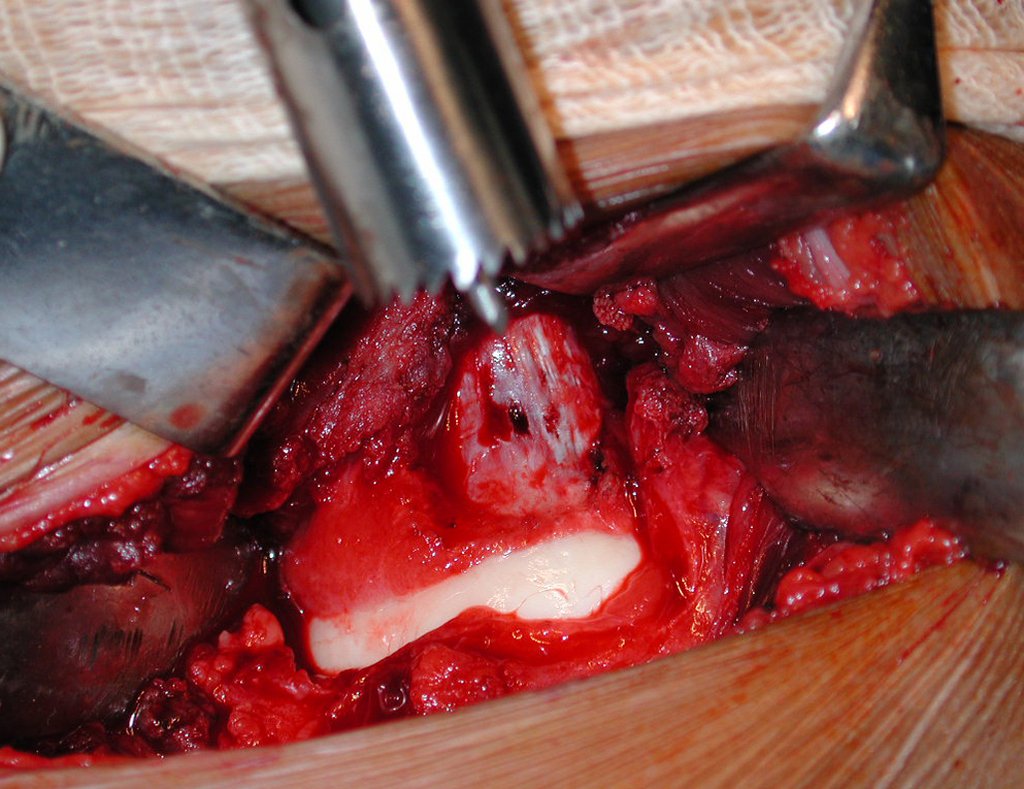
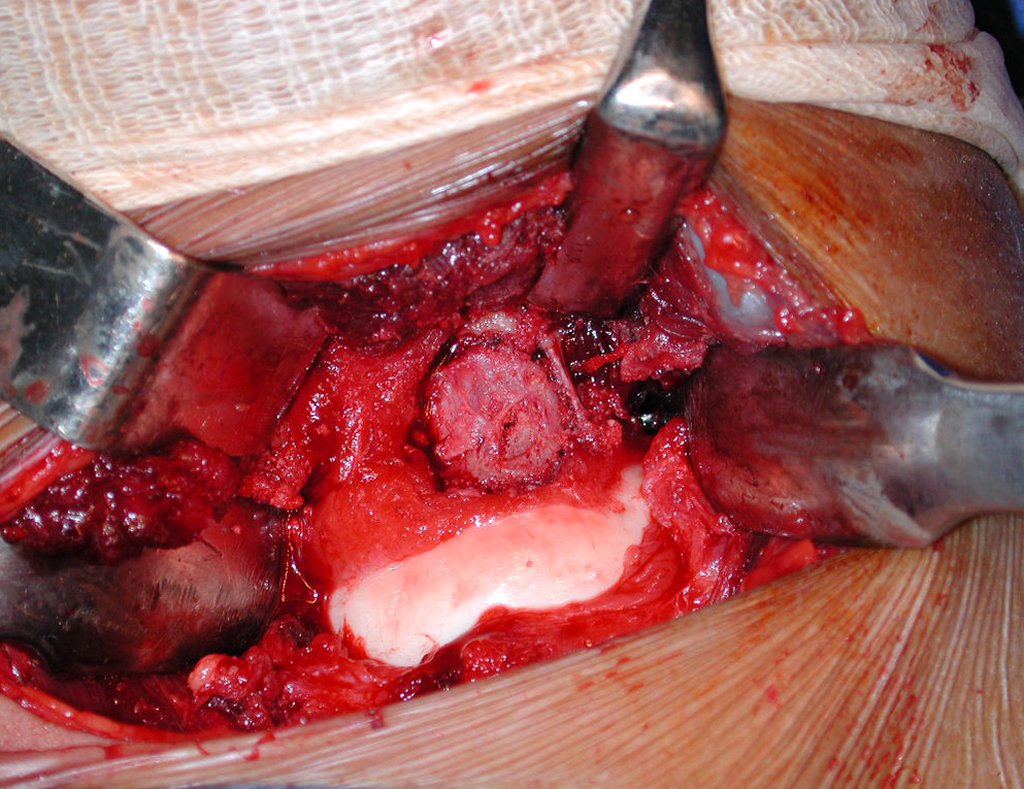
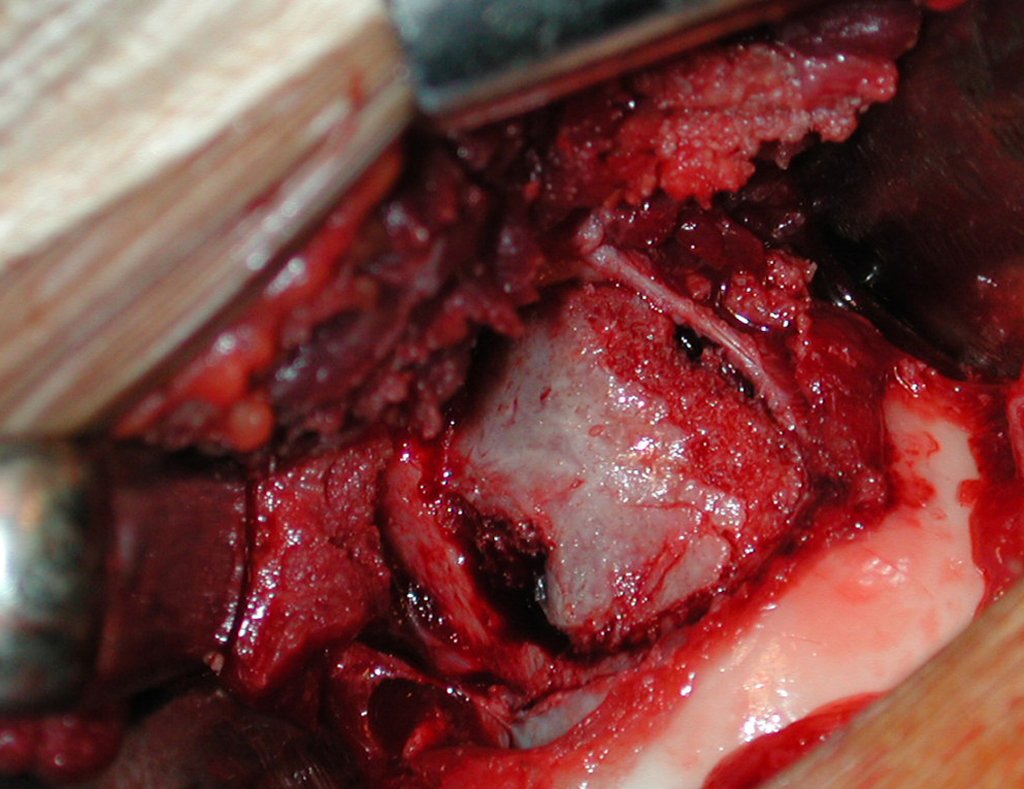
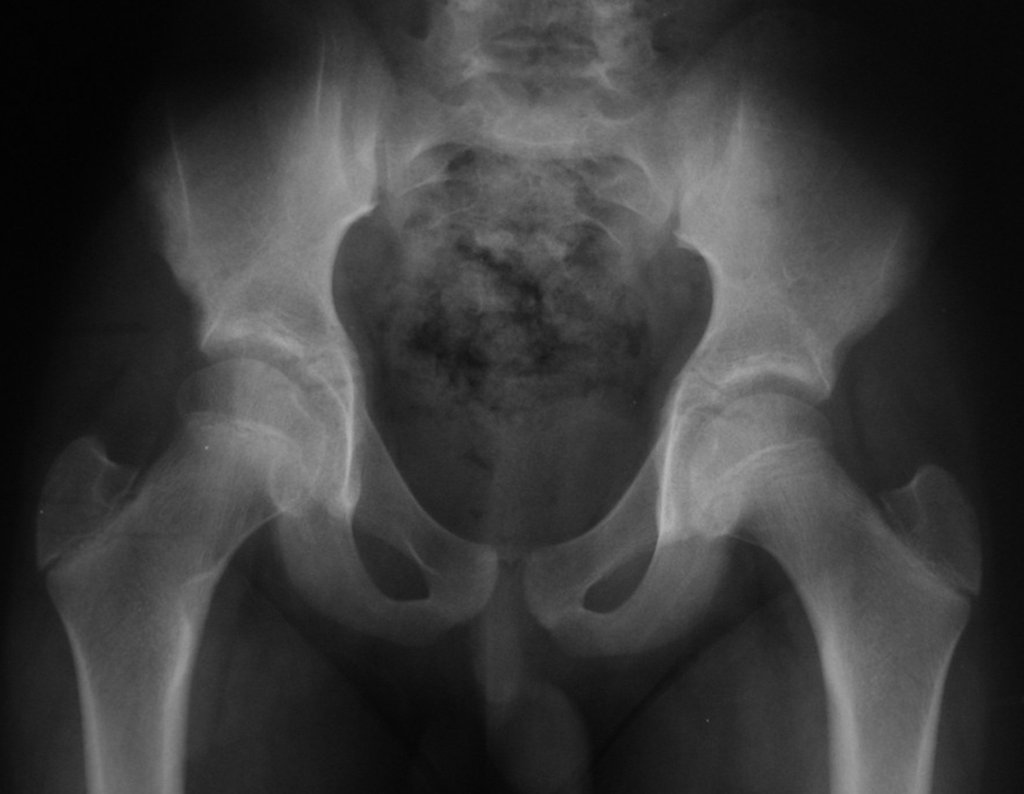
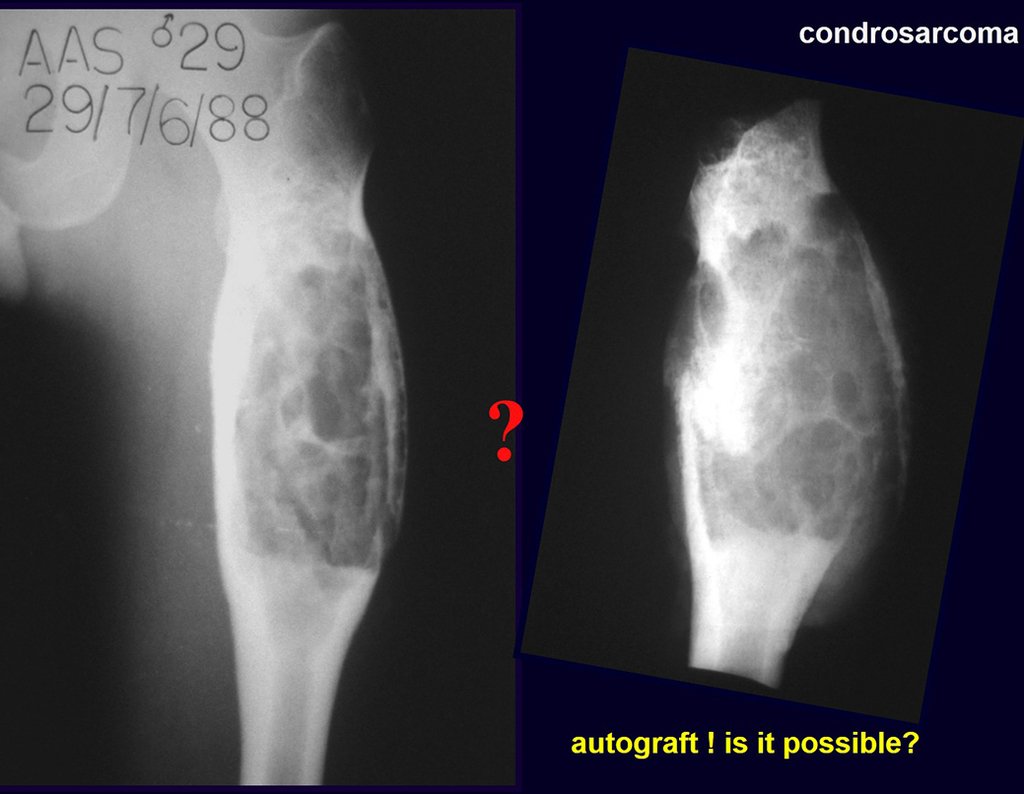
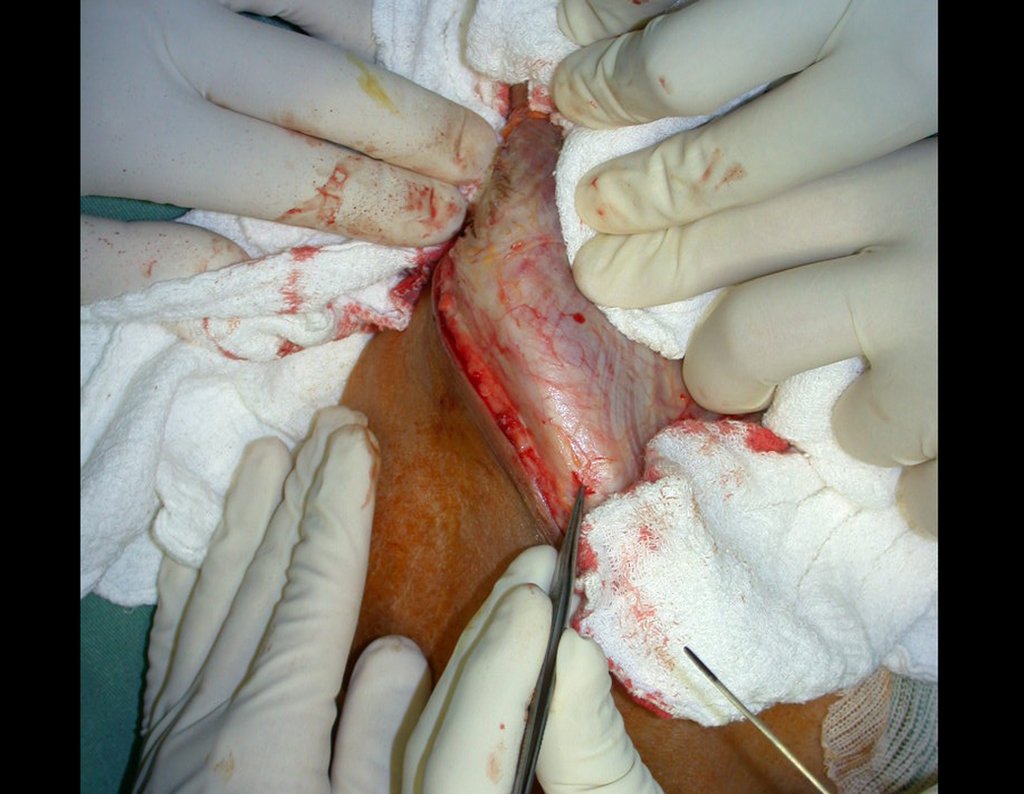
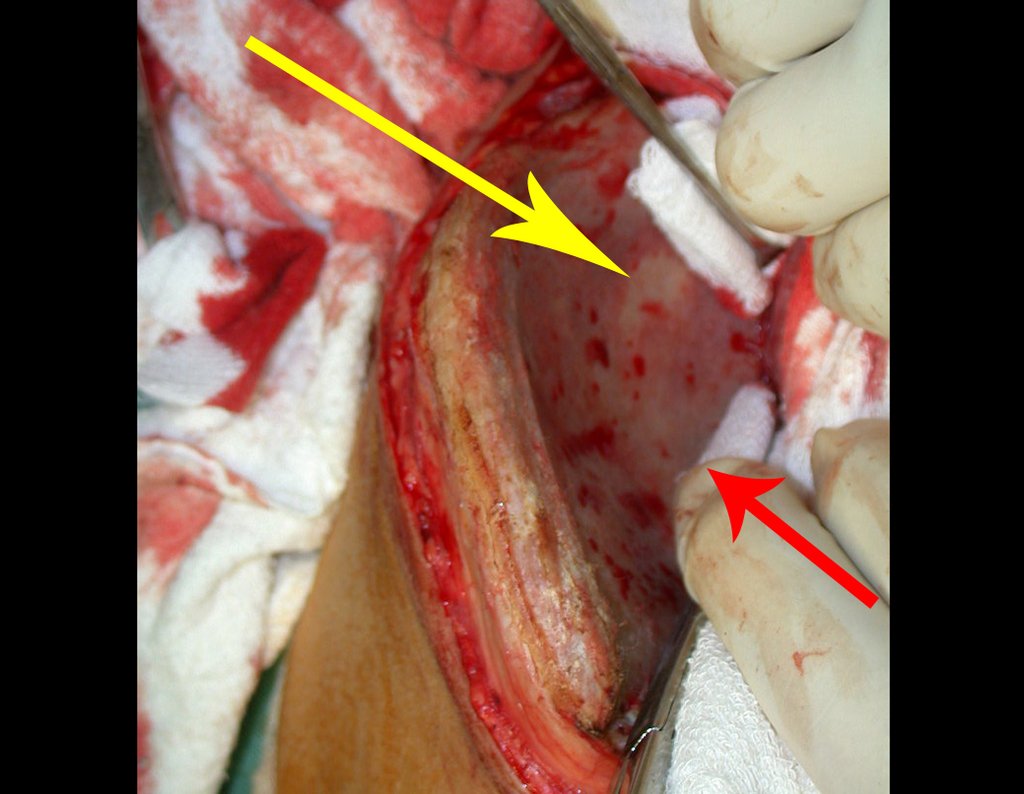
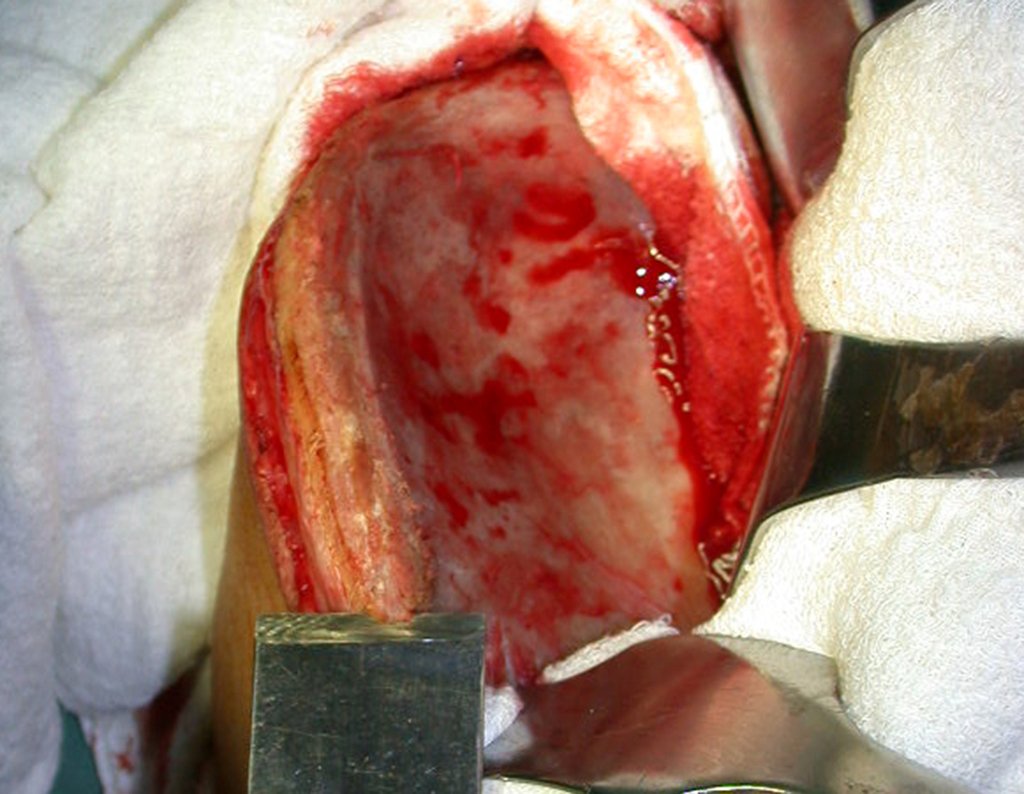
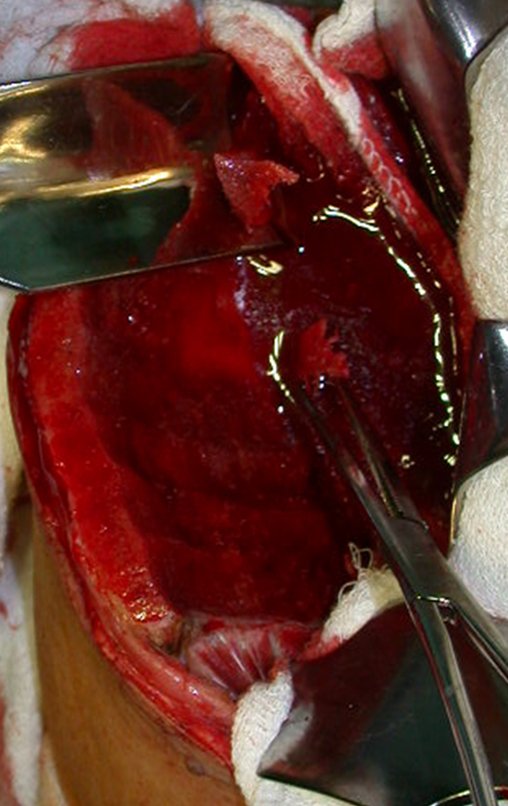
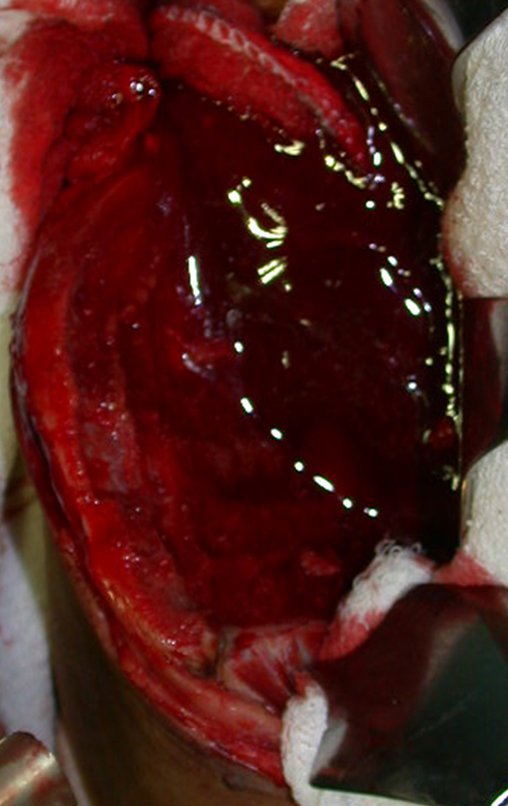
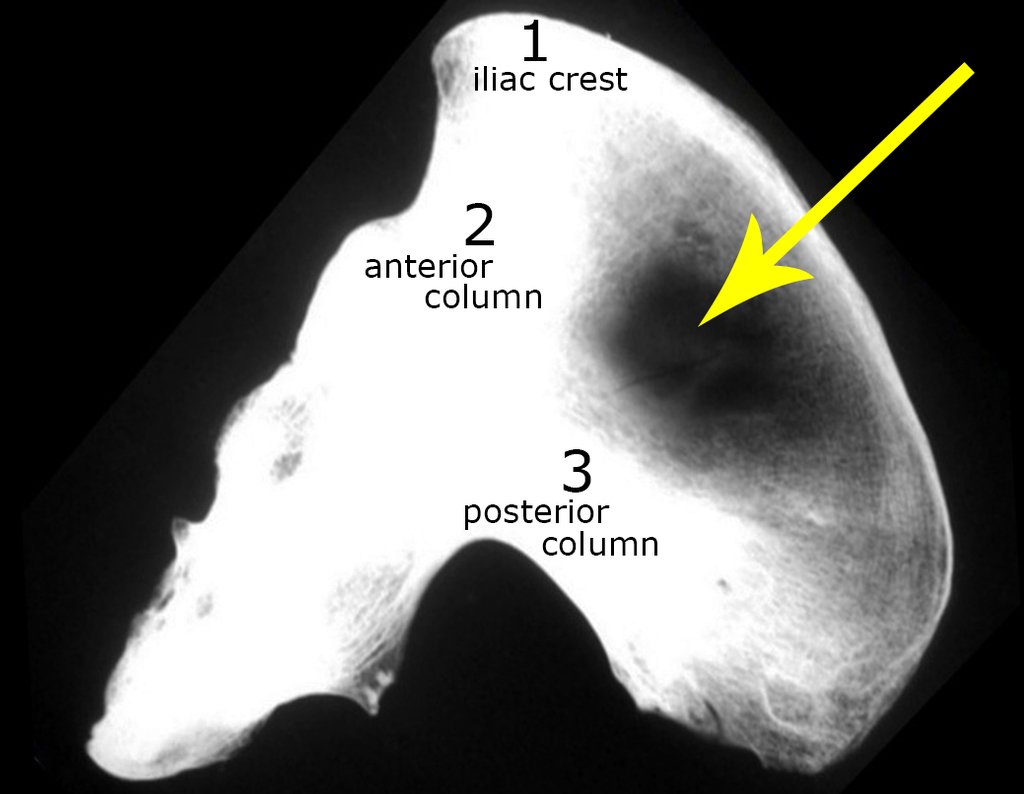
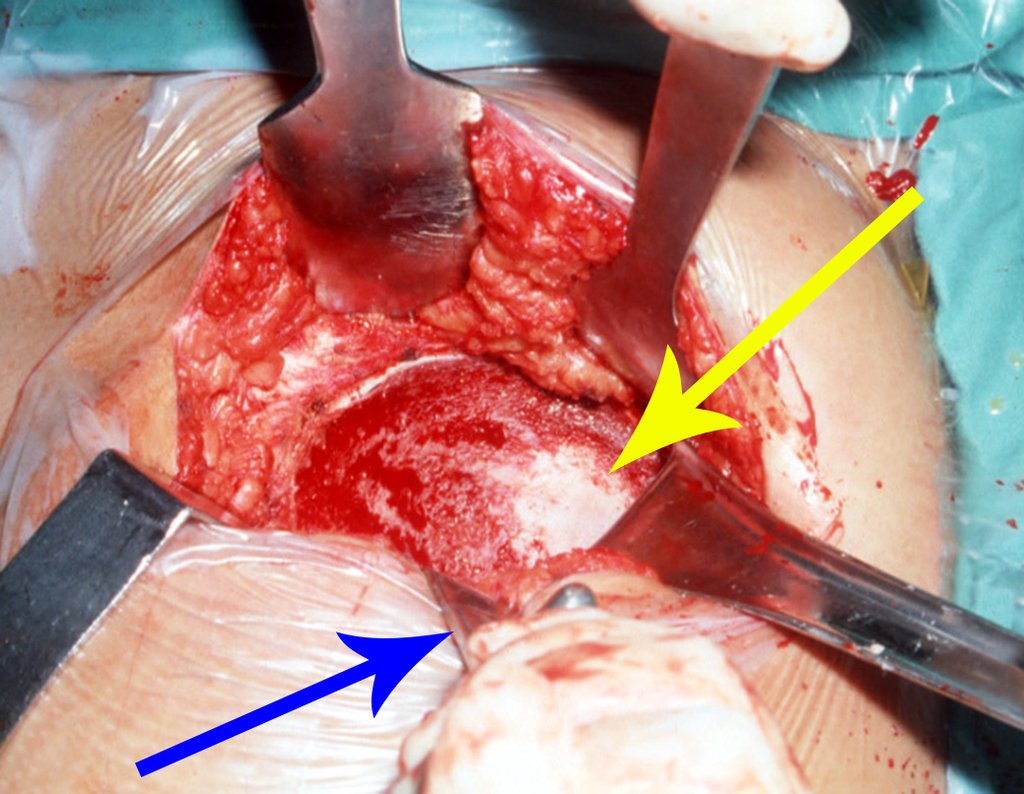
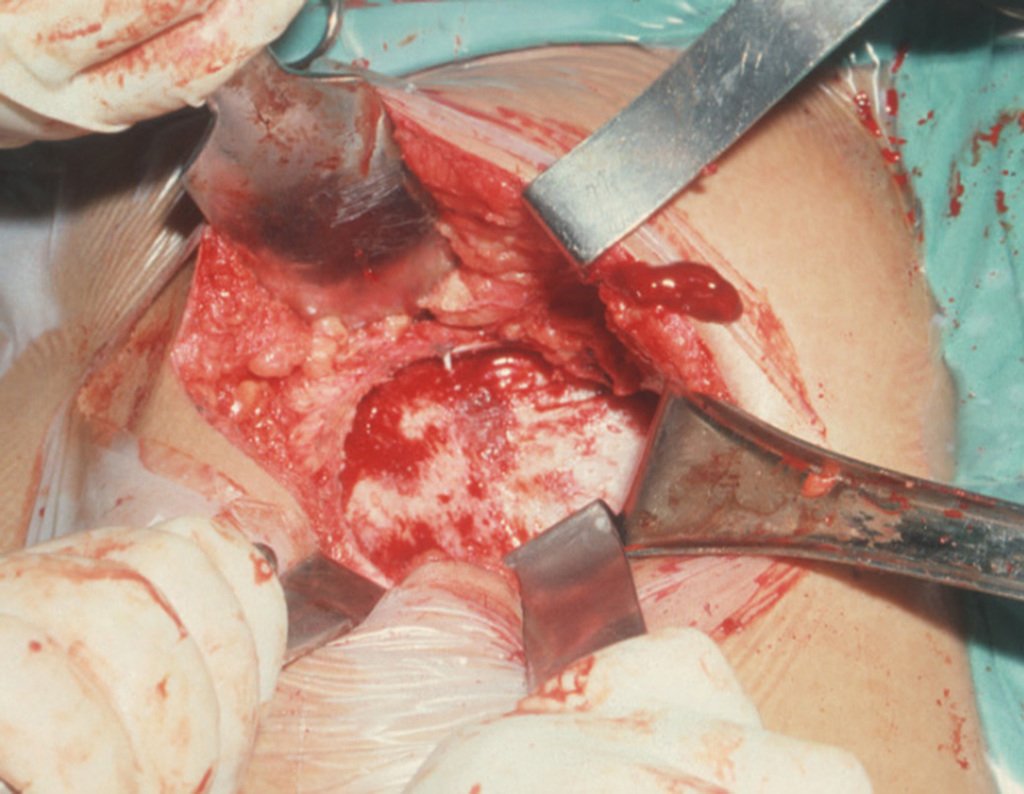
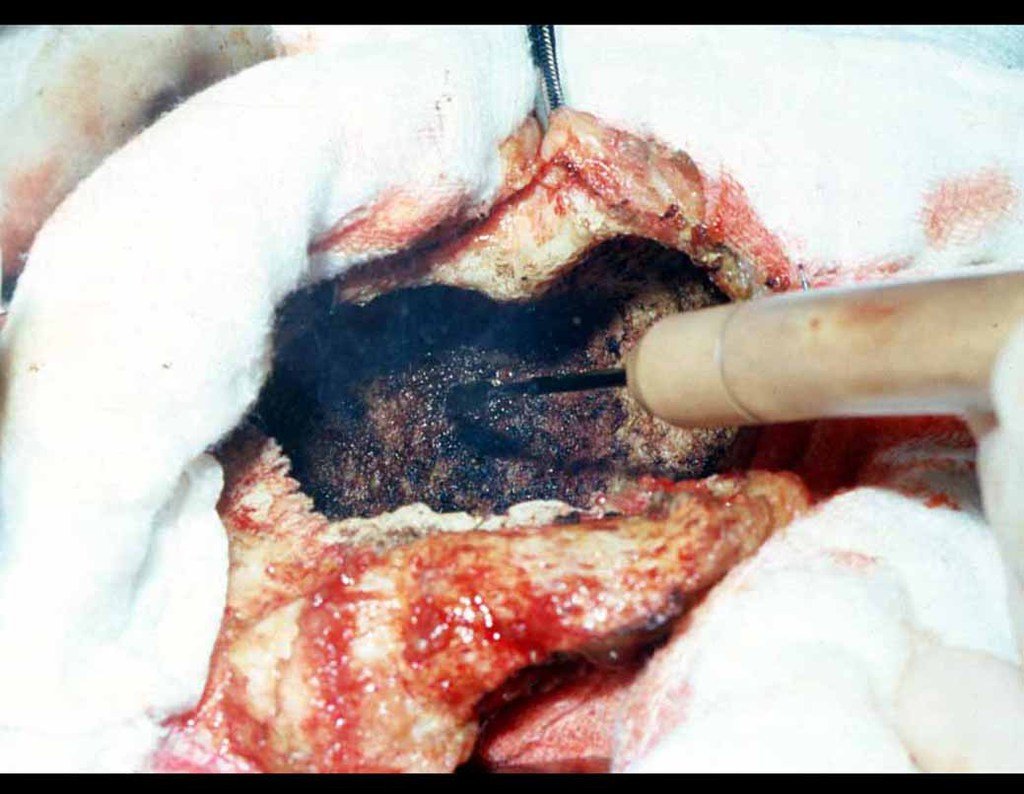
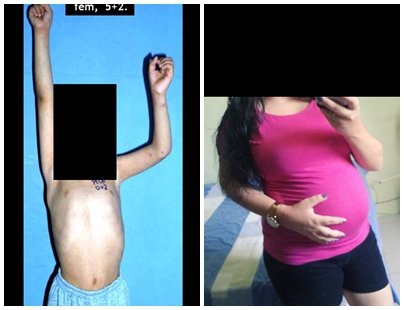
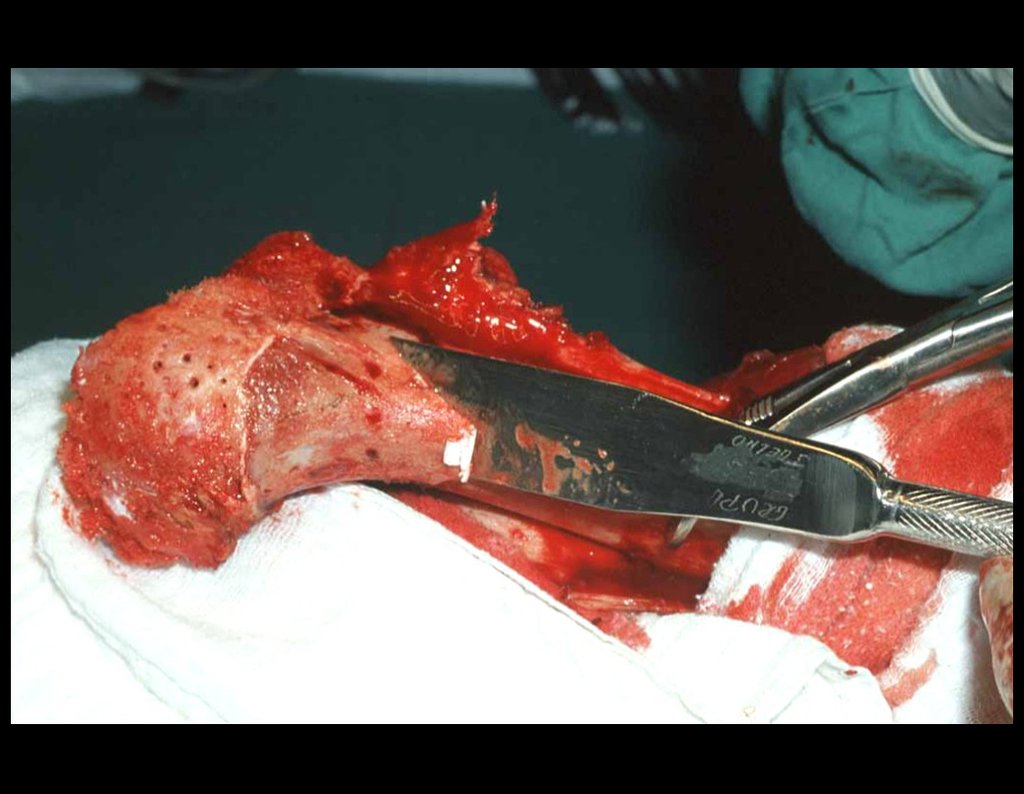
Entretanto, este “fenômeno” do cisto ósseo aneurismático pode aparecer acompanhando outras lesões tumorais tais como o osteoblastoma, o condroblastoma, o fibroma condromixóide, o tumor de células gigantes, o osteossarcoma teleangiectásico, a displasia fibrosa e o tumor marrom do hiperparatireoidismo, além de lesões metastáticas secundarias à neoplasia da tireóide ou rim. Estes tumores com sua histologia característica podem apresentar áreas isoladas do cisto ósseo aneurismático clássico. Desta forma, pequenos fragmentos de biópsia podem dificultar o diagnóstico preciso (fig 3).
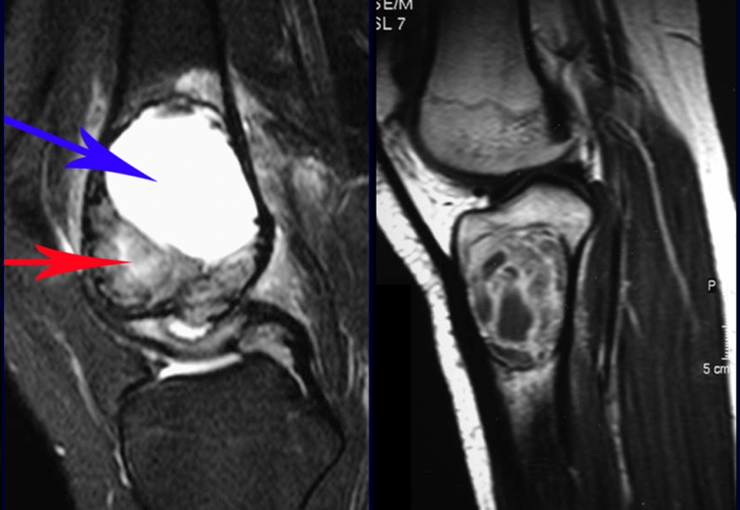
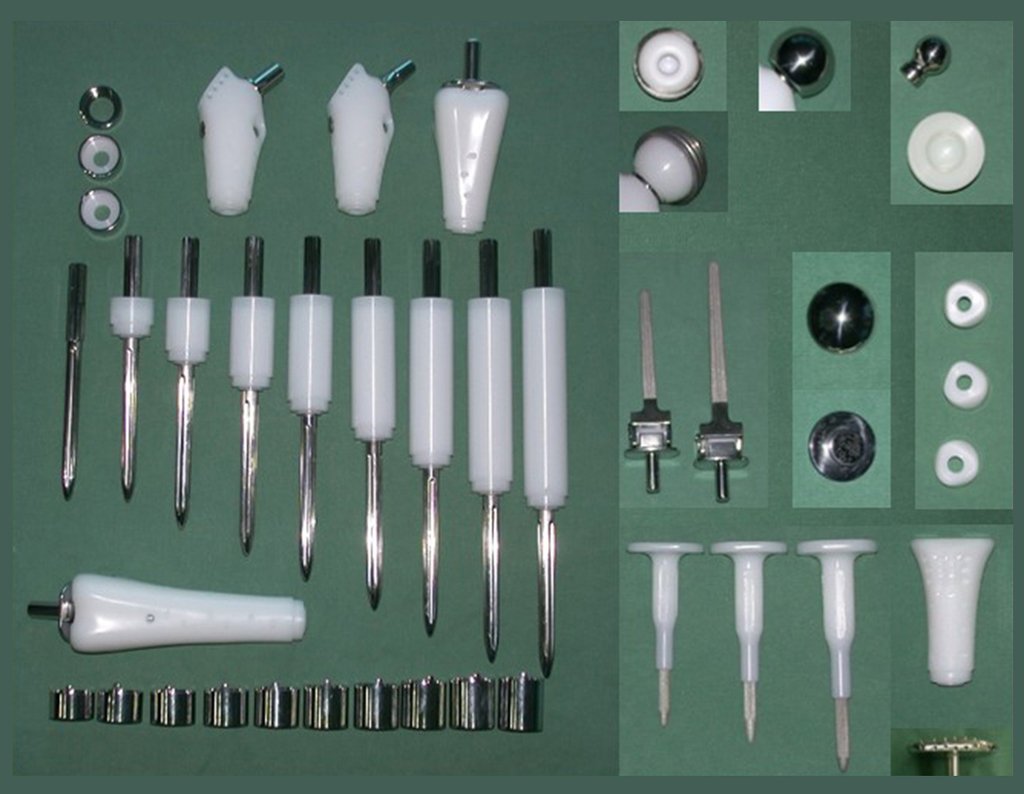
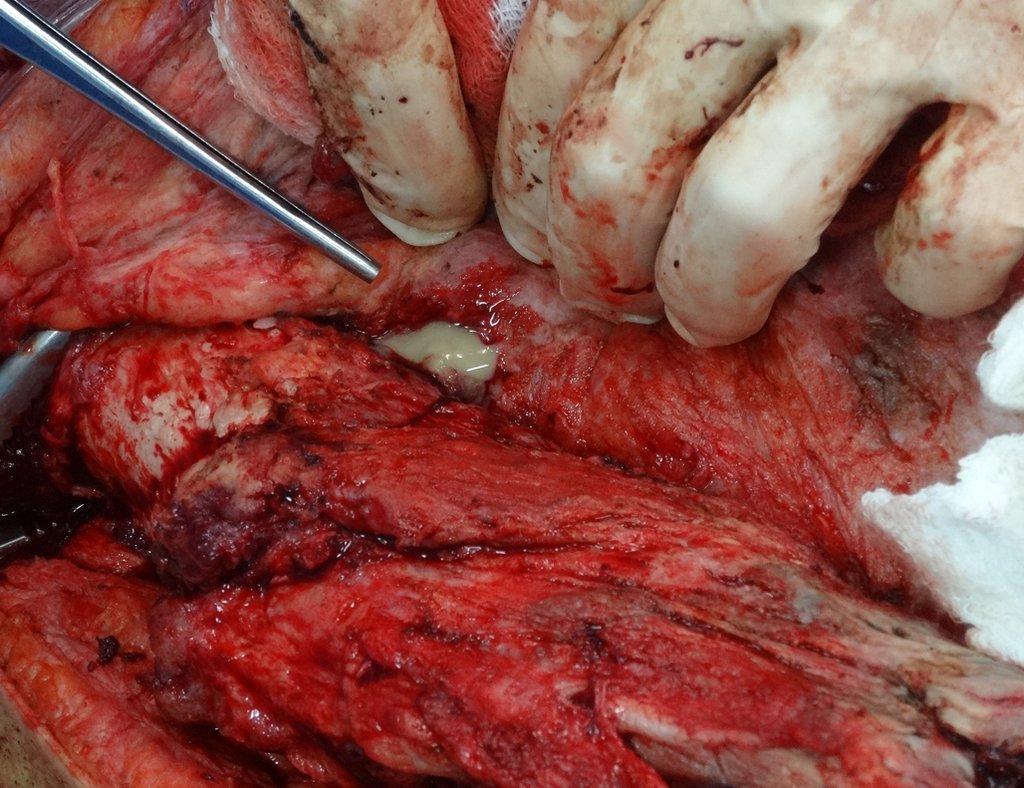
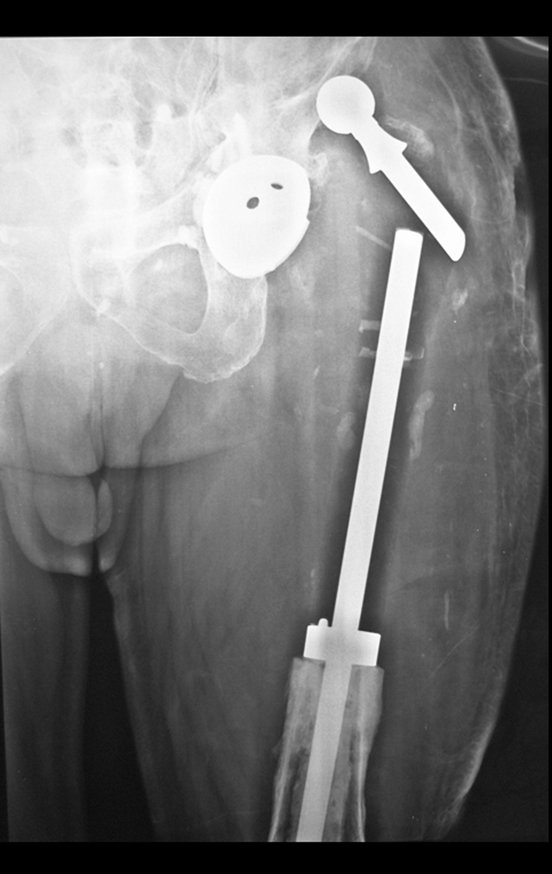
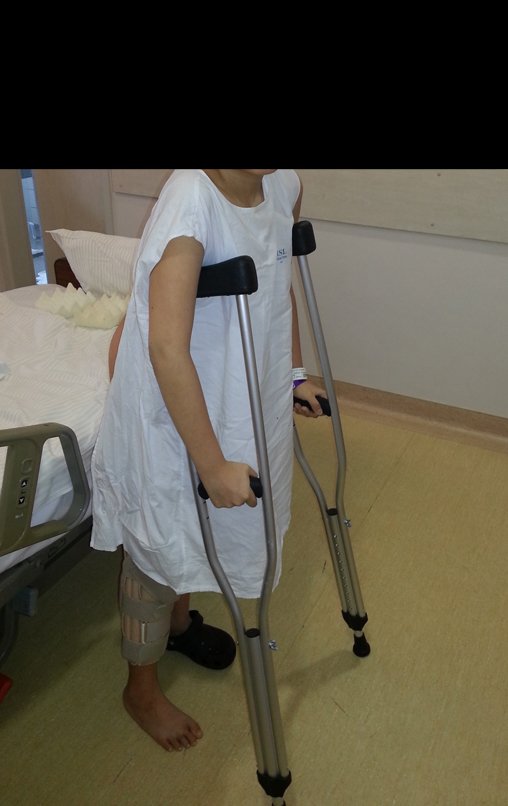
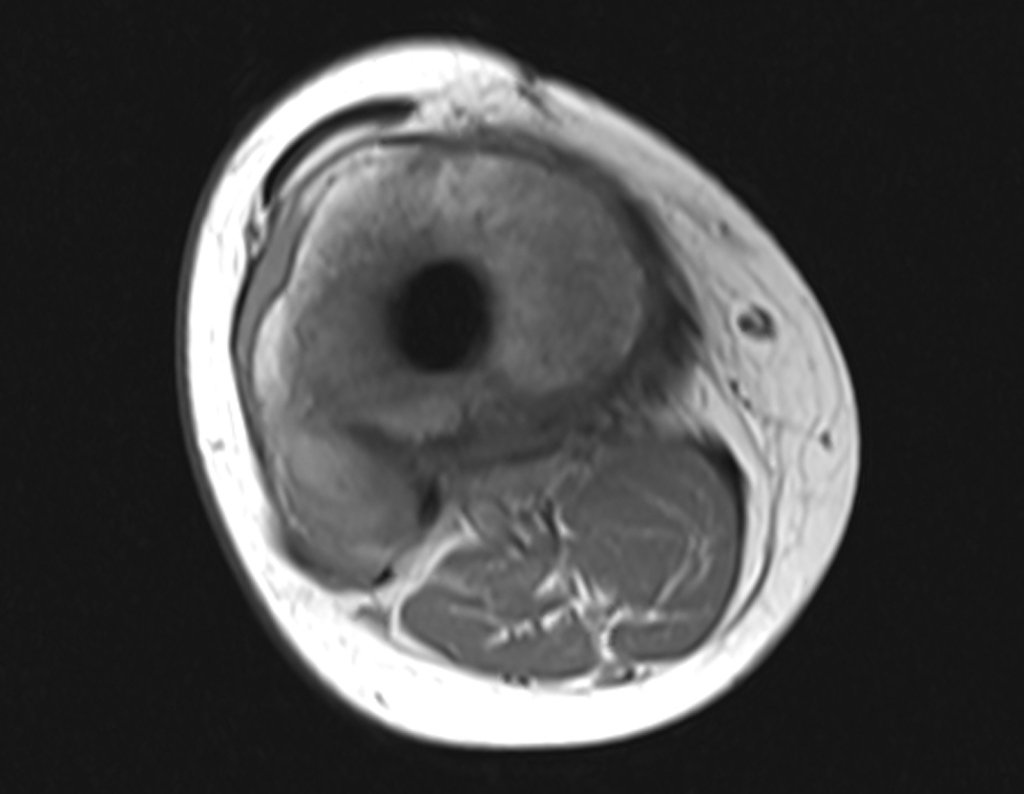
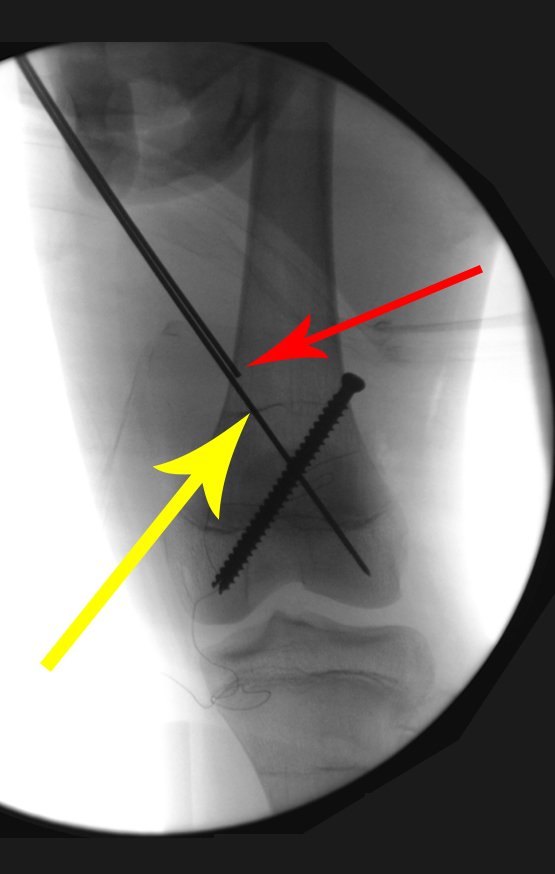
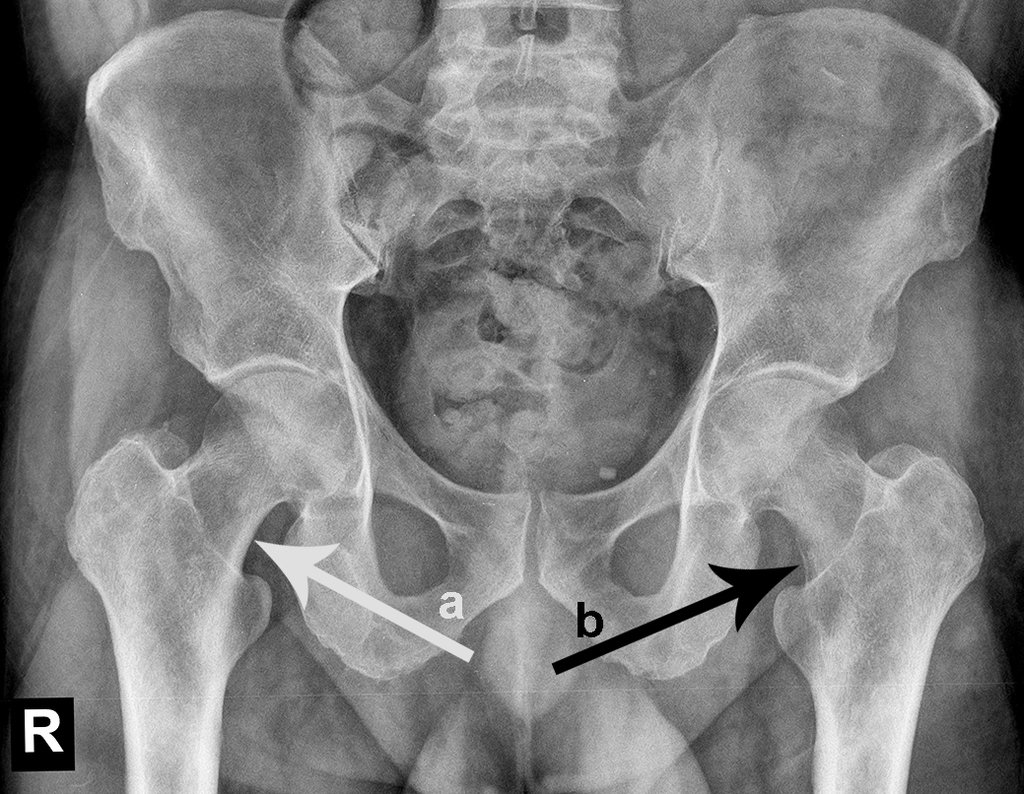
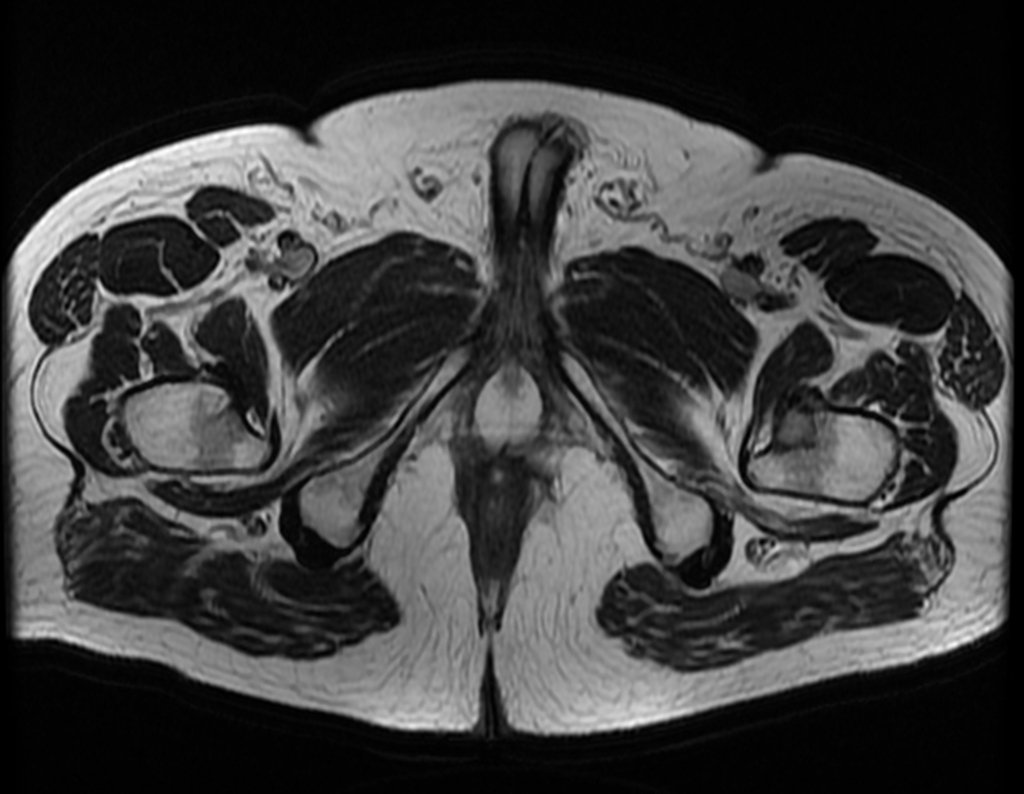
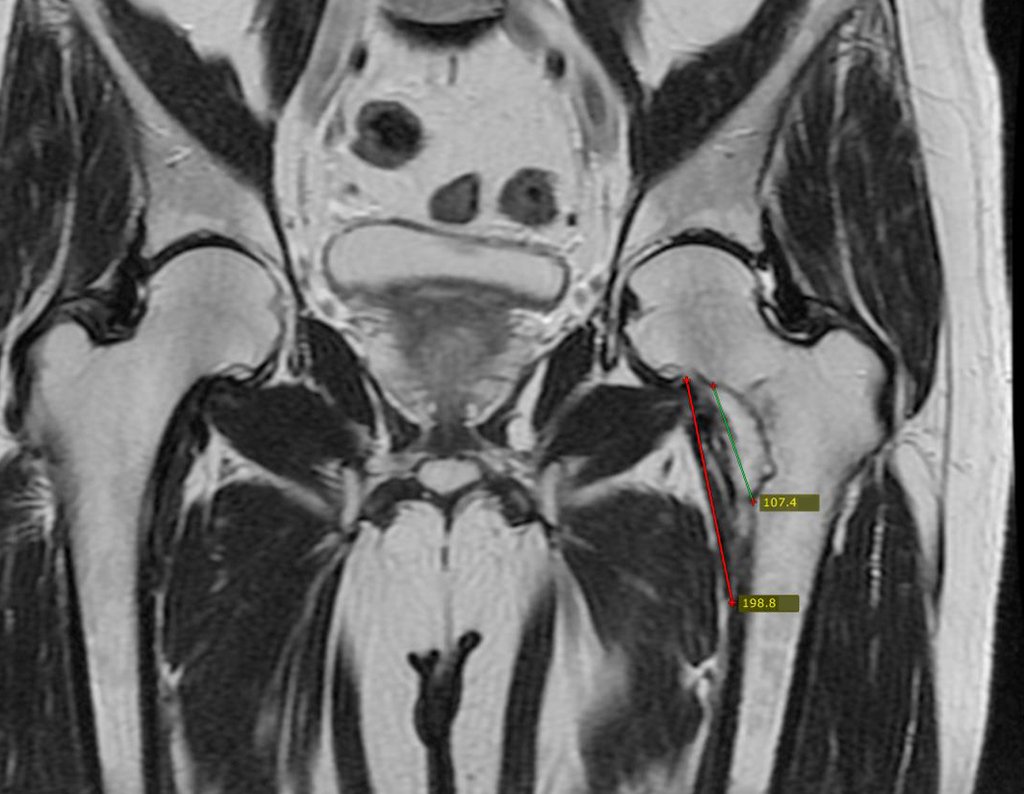
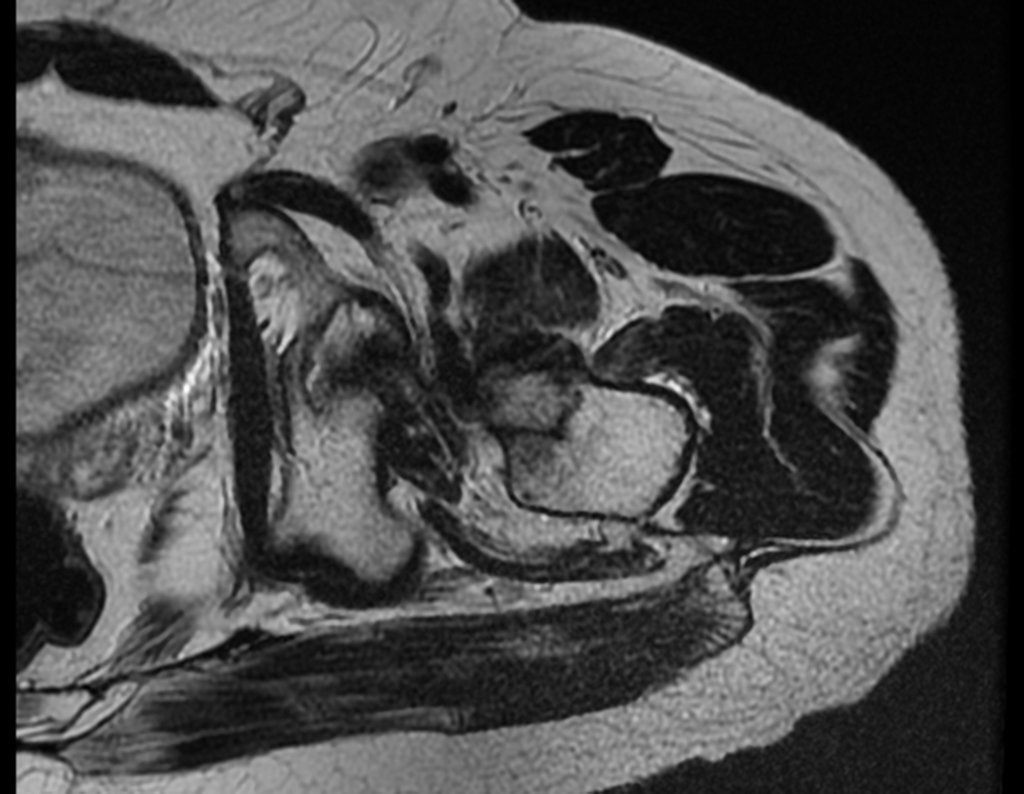
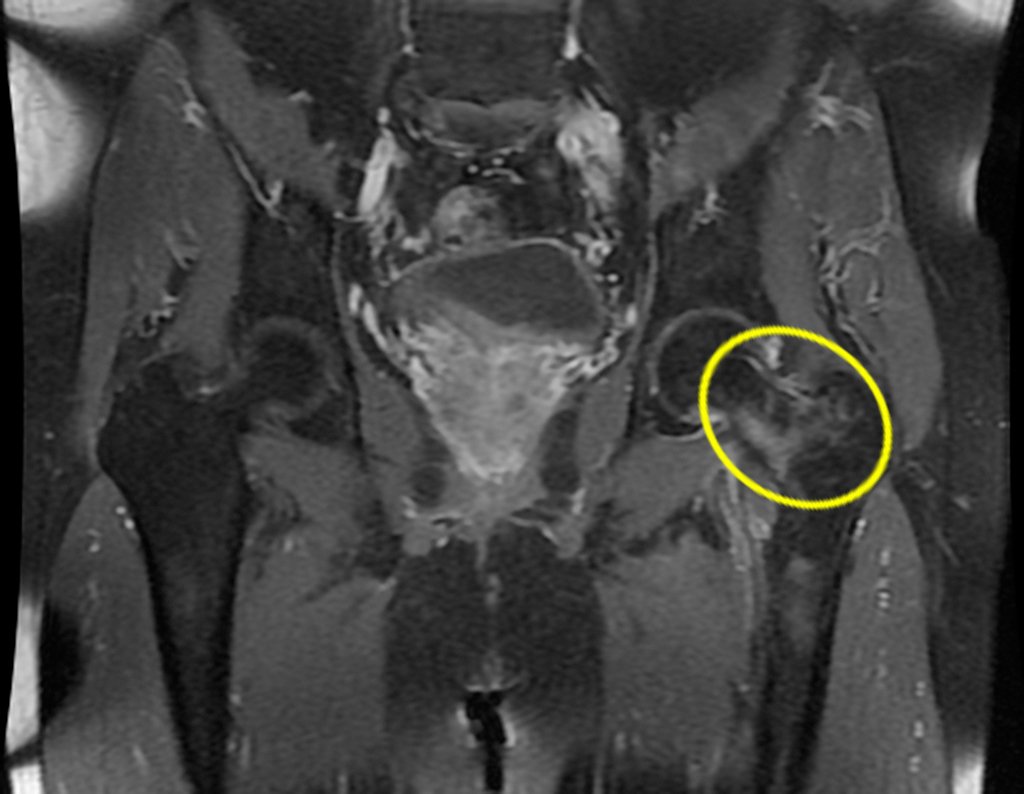
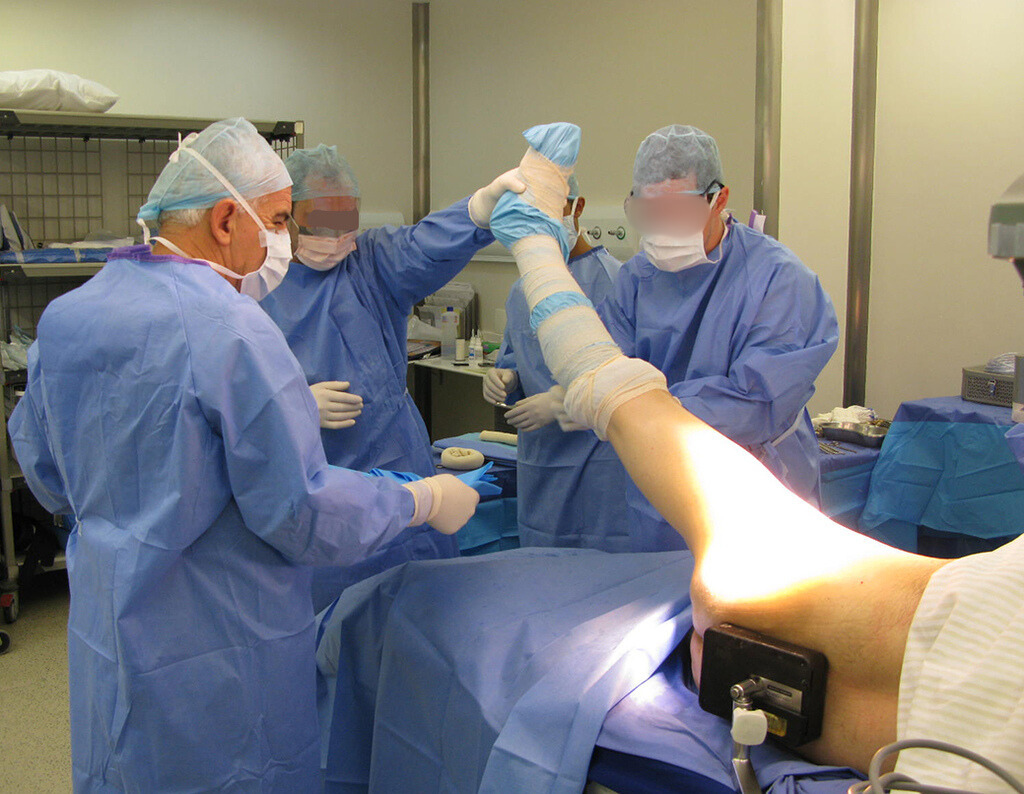
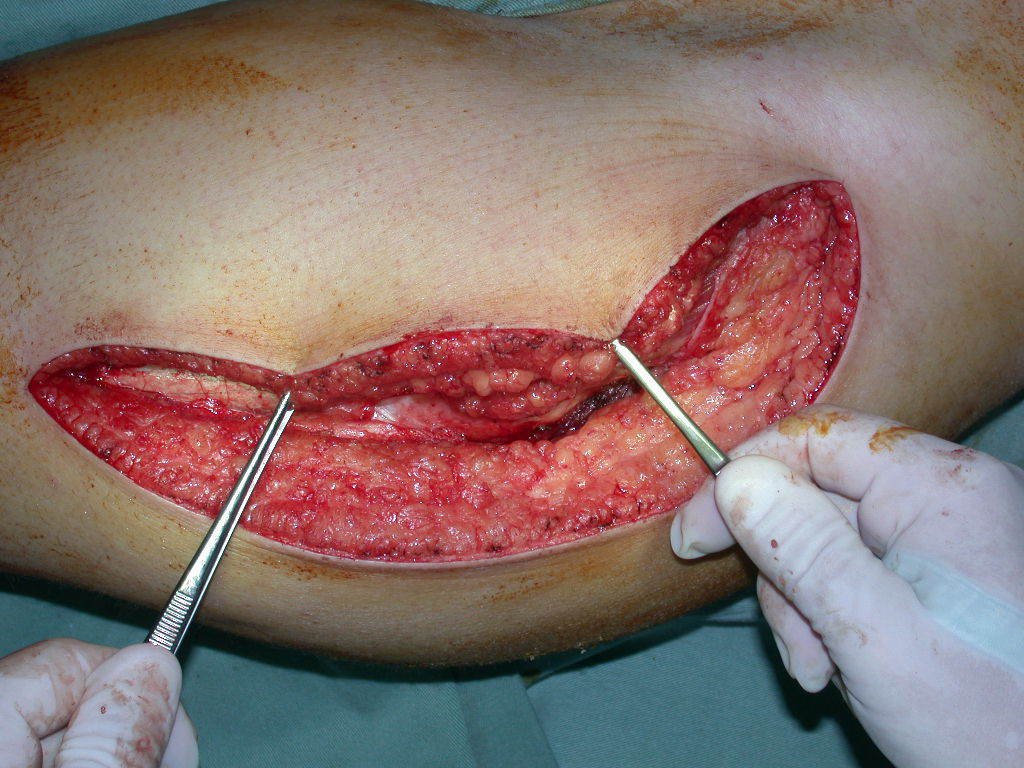
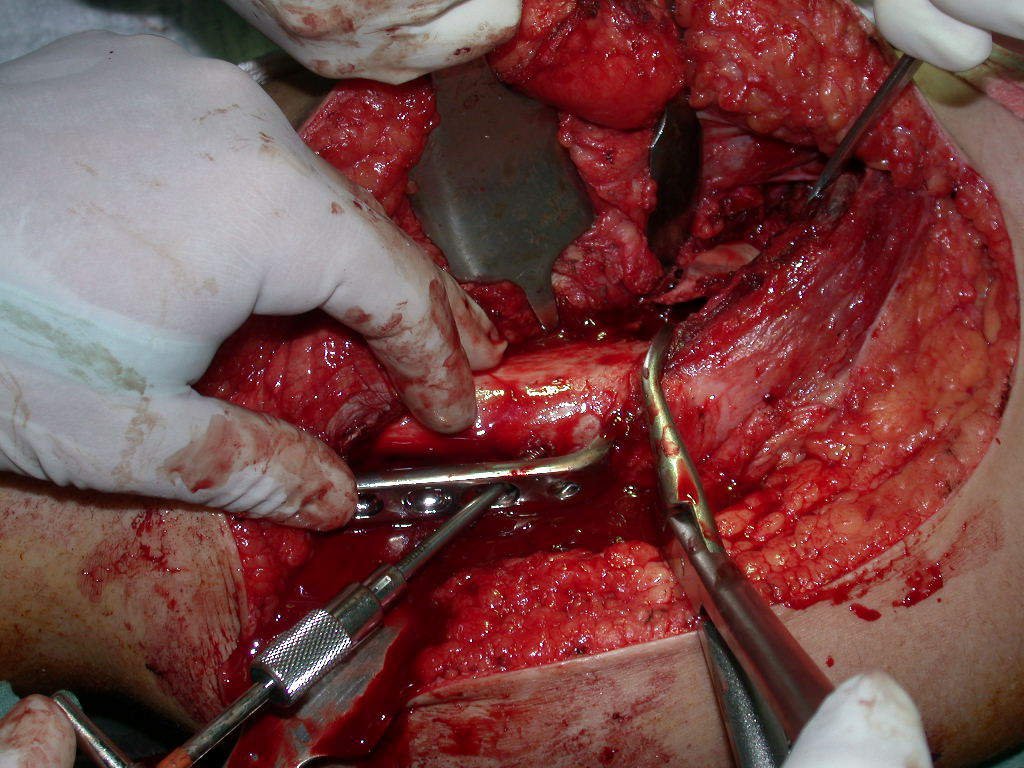
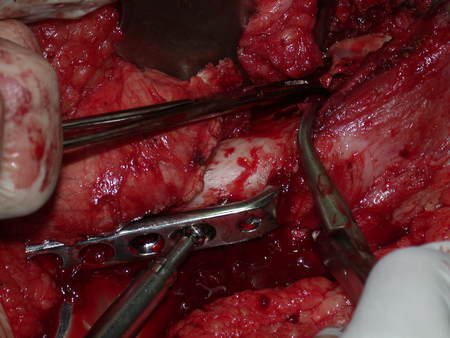
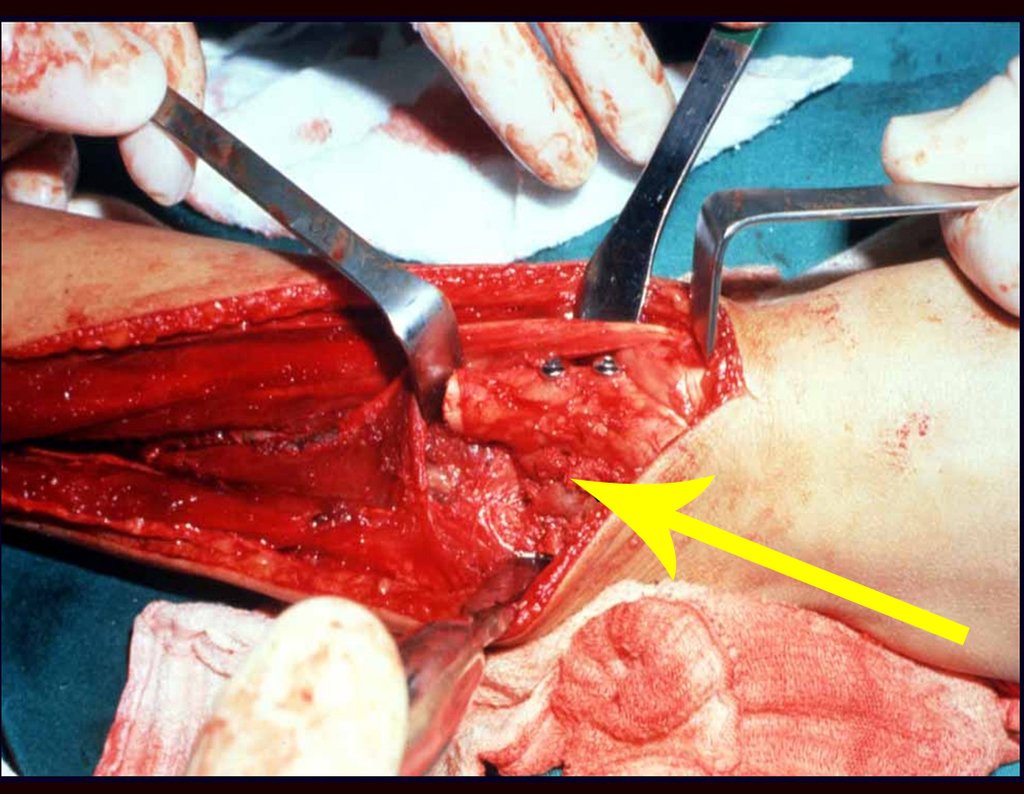
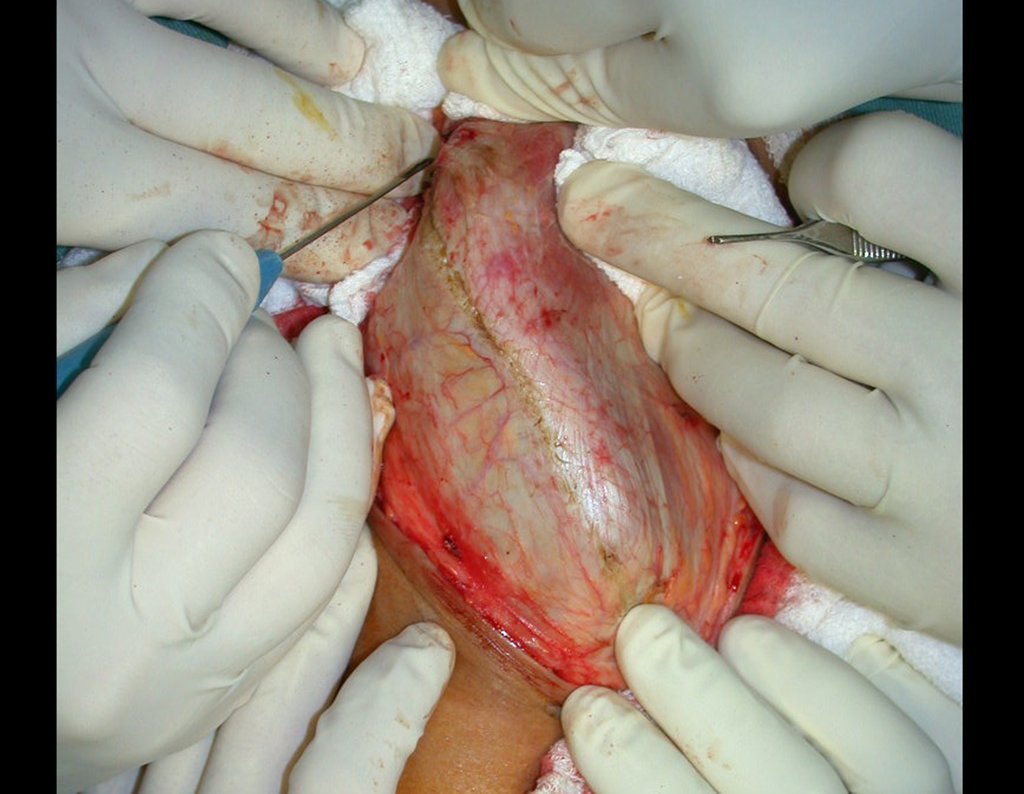
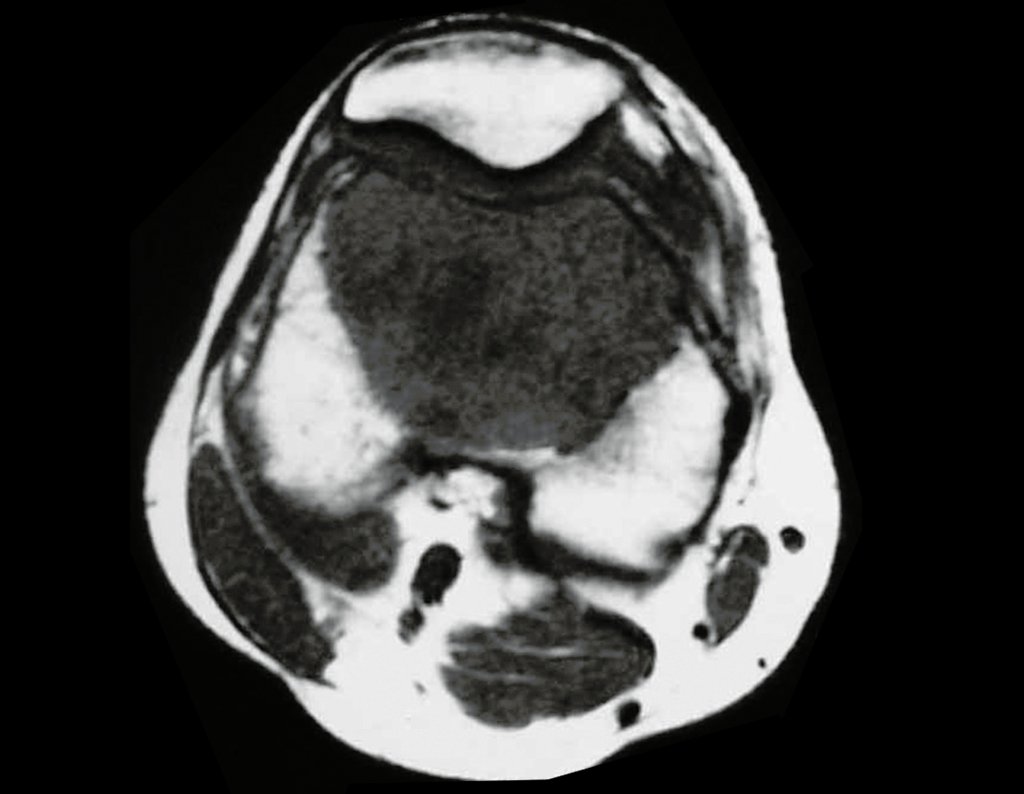
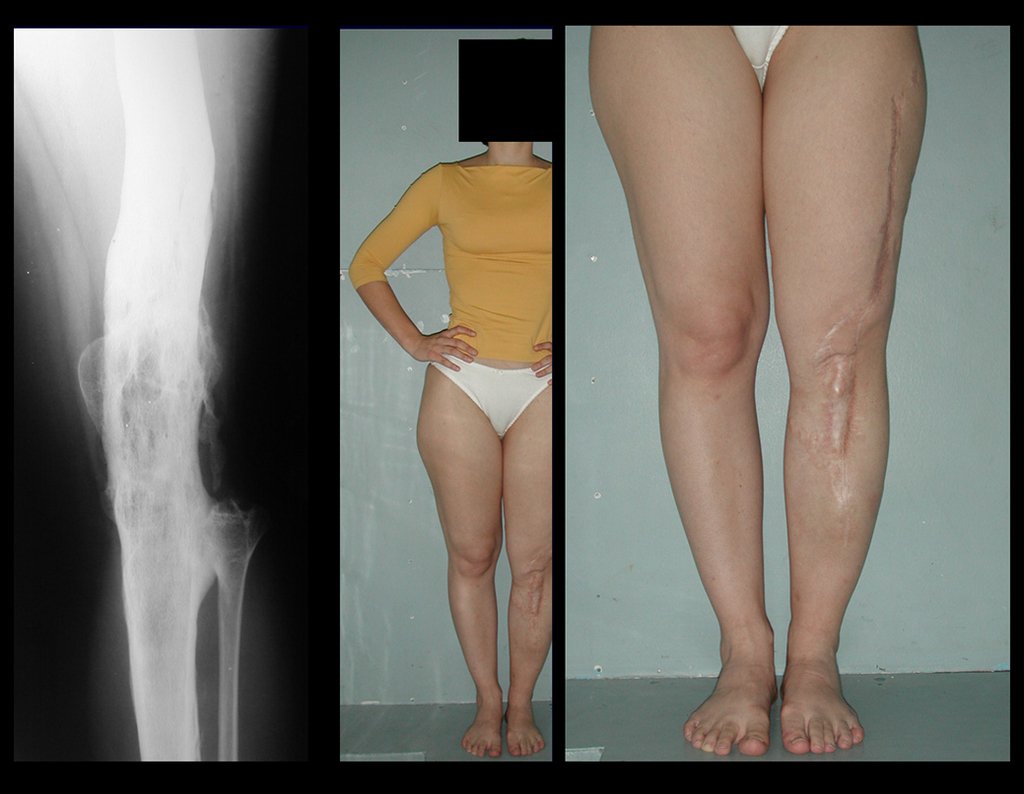
A escolha do local de biópsia deve permitir a obtenção de amostra representativa da heterogeneidade da lesão: A) COA ; B) TGC
Observa-se que a lesão apresenta áreas de conteúdo líquido (a-COA) e áreas sólidas (b-TGC).
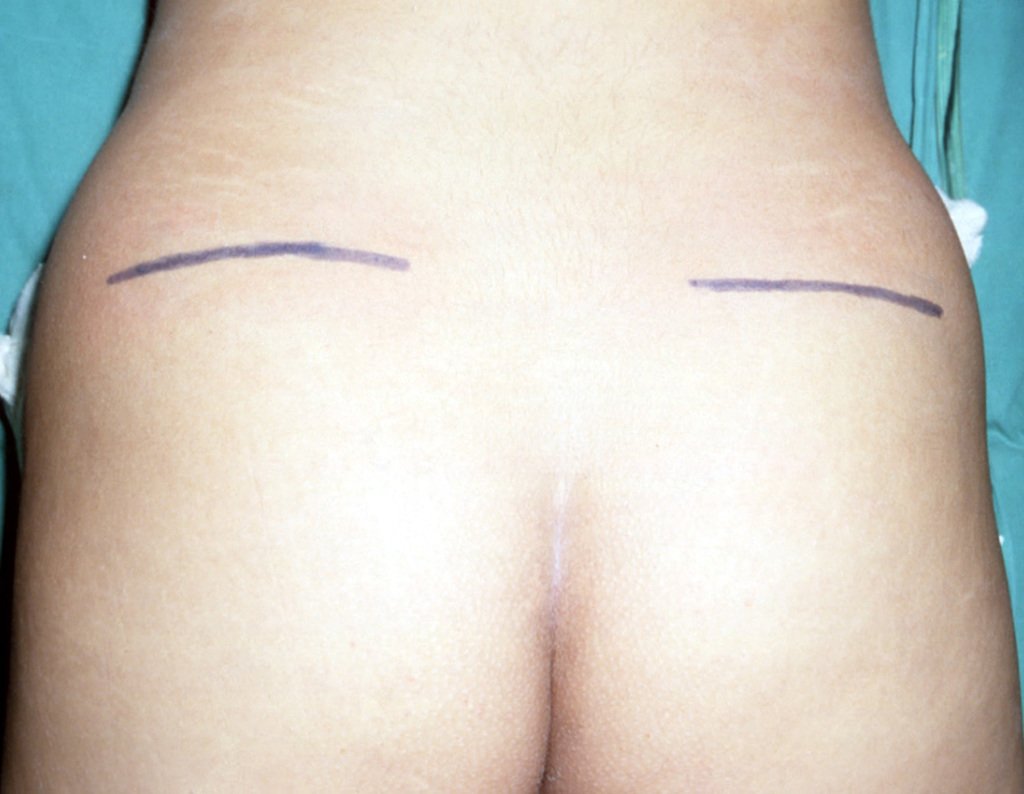
Deve-se analisar cuidadosamente a anamnese e as imagens da lesão, escolher o sitio da biópsia que permita colher amostra das diferentes áreas que se apresentam heterogêneas na ressonância magnética, para permitir o diagnóstico preciso.
O cisto ósseo aneurismático clássico tem aspecto homogêneo, enquanto as lesões tumorais citadas, quando acompanhadas de áreas de cisto ósseo aneurismático, tornam-se obrigatoriamente heterogêneas.
É mais freqüente nas três primeiras décadas de vida, com seu pico de incidência entre os 5 e 20 anos de idade, ocorrendo uma leve predominância no sexo feminino.
O paciente geralmente apresenta quadro de dor leve no local da lesão e quando o osso comprometido é superficial pode-se observar sinais inflamatórios como aumento de volume e calor. Geralmente o paciente correlaciona o início dos sintomas com algum traumatismo.
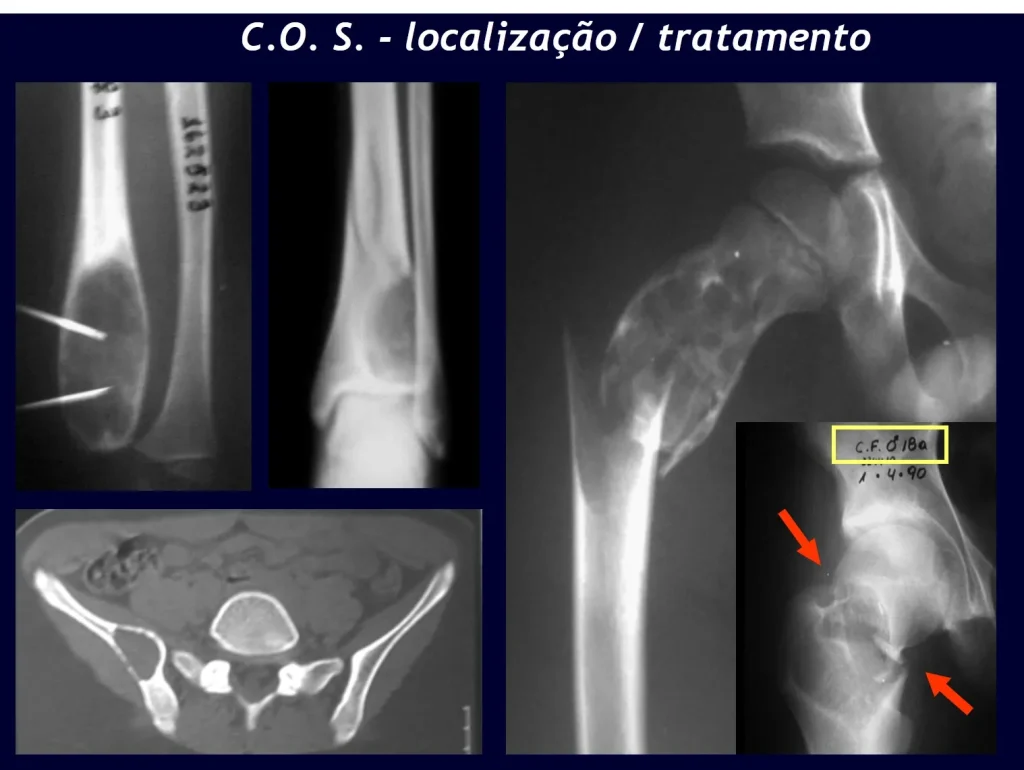
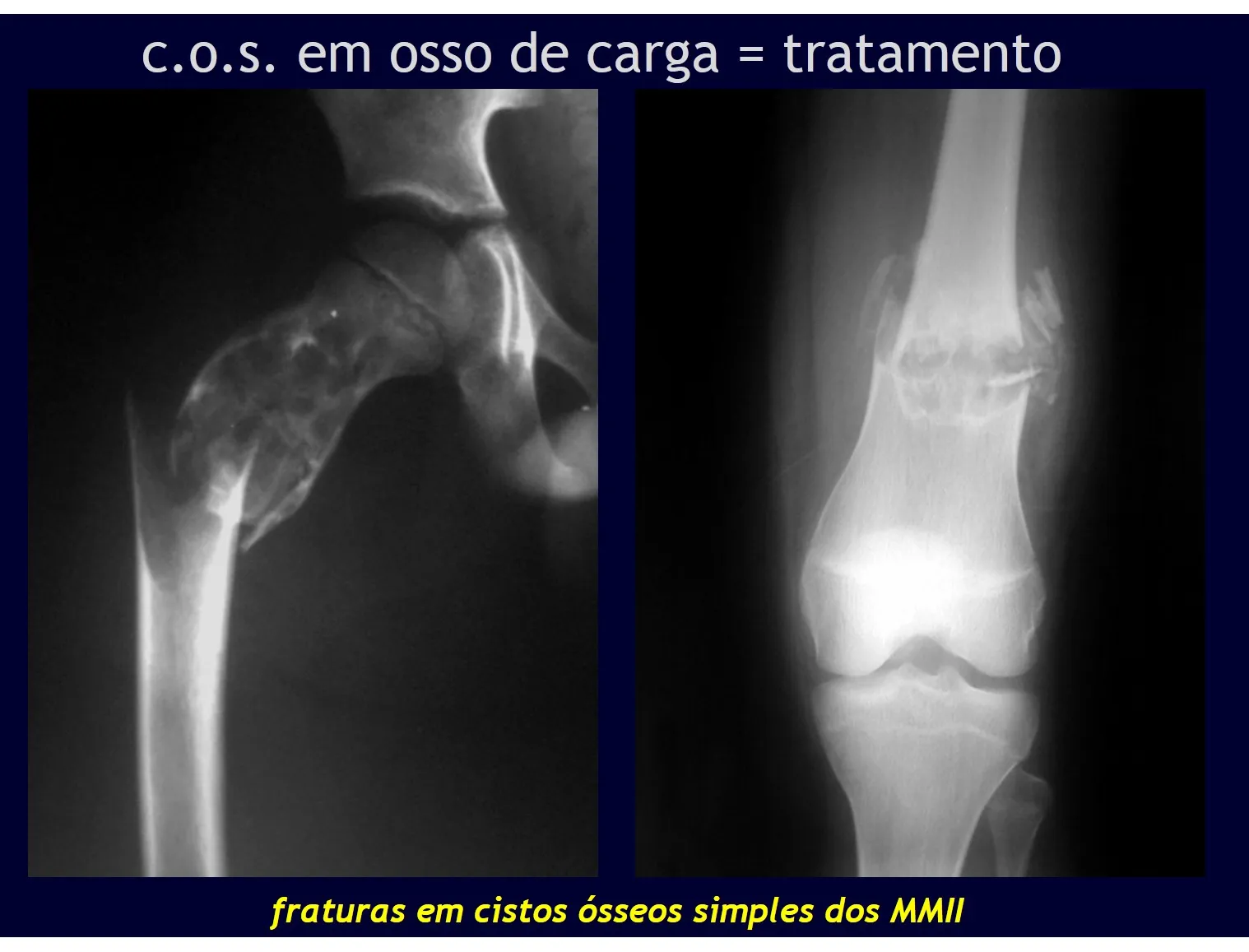
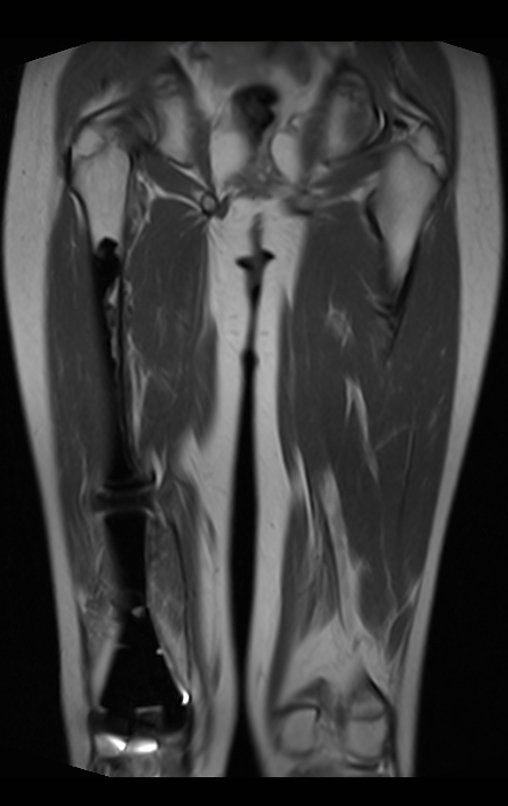
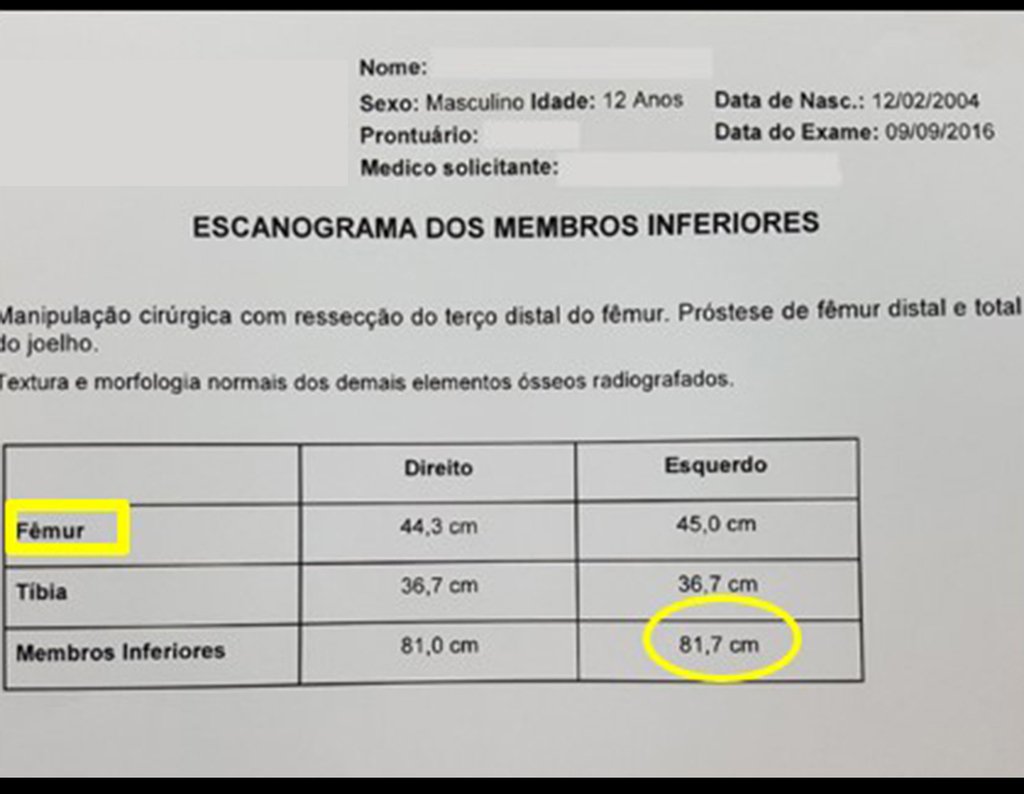
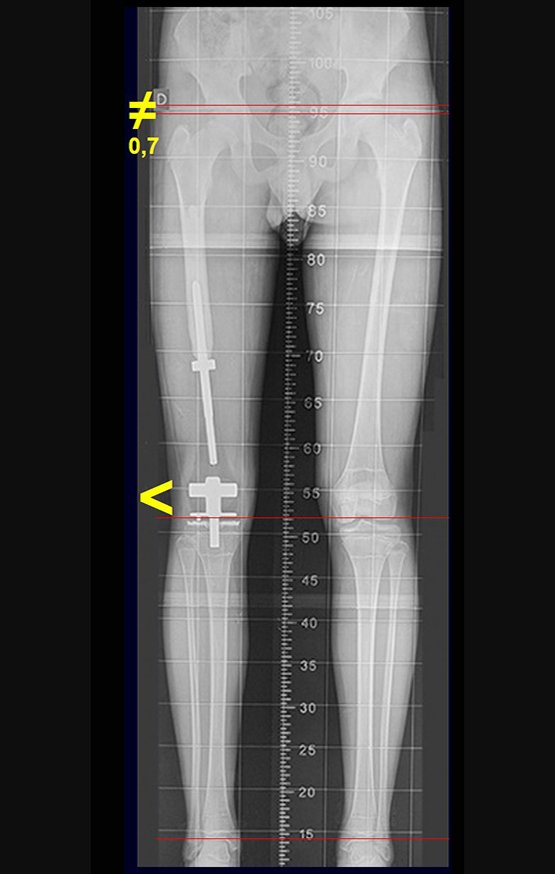
Na evolução pode haver aumento lento, progressivo ou rapidamente expansivo. Acomete qualquer osso, mais freqüentemente os membros inferiores (tíbia e fêmur representando 35% dos casos) e vértebras, inclusive o sacro e na pelve principalmente o ramo iliopúbico. Podem mimetizar sintomas articulares quando se localizam na epífise. O comprometimento na coluna vertebral pode ocasionar sintomas neurológicos compressivos, apesar de na maioria dos casos acometer as estruturas posteriores.
OBJETIVOS
Ao final da leitura deste capítulo, o leitor poderá:
- conhecer o grupo de lesões pseudo-tumorais;
- caracterizar o cisto ósseo aneurismático típico;
- determinar os exames de imagem necessários para o esclarecimento da lesão;
- fazer o diagnóstico diferencial;
- escolher o melhor tratamento para cada situação.
ESQUEMA CONCEITUAL: C. O. A.
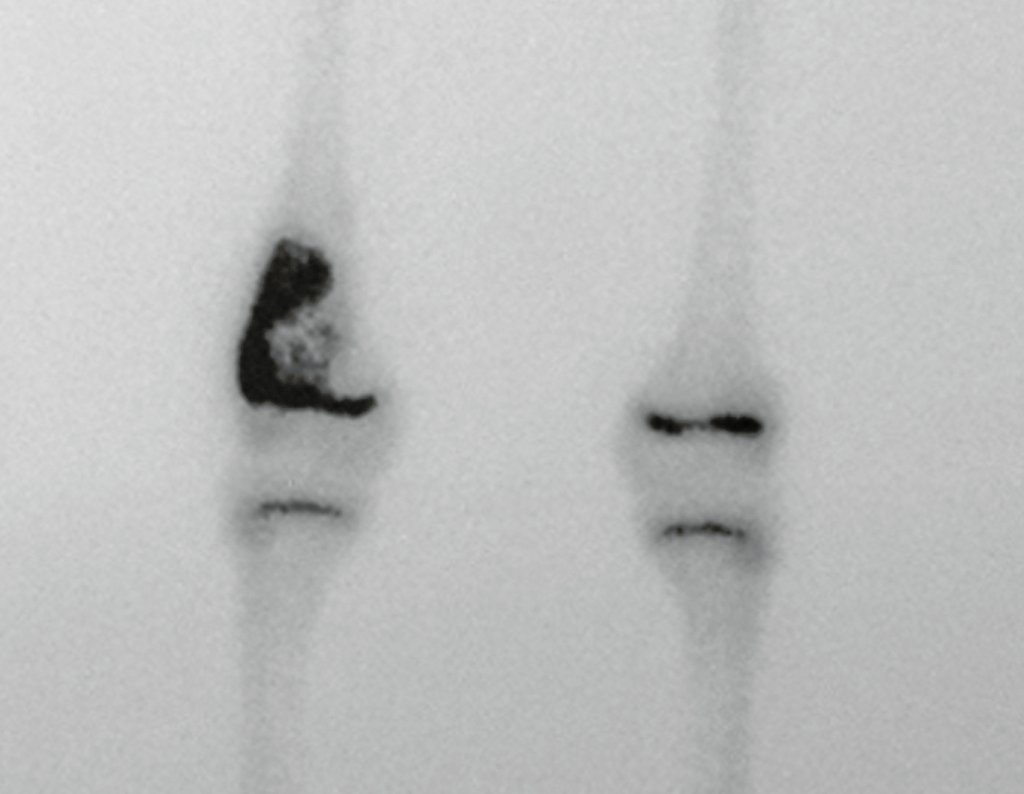
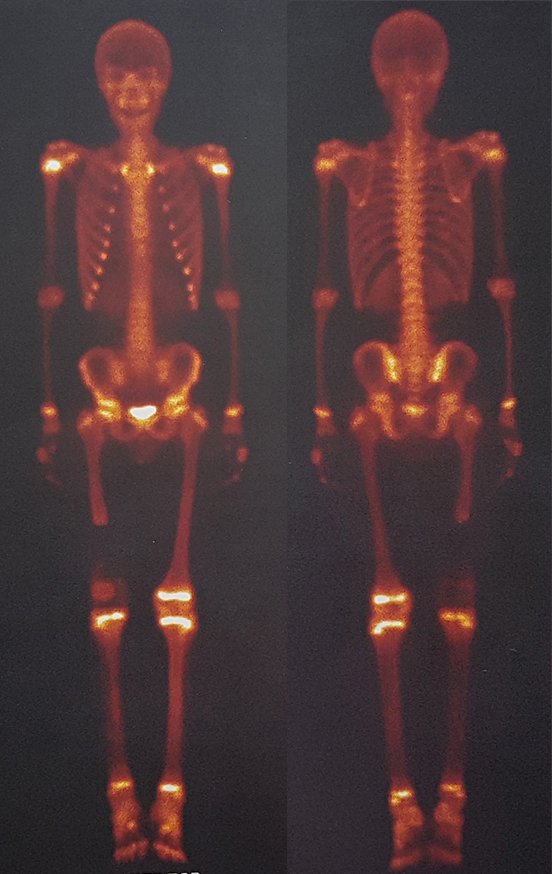
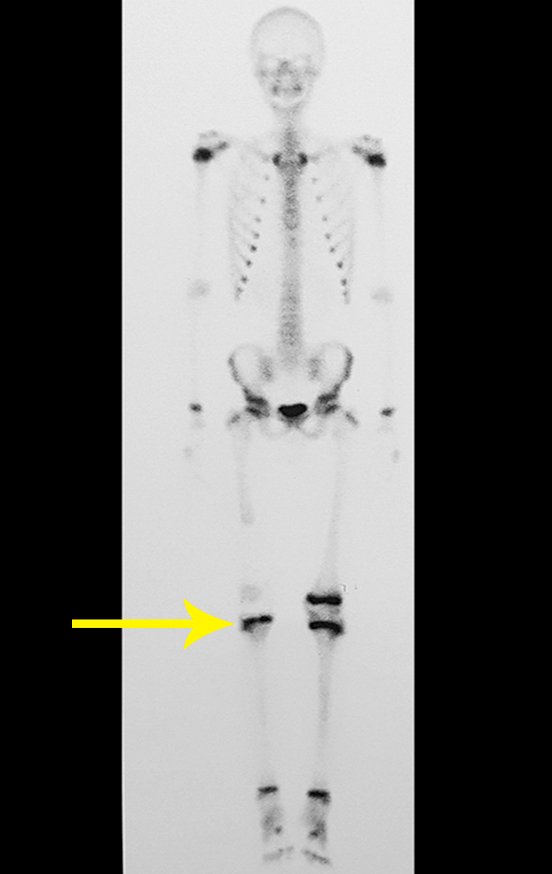
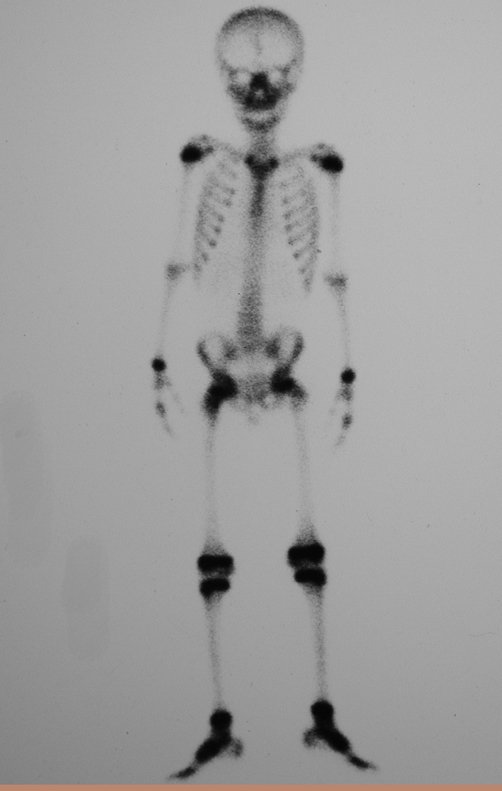
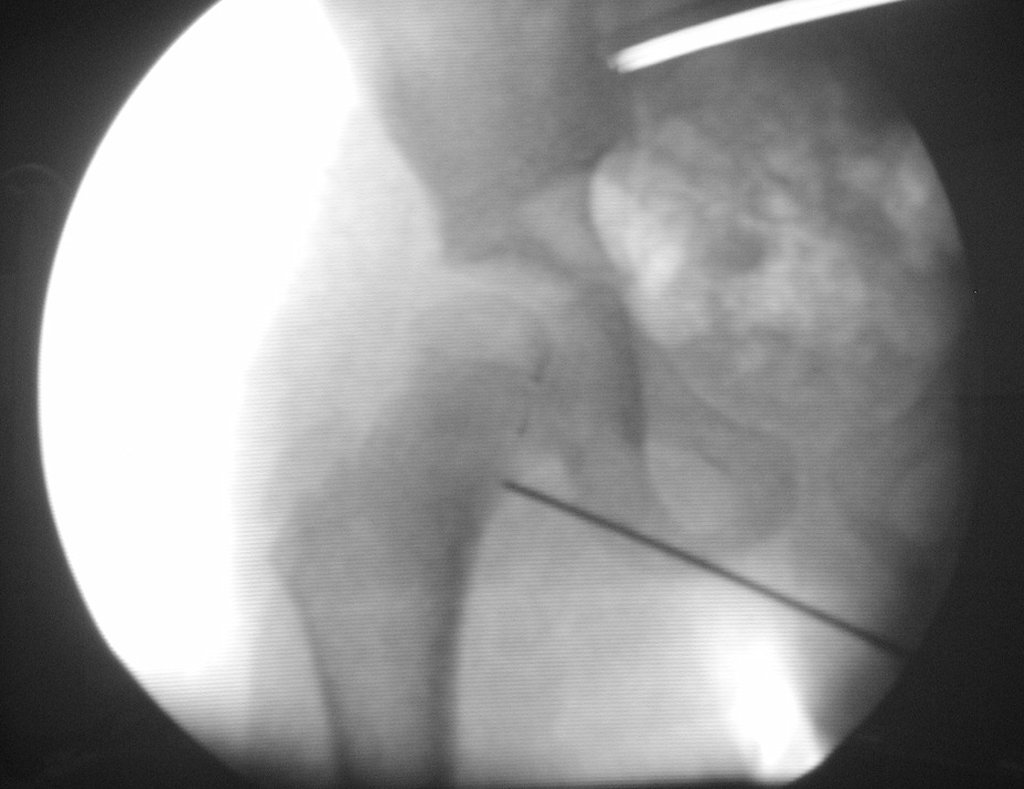
No estadiamento ósseo realizado com a cintilografia encontramos lesão única com captação discreta na periferia da lesão.
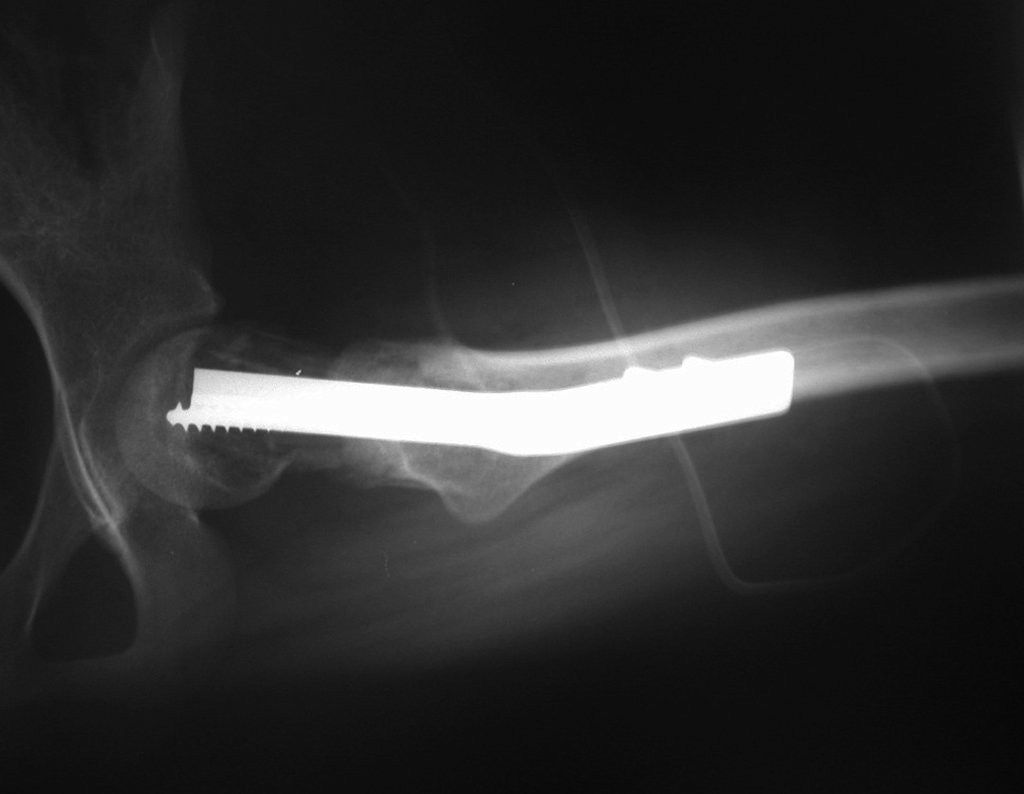
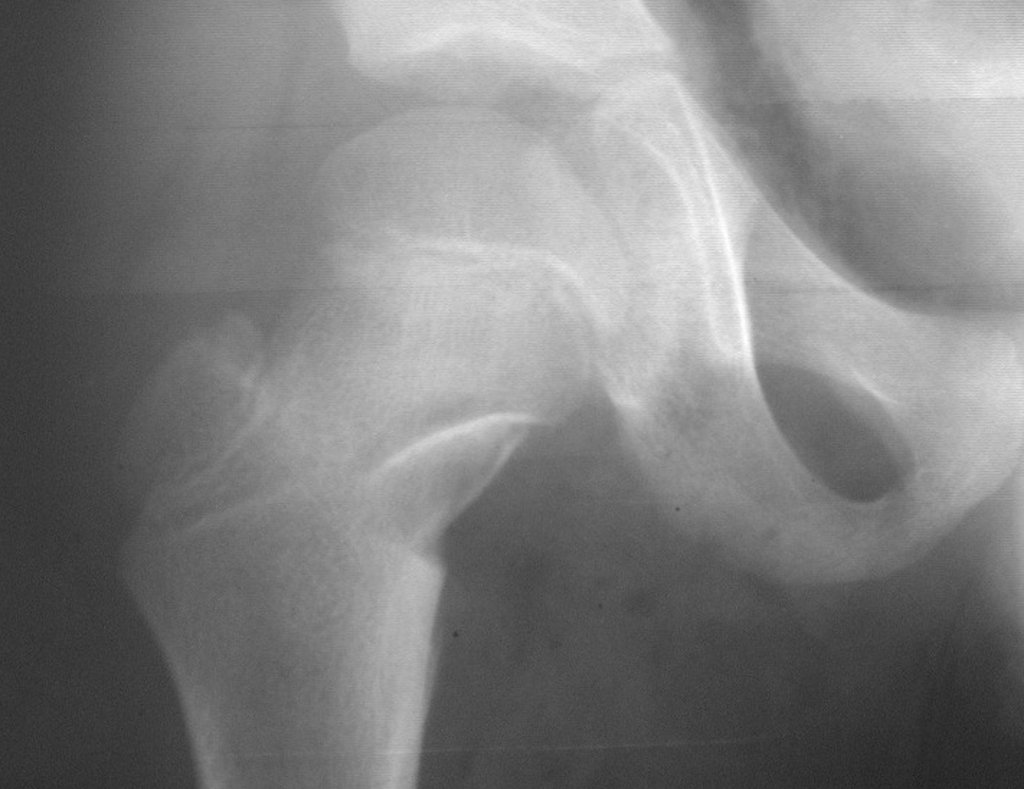
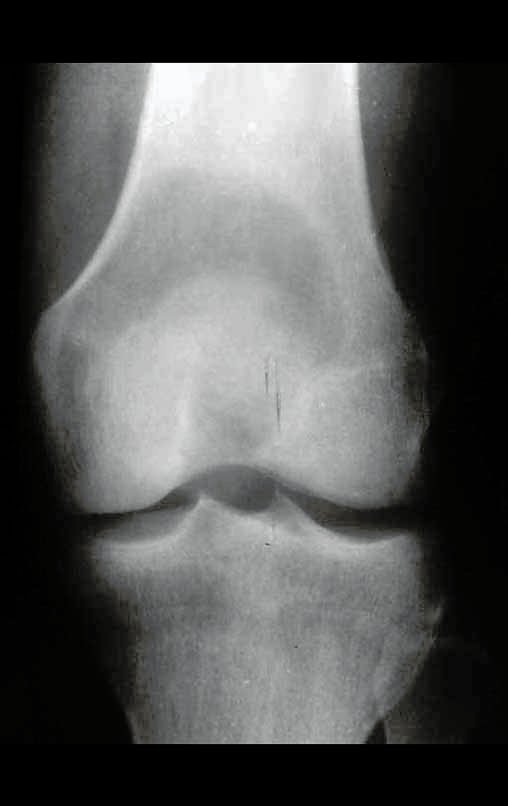
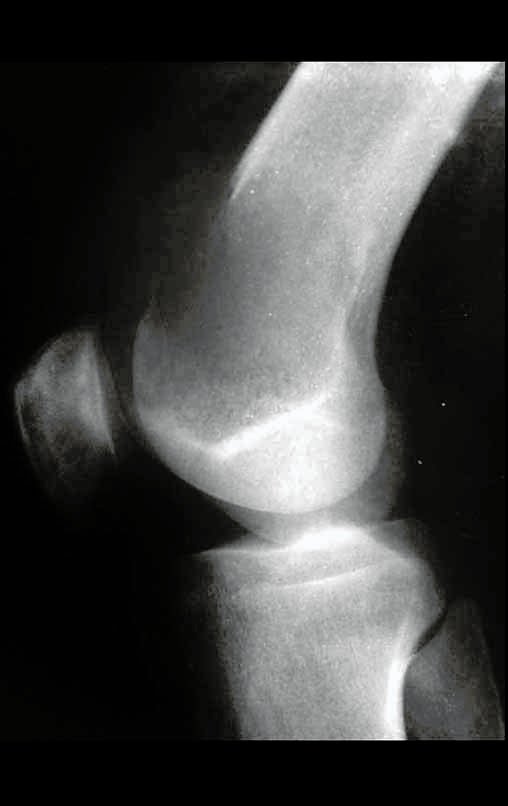
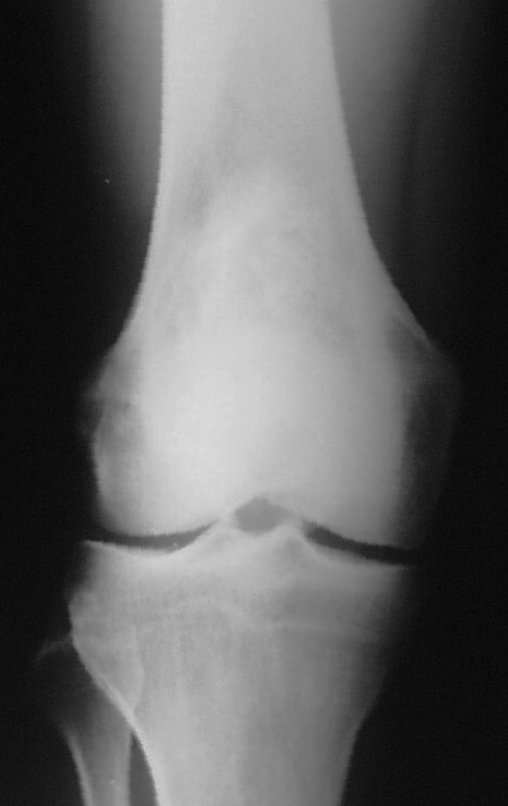
Radiograficamente apresenta-se como lesão insuflativa radiotransparente, preferencialmente na região metafisária dos ossos longos (podendo ocorrer também na epífise e diáfise), com presença de septos dispersos em todo o seu conteúdo, com aspecto “bolhoso” (ou em favo de mel), com afilamento e expansão da cortical, de localização excêntrica em 50% dos casos ou central. Podem ainda ocorrer centralmente na cortical do osso e em menos de 8% dos casos na superfície.
O aspecto radiográfico entretanto é homogêneo. Com a progressão da lesão pode ocorrer formação de triangulo de Codman, dando uma falsa impressão de invasão de tecidos moles, fato este que não ocorre pois a lesão sempre apresenta uma superfície de tecido conjuntivo que a circunscreve (pseudo-cápsula que delimita a área de lesão do osso comprometido e dos tecidos adjacentes).
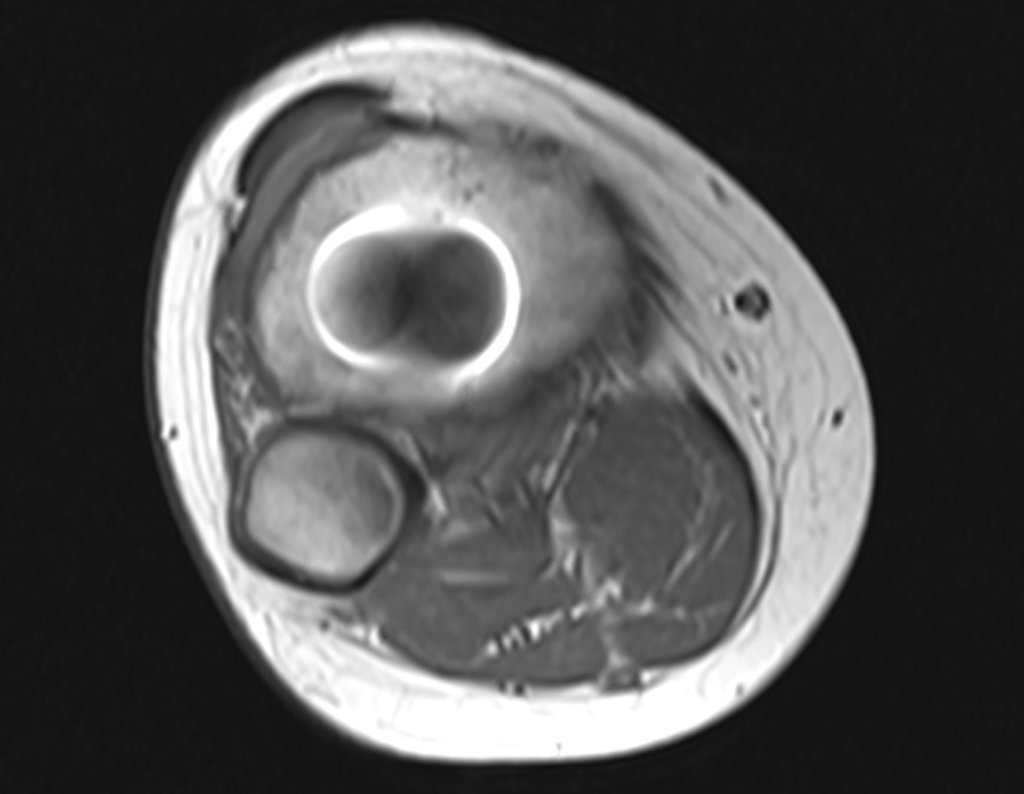
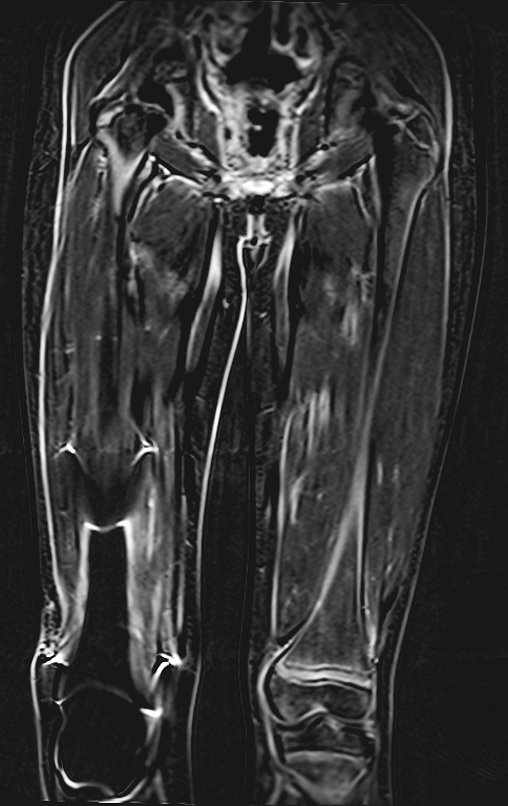
A ressonância magnética por realizar cortes em diferentes planos mostra com freqüência a presença de níveis líquidos, evidenciando as numerosas bolsas separadas pelos septos conjuntivos. O diagnóstico de cisto ósseo aneurismático na biópsia é aceito com maior tranqüilidade quando na análise da ressonância de toda a lesão não se evidencia nenhum aspecto heterogêneo. A presença de estrutura heterogenia na ressonância magnética, em que a área sólida apresenta impregnação de contraste, implica na necessidade de se obter amostra desta área para o diagnóstico, pois deve tratar-se de caso de associação de cisto ósseo aneurismático com alguma das lesões citadas.
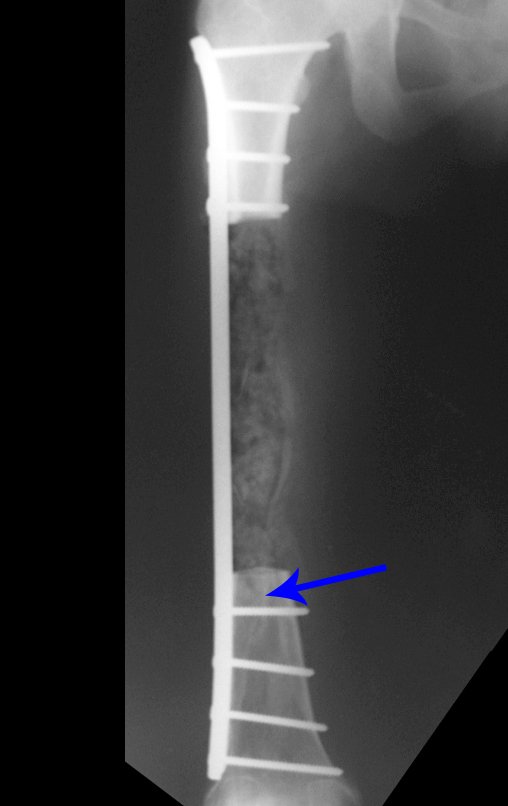
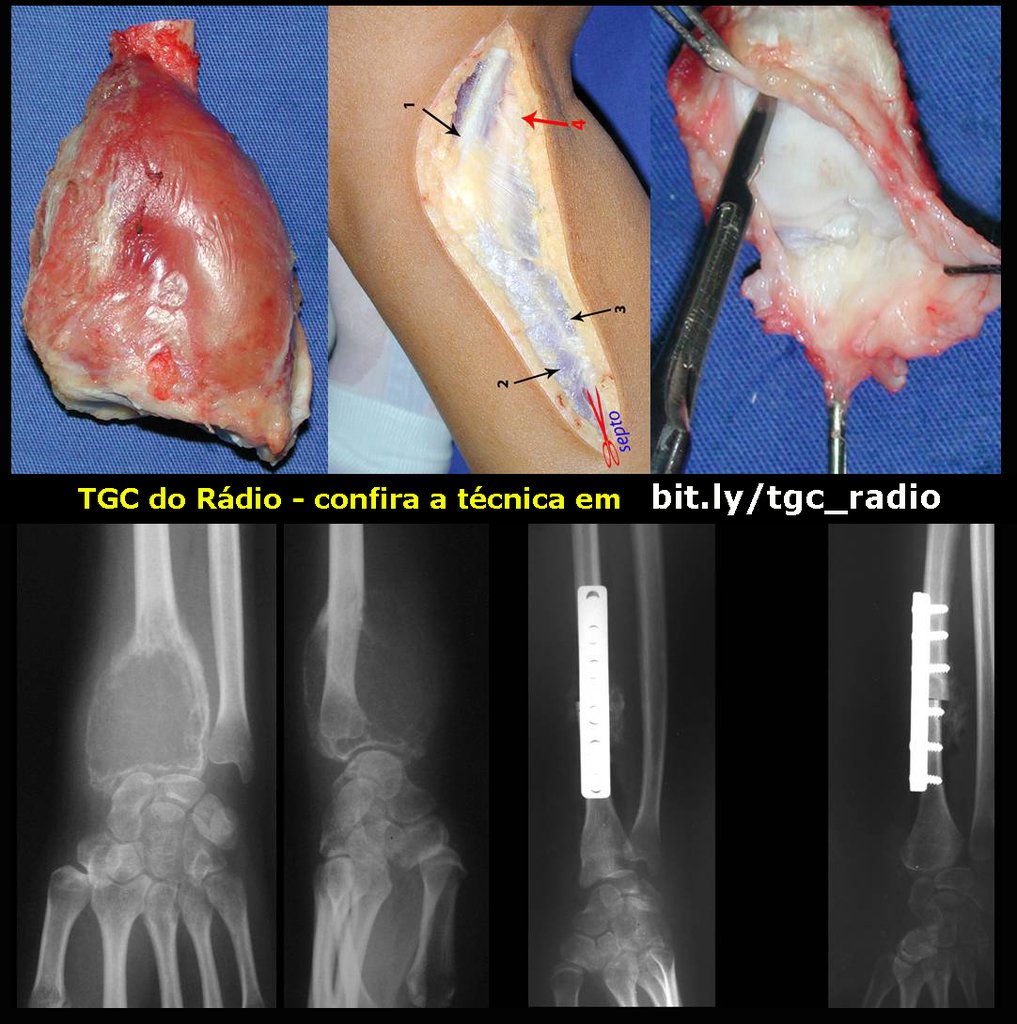
Alguns segmentos ósseos como as extremidades da fíbula, clavícula, costela, terço distal da ulna, proximal do rádio, etc podem ser reessecados, sem a necessidade de reconstrução.
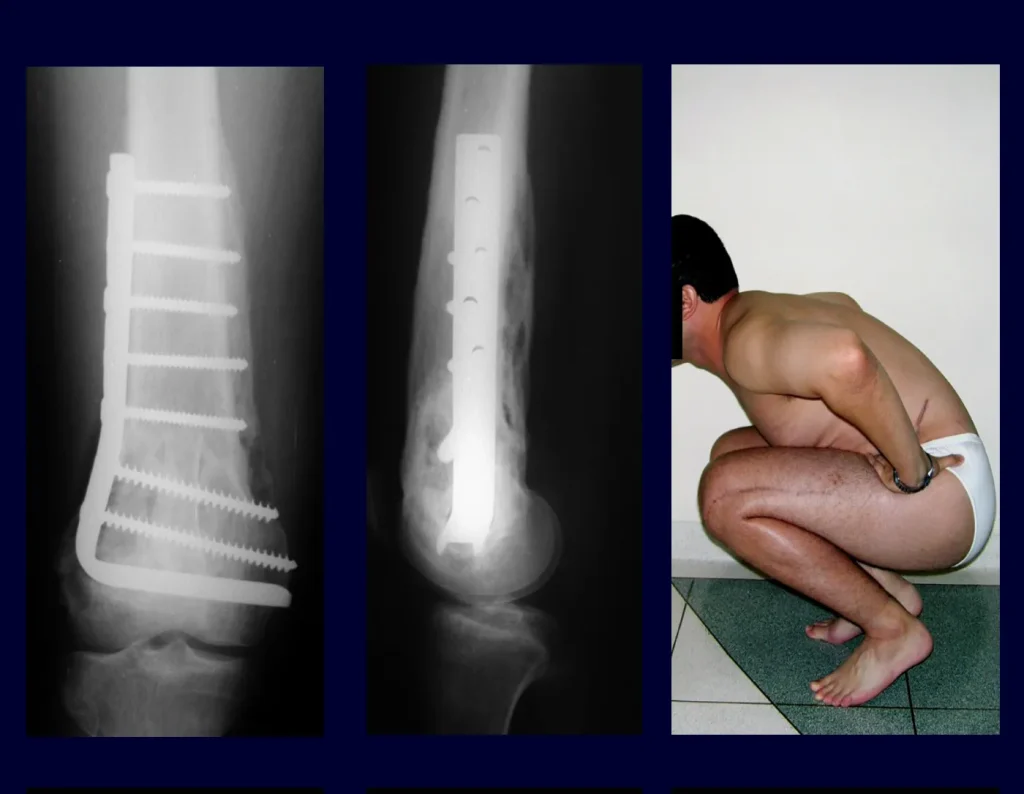
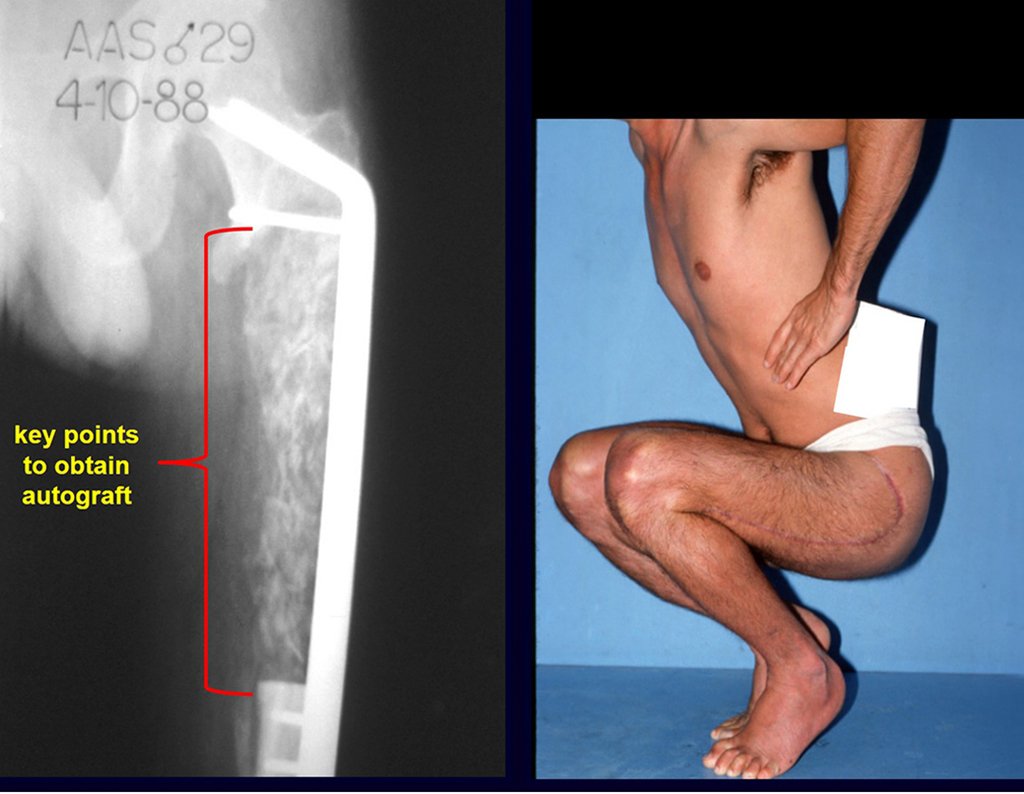
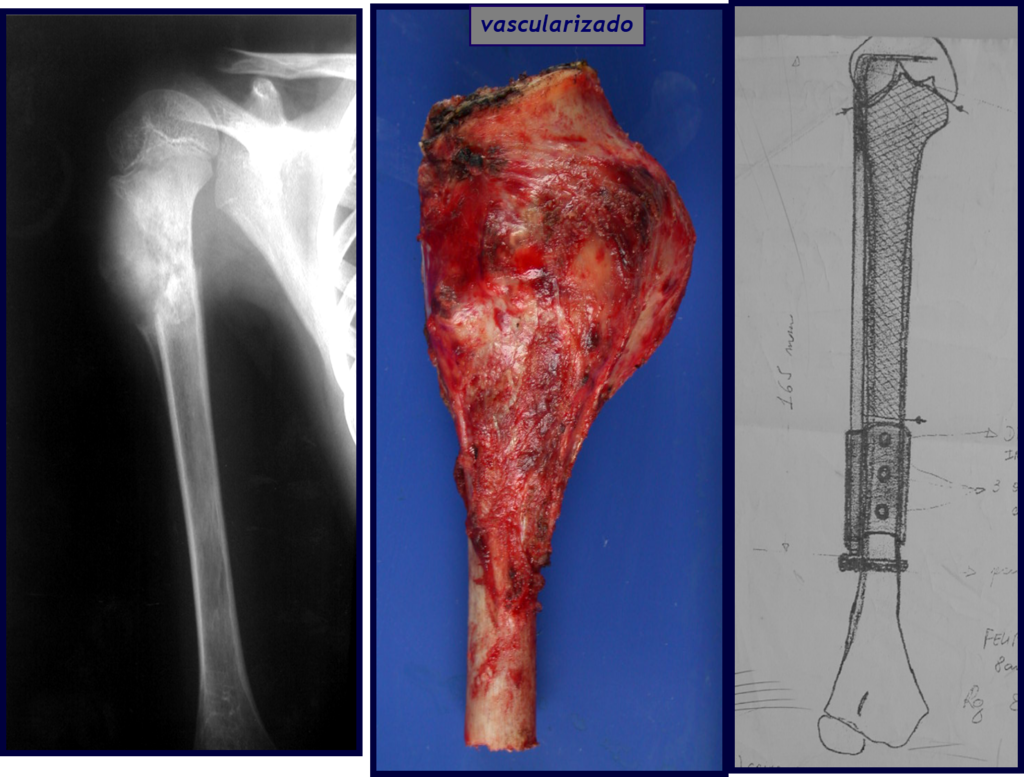
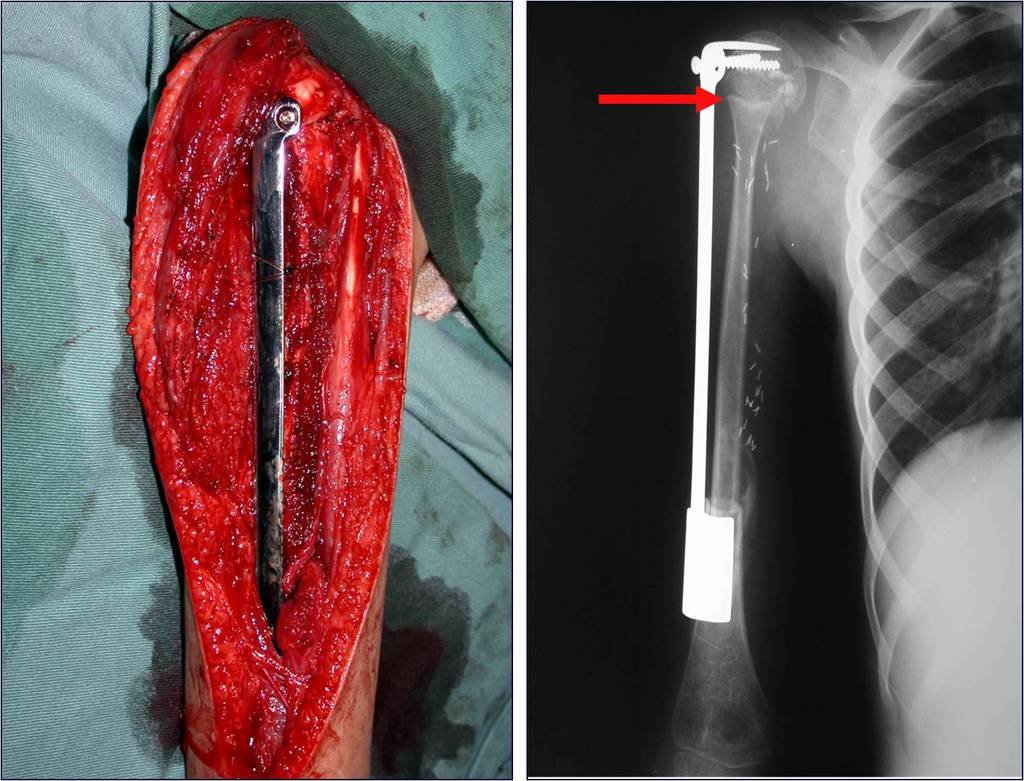
Em outras situações poderemos necessitar de reconstruções segmentares com enxerto ósseo livre ou até mesmo vascularizado ou ainda de reconstruções articulares com próteses nos casos avançados com grande compromentimento articular. Na coluna vertebral, após a ressecção da lesão, pode haver necessidade de artrodese, a fim de evitar instabilidade.
A radioterapia deve ser evitada pelo risco de malignização, entretanto tem sua indicação reservada no controle evolutivo de lesões de difícil acesso, como a coluna cervical por exemplo, ou outras situações em que a reintervenção cirúrgica não é recomendada.
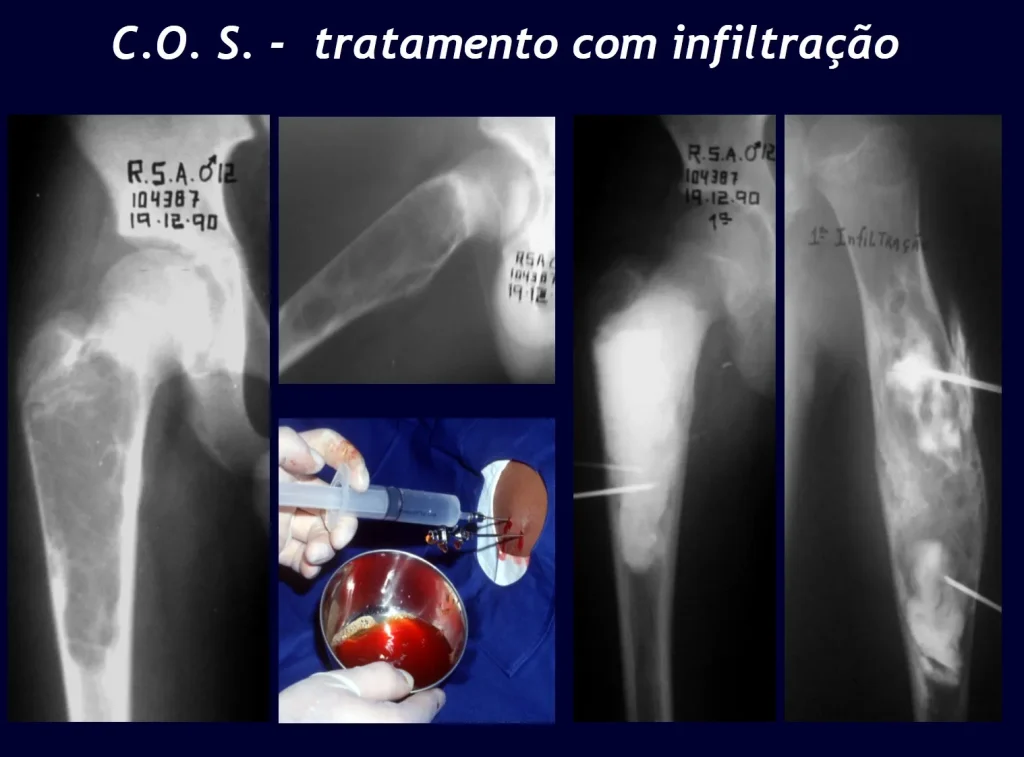
A embolização como terapia isolada é controversa. Pode entretanto ser empregada pré-operatóriamente visando minimizar o sangramento durante a cirurgia. Esta prática é mais utilizada em casos de difícil acesso, embora sua eficácia nem sempre é obtida. A infiltração com calcitonina tem sido relatada com resultado satisfatório em casos isolados.
A recidiva pode ocorrer, pois o fenômeno que originou o cisto é desconhecido e não podemos assegurar que a cirurgia o reparou. O índice de recorrencia pode atingir trinta por cento dos casos.
Questões:
1- O cisto ósseo aneurismático:
a- é uma lesão tumoral
b- é uma lesão mestastática
c- ocorre isoladamente ou acompanha outras lesões ósseas
d- é um pseudo-aneurisma
2- Dentre os diagnósticos diferenciais do COA inclui-se:
a- Condrossarcoma
b- TGC
c- Sarcoma de Ewing
d- defeito fibroso cortical
3- Segundo a classificação de Enneking o COA é:
a- lesão benigna ativa
b- lesão benigna latente
c- lesão maligna de baixo grau
d- lesão maligna de alto grau
4- Em relação ao COA é correto afirmar:
a- ocorre mais frequentemente no paciente idoso
b- apresenta células gigantes do tipo osteoclastos
c- deve preferencialmente ser tratado com ressecção ampla
d- apresenta focos de calcificação
5- O aspecto radiográfico do COA é:
a- lesão óssea condensante
b- lesão óssea heterogênia
c- lesão de rarefação óssea homogênia
d- lesão óssea sem limites precisos.
6- O tratamento preferencial do COA é:
a- curetagem intralesional
b- ressecção segmentar
c- ressecção segmentar + endoprótese
d- Artrodese
7- As lesões tumorais que mais freqüentemente apresentam áreas de cisto ósseo aneurismático são:
a- tgc; condrossarcoma; osteossarcoma e sarcoma de Ewing
b- defeito fibroso; tgc; adamantinoma e cordoma
c- osteoblastoma; condroblastoma; fibroma condromixóide e tgc;
d- osteossarcoma; condroblastoma; granuloma eosinófilo e lipoma
Bibliografia
- ALEOTTI, A.; CERVELLATTI, A.A.;BOVOLENTA, M.R.;ZAGOS,S. Et al Birbeck granules : contribution to the comprehension of intracytoplasmatic evolution. L.Submicrosc. Cytol. Pathol.,30(2):295, 1998.
- AVANZI, O.;JOILDA. F.G.;SALOMÃO, J.C.;PROSPERO, J.D. Cisto ósseo aneurismático na coluna vertebral . Rev. Brás. Ortop., 31:103,1996
- AVANZI, O.;JOILDA. F.G.;PROSPERO , J.D.;CARVALHO PIN TO, W. Tumores benignos e lesões pseudotumorais na colina vertebral . Rev. Brás. Ortop.,31:131,1996.
- BIESECKER, J.L.;HUVOS,A.G .;MIKÉ. V. Aneurisma boné cysts.A clinicopathologic study of 66 cases, Câncer , 26:615,1970
- BURACZEWSKI, J.;M Pathogenesis of aneurismal boné cyst. Ralationship between the aneurismal boné cyst and fibrous displasia of boné . Câncer , 28:116,1971.
- C.D.M. Fletcher…[et al] . Classification of tumor. Pathology and genetics of tumours of solf tissue and bone. World Health Organization
- DABSKA, M,;BURACZEWSKI, J.- Aneurismal boné cyst . Pathology, clinical course and radiologic appearance . Câncer . 23:371,1969.
- DAHLIN, D.C,;IVINS, J.C.- Benignin chondroblastoma of boné . A clinicopathology and electron microscopc study . Câncer .29:760,1972.
- DAILEY , R .; GILLILAUD, C.;McCOY, G.B. Orbital aneuriysmal boné cyst in a patient with renal carcinoma . Am. J . Ophtalm., 117:643, 1944.
- DORFMAN ,H.D.;CZERBIAK,B.Bone tumors. St. Louis,C.V.Mosby Co.,1997. P 855.
- DORFMAN ,H.D.; STEINER, G.C.;JAFFE, H.L. Vascular tumors of thr boné . Hum. Pathol.,2:349, 1971.
- JAFFE, H.L.;LICHTENSTEIN, L . Aneurismal boné cyst :obeservation on fifty cases . J.Bone Join Surg.,39 A :873, 1957.
- JAFFE, H.L.;LICHTENSTEIN, L .Benign chondroblastoma of boné . A reinterpretation of the so called calcifying or chondronaous giant cell tumor. Am J. .,18:969, 1942.
- JAFFE,H . L. Aneurismal boné cyst.Bull. Hosp. J .Dis.,11:3,1950.
- LICHTENSTEIN, L Aneurysmal boné cyst. A pathological entity commonly mistaken for giant cell tumor and occasionally for hemangioma sarcoma. Câncer, 3:279,1954.
- MARTINEZ, V.;SISSONS.H.A. Aneurysmal boné cyst.A review of 123 cases including primary lesions and those secondary to other boné pathoogy. Câncer,61:2291 , 1988.
- PROSPERO, J.D.;RIBEIRO BAPTISTA , P.P.;de Lima Jr., H. Doenças ósseas com células gigantes multinucleadas. Diagnostico diferencial. Rev. Brás. Ortop.,34:214,1999.
- RIUTTER,D.J,;VAN RUSSEL, T.H.G.;VANder VELDE, E.A. Aneuryamal boné cyst. A clinicopathological study of 105 cases. Câncer. 39:2231,1977.
- SCHAJOWICZ,F. Giant cell tumors aneuryamal boné cyst of the spine. J .Bone Joint Surg.,47B:699, 1965.
Autor : Prof. Dr. Pedro Péricles Ribeiro Baptista
Oncocirurgia Ortopédica do Instituto do Câncer Dr. Arnaldo Vieira de Carvalho
Consultório: Rua General Jardim, 846 – Cj 41 – Cep: 01223-010 Higienópolis São Paulo – S.P.
Fone:+55 11 3231-4638 Cel:+55 11 99863-5577 Email: drpprb@gmail.com